![]() .
.
Заметим, что величина ![]() не является в буквальном смысле плотностью числа частиц в фазовом объеме. Она отличается от нее на постоянный множитель
не является в буквальном смысле плотностью числа частиц в фазовом объеме. Она отличается от нее на постоянный множитель ![]() . Однако данная величина удобнее, поскольку она безразмерна (имеет размерность числа частиц), и именно она является аналогом квантовомеханического выражение (25.4). Соответственно, для этой величины мы имеем:
. Однако данная величина удобнее, поскольку она безразмерна (имеет размерность числа частиц), и именно она является аналогом квантовомеханического выражение (25.4). Соответственно, для этой величины мы имеем:
![]() .
.
Перейдем теперь к потенциальной энергии. Поскольку молекулы между собой не взаимодействуют, то потенциальную энергию тоже можно разбить на два независимых слагаемых: потенциальную энергию, связанную с координатами центра масс, и потенциальную энергию взаимодействия атомов внутри молекулы. Для первого слагаемого имеем независимое распределение по координатам центра масс молекулы:
![]() , где
, где ![]() ;
;
![]() . (26.3)
. (26.3)
Данное выражение иногда называют распределением Больцмана в узком значении этого термина (или просто формулой Больцмана). Физический смысл коэффициента нормировки ![]() очень прост. Это плотность газа в точке, где потенциальная энергия равна нулю. Если внешнее поле отсутствует:
очень прост. Это плотность газа в точке, где потенциальная энергия равна нулю. Если внешнее поле отсутствует: ![]() , то распределение будет изотропным:
, то распределение будет изотропным:
![]() .
.
Если же мы рассматриваем газ в поле силы тяжести, то плотность будет меняться только в одном направлении – вертикальном.
![]() .
.
Итак, если газ сильно разрежен, то взаимодействием между его молекулами можно пренебречь. В этом случае газ можно рассматривать как идеальный.
При сжатии газа и увеличении его плотности начнет проявляться парное взаимодействие. При еще большом сжатии скажутся тройные, четверные и т. д. столкновения. Наконец, газ начнет конденсироваться в жидкость, которая обладает уже ограниченной сжимаемостью. В жидкости межмолекулярное взаимодействие уже играет важную роль. Характер этого взаимодействия зависит от рода жидкости. По этой причине получить какие-то общее формулы для всех жидкостей не представляется возможным.
Уравнение состояния (31.5), так же, как и уравнение состояние идеального газа, дает плавное изменение давления при изменении объема и не отражает ограничение сжимаемости при конденсации газа в жидкость. Хотелось бы иметь экстраполяционную формулу, которая, с одной стороны, при низких плотностях описывала свойства идеального газа, а, с другой стороны, имела бы верхний предел для изменения плотности, и таким образом хотя бы качественно описывала переход от газа к жидкости. Естественно, получение такой формулы неоднозначно. Один из вариантов был предложен Ван-дер-Ваальсом. Приведенные ниже рассуждения не следует рассматривать как вывод. Это обоснование выражения, полученного эмпирическим путем.
Вначале попытаемся хотя бы приближенно определить зависимость ![]() . Будем считать, что температура достаточно высокая, чтобы выполнялось неравенство
. Будем считать, что температура достаточно высокая, чтобы выполнялось неравенство ![]() . Разобьем область интегрирования в равенстве (31.1) на две части – область положительных значений потенциальной энергии, и область отрицательных ее значений.
. Разобьем область интегрирования в равенстве (31.1) на две части – область положительных значений потенциальной энергии, и область отрицательных ее значений.
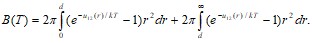
При ![]() потенциальная энергия
потенциальная энергия ![]() имеет большое положительное значение. Следовательно, экспонентой можно пренебречь по сравнению с единицей. Тогда для первого интеграла получим
имеет большое положительное значение. Следовательно, экспонентой можно пренебречь по сравнению с единицей. Тогда для первого интеграла получим
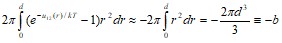 .
.
Поскольку ![]() - это диаметр молекул, то
- это диаметр молекул, то ![]() есть 4х-кратный объем молекулы.
есть 4х-кратный объем молекулы.
При ![]() выполняется неравенство
выполняется неравенство ![]() . Раскладывая экспоненту в ряд с точностью до линейного члена, получим для второго интеграла:
. Раскладывая экспоненту в ряд с точностью до линейного члена, получим для второго интеграла:
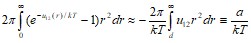 ,
,
где 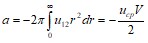 , а
, а ![]() - среднее по объему значение потенциальной энергии взаимодействия пары молекул в области сил притяжения.
- среднее по объему значение потенциальной энергии взаимодействия пары молекул в области сил притяжения.
Таким образом, имеем:
![]() , где
, где ![]() и
и ![]() .
.
Соответственно, для свободной энергии получим:
![]() .
.
Напомним, что в нашей модели газ считается еще достаточно разреженным, так что ![]() поэтому можно использовать приближение
поэтому можно использовать приближение ![]()
В результате получаем:
![]() (32.1)
(32.1)
Далее, по свободной энергии находим давление или уравнение состояния:
![]()
(32.2а)
Обычно это уравнение записывают в виде:
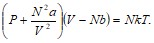 (32.2б)
(32.2б)
Это и есть уравнение Ван-дер-Ваальса.
Тема: Равновесие двух фаз.
Определим общие критерии наличия устойчивого равновесного состояния полифазной системы. Как уже отмечалось, в равновесном состоянии термодинамические функции имеют экстремум. Обозначим через ![]() значение параметра
значение параметра ![]() в равновесном состоянии, а через
в равновесном состоянии, а через ![]() его виртуальное изменение. Под виртуальным изменением понимается такое бесконечно малое изменение, которое находится в полном согласии с внешними условиями. Пусть
его виртуальное изменение. Под виртуальным изменением понимается такое бесконечно малое изменение, которое находится в полном согласии с внешними условиями. Пусть ![]() некоторая термодинамическая функция, имеющая экстремум в равновесном состоянии. Условие экстремума функции сводится к тому, чтобы ее вариация равнялась нулю:
некоторая термодинамическая функция, имеющая экстремум в равновесном состоянии. Условие экстремума функции сводится к тому, чтобы ее вариация равнялась нулю:
![]() или
или ![]()
Правда, это лишь необходимое условие. Для того чтобы при данном значении параметра был именно экстремум, а не точка перегиба, необходимо еще, чтобы вторая производная 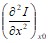 имела определенный знак. Если же окажется, что она равна нулю, то необходимо, чтобы третья производная равнялась нулю, а четвертая имела определенный знак. Заметим, что термодинамические функции могут иметь несколько экстремумов требуемого типа. Состояние, отвечающее абсолютному экстремуму, называется стабильным, или абсолютно устойчивым. Состояние, отвечающее локальному экстремуму, называется метастабильным. Система не может вечно находиться в метастабильном состоянии. Рано или поздно, под воздействием флуктуаций, она переходит в стабильное состояние. Другое дело, что на практике время перехода из метастабильного состояния в стабильное может быть настолько большим, что первое практически можно считать стабильным.
имела определенный знак. Если же окажется, что она равна нулю, то необходимо, чтобы третья производная равнялась нулю, а четвертая имела определенный знак. Заметим, что термодинамические функции могут иметь несколько экстремумов требуемого типа. Состояние, отвечающее абсолютному экстремуму, называется стабильным, или абсолютно устойчивым. Состояние, отвечающее локальному экстремуму, называется метастабильным. Система не может вечно находиться в метастабильном состоянии. Рано или поздно, под воздействием флуктуаций, она переходит в стабильное состояние. Другое дело, что на практике время перехода из метастабильного состояния в стабильное может быть настолько большим, что первое практически можно считать стабильным.
То, какой вид критерия устойчивости будет иметь место, зависит от конкретных условий. Рассмотрим несколько примеров для простой ![]() системы.
системы.
1. Если система изолирована, и имеет фиксированные значения энергии, объема и числа частиц, то в устойчивом равновесном состоянии энтропия имеет максимум. Соответственно, наш критерий будет следующим:
![]()
![]()
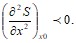
Начнем с рассмотрения двухфазной ![]() -системы. Отметим, что задание
-системы. Отметим, что задание ![]() - параметров такой системы еще не полностью определяет ее состояние. Существует еще одна степень свободы, связанная с количеством вещества в каждой фазе. В общем случае, при произвольных значениях
- параметров такой системы еще не полностью определяет ее состояние. Существует еще одна степень свободы, связанная с количеством вещества в каждой фазе. В общем случае, при произвольных значениях ![]() -параметров, состояние системы не будет равновесным, и будет происходить переход вещества из одной фазы в другую. (Разумеется, мы предполагаем, что обе фазы состоят из одного и того же вещества). Подобные переходы называют фазовыми переходами. Найдем условие, которому должны удовлетворять параметры системы, чтобы она находилась в равновесии.
-параметров, состояние системы не будет равновесным, и будет происходить переход вещества из одной фазы в другую. (Разумеется, мы предполагаем, что обе фазы состоят из одного и того же вещества). Подобные переходы называют фазовыми переходами. Найдем условие, которому должны удовлетворять параметры системы, чтобы она находилась в равновесии.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 |




