Таким образом, тепловая машина включает себя три основных частей. Это нагреватель, рабочее тело и холодильник.
Тема: III закон термодинамики. Термодинамические функции.
После того, как мы установили закономерности поведения макросистем, состоящих из большого числа микрочастиц, дальнейшее их изучение можно вести термодинамическими методами, т. е. отвлекаясь от внутренней структуры макросистем, и основываясь только на их макропараметрах.
Микросостояние системы может характеризоваться множеством различных параметров, но не все они независимы. Число независимых параметров ![]() однозначно определяющих микросостояние системы, будем называть, числом степеней свободы макросистемы. Не следует путать это, понятие с числом степеней свободы
однозначно определяющих микросостояние системы, будем называть, числом степеней свободы макросистемы. Не следует путать это, понятие с числом степеней свободы ![]() микросостояния. Последняя величина очень большая. В то время как
микросостояния. Последняя величина очень большая. В то время как ![]() величина маленькая, и составляет всего несколько единиц. Напомним, что макропараметры определяют поведение системы как целого, а степени свободы микросостояния - поведение каждой микрочастицы.
величина маленькая, и составляет всего несколько единиц. Напомним, что макропараметры определяют поведение системы как целого, а степени свободы микросостояния - поведение каждой микрочастицы.
Среди различных зависимостей макропараметров друг от друга важное место занимают уравнения состояния. Так называется любая зависимость внутреннего параметра равновесного состояния от температуры и внешних параметров. Различают два вида уравнений состояния: термическое и калорическое.
В термическом уравнении роль внутреннего параметра играет обобщенная сила, в калорическом уравнении эту роль играет внутренняя энергия. Например, для идеального газа эти уравнения выглядят как:
Термическое уравнение: ![]()
Калорическое уравнение:![]() .
.
В термодинамике уравнения состояния не выводятся. Они получаются эмпирическим путем, на основе обобщения опытных данных. В статистической физике эти уравнения получаются как следствие более общих положений.
В уравнении состояния, в качестве независимых переменных, можно выбрать, любые ![]() параметров, как внешних, так и внутренних. Главное, чтобы они были независимы. Их выбор определяется удобством рассмотрения конкретной задачи. При этом большую вспомогательную роль играют так называемые термодинамические потенциалы, или характеристические функции. Термодинамический потенциал-это функция параметров системы, удовлетворяющая ряду следующих требований:
параметров, как внешних, так и внутренних. Главное, чтобы они были независимы. Их выбор определяется удобством рассмотрения конкретной задачи. При этом большую вспомогательную роль играют так называемые термодинамические потенциалы, или характеристические функции. Термодинамический потенциал-это функция параметров системы, удовлетворяющая ряду следующих требований:
1) Она должна быть однозначной функцией состояния системы. Т. е. каждому состоянию системы должно соответствовать одно и только одно значение термодинамического потенциала.
2) Она должна быть аддитивной функцией. Это означает, что каждое слагаемое должно содержать только один аддитивный множитель. Остальные множители могут содержать только интенсивные параметры.
3) Производные от этих функций по независимым параметрам должны иметь простой физический смысл.
4) Как правило, равновесным состояниям при определенных условиях соответствует экстремум функции, а изменение самой функции определяет работу процесса или количество переданной теплоты.
Примеры таких функций мы уже рассматривали. Это энергия и энтропия. Прежде всего, их значение однозначно определяется состоянием системы, и они являются аддитивными величинами.
Рассмотрим другие характеристические функции. Наибольшее распространение имеют функции систем, одним из параметров которых является объем. В дальнейшем этот параметр мы будем выделять отдельно. Вначале рассмотрим случай, когда объем является единственным внешним параметром, и состояние системы может быть задано величинами ![]() и
и ![]() . Пусть процесс протекает при постоянном давлении
. Пусть процесс протекает при постоянном давлении ![]() . Изменение энергии равно:
. Изменение энергии равно:
![]()
Отсюда, учитывая, что ![]() получаем:
получаем:
![]() где
где
![]() (13.1)
(13.1)
Величину ![]() называют энтальпией, или тепловой функцией, или теплосодержанием системы. Последние два названия связаны с тем, что в изобарических процессах изменение этой функции равно изменению теплоты:
называют энтальпией, или тепловой функцией, или теплосодержанием системы. Последние два названия связаны с тем, что в изобарических процессах изменение этой функции равно изменению теплоты:
![]() (13.2)
(13.2)
На основании этого можно написать:
![]() (13.3)
(13.3)
В изохорических процессах ![]() . Следовательно:
. Следовательно:
![]() (13.4)
(13.4)
Т. е. при постоянном давлении энтальпия обладает такими же свойствами, что и внутренняя энергия при постоянном объеме.
Если состояние системы, помимо объема, зависит еще от каких-то внешних параметров ![]() то энтальпия и энергия тоже будут от них зависеть, т. к. они являются функциями этого состояния. В этом случае, полный дифференциал энергии запишется как:
то энтальпия и энергия тоже будут от них зависеть, т. к. они являются функциями этого состояния. В этом случае, полный дифференциал энергии запишется как:
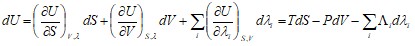 (13.5)
(13.5)
Найдем полный дифференциал энтальпии, опираясь на ее определение (13.1) и равенство (13.5):
![]() (13.6)
(13.6)
В такой интерпретации свободными параметрами, от которых зависит энтальпия, являются: ![]() То есть:
То есть: ![]() Продифференцировав это выражение, получим:
Продифференцировав это выражение, получим:
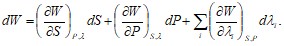
Сравнивая эти два дифференциала, находим:
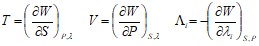 (13.7)
(13.7)
В нашем рассмотрении внутренняя энергия является характеристической функцией свободных (характеристических)параметров:![]() а энтальпия имеет характеристические параметры:
а энтальпия имеет характеристические параметры:![]()
Рассмотрим функцию, имеющую характеристические параметры: ![]() Эта функция называется свободной энергией. Ее изменение показывает работу внешних сил в изотермическом процессе. Отсюда и ее название. Согласно (10.5) и (11.3), при
Эта функция называется свободной энергией. Ее изменение показывает работу внешних сил в изотермическом процессе. Отсюда и ее название. Согласно (10.5) и (11.3), при ![]() имеем:
имеем:
![]() где (13.8)
где (13.8)
![]() (13.9)
(13.9)
и есть свободная энергия. Ее еще называют потенциалом Гельмгольца. Полный дифференциал этой функции равен:
![]() (13.10 а)
(13.10 а)
С другой стороны ![]() Следовательно:
Следовательно:
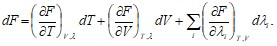 (13.10 б)
(13.10 б)
Отсюда имеем:
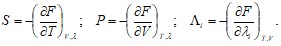 (13.11)
(13.11)
Физический смысл имеют и вторые производные от свободной энергии. Используя (13.11) и (11.5) получим:
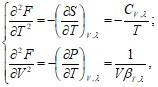 (13.12)
(13.12)
где
![]() (13.13)
(13.13)
Величина ![]() называется изотермической сжимаемостью системы. Смешанные производные можно брать в разной очередности:
называется изотермической сжимаемостью системы. Смешанные производные можно брать в разной очередности:
![]()
![]()
Поскольку переменные ![]() и
и ![]() независимы, то:
независимы, то:

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 |




