![]()
![]() . (60.1)
. (60.1)
Химический потенциал является функцией температуры, давления и концентрации. Поскольку давление одинаково но всему объему, то, учитывая равенство (17.8), градиент разности химических потенциалов равен
![]()
![]() . (60.2)
. (60.2)
Связь изменений химических потенциалов с концентрациями дается так называемым соотношением Гиббса - Дюгема
![]() .
.
Таким образом, производную, входящую во второе слагаемое предыдущего выражения, можно представить как
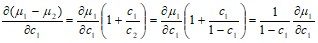 .
.
Выражение (60.2) перепишется в виде
![]() .
.
Подставим это значение градиента в равенство (60.1):
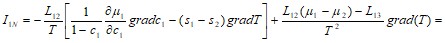
![]() .
.
Далее, используя равенство (59.7), получим
![]()
Множитель, стоящий перед градиентом концентрации, называется коэффициентом диффузии:
![]() , (60.5)
, (60.5)
а перед градиентом температуры - коэффициентом термодиффузии:
![]() . (60.6)
. (60.6)
Окончательно выражение для потока принимает стандартный вид
![]() . (60.7)
. (60.7)
Практические занятия
Целью проведения практических занятий является помощь в освоении теоретического материала и приобретение определенных навыков в решении задач.
При решении задач рекомендуется определенная последовательность.
Необходимо:
- изучить теоретический материал по теме;
- начиная решать задачу, вникнуть в ее смысл. Представить себе не только физическое явление, о котором идет речь, но и те упрощающие предположения, которые надо сделать, проводя решение; - если позволяет характер задачи, обязательно сделать рисунки, поясняющие содержание и решение задачи. Рисунок должен быть достоверным (например, равные по модулю силы изображать векторами-отрезками одинаковой длины и т. д.);
- условие задачи записывать кратко, все, входящие в неё величины, выразить в единицах СИ;
- недостающие в условии данные при необходимости выписать из таблиц;
- решение задачи сопровождать пояснительным текстом;
- решив задачу в общем виде, проверить ответ по равенству размерности отдельных членов формулы;
-выполнить числовые расчеты;
- получив числовой ответ, оценить его правдоподобность.
Тема: Термодинамические параметры. Законы термодинамики.
Цель занятия: определить термодинамические параметры, рассмотреть изменение внутренней энергии, определить совершенную работу и выделенное тепло, кпд цикла Карно. Рассмотреть изменение температуры при адиабатическом обратимом расширении и максимальную работу при абсолютном нуле температуры на основе теоремы Карно.
Примеры решения задач
Задача 1. Киломоль кислорода находится при температуре ![]() и давление
и давление ![]() . Найдите объем газа, считая, что состояние кислорода при данных условиях описывается уравнением Ван-дер-Ваальса. Постоянные
. Найдите объем газа, считая, что состояние кислорода при данных условиях описывается уравнением Ван-дер-Ваальса. Постоянные ![]() и
и ![]() в уравнении Ван-дер-Ваальса для кислорода имеют значения:
в уравнении Ван-дер-Ваальса для кислорода имеют значения:
![]() ,
,
![]() .
.
Решение
Задачу решаем методом последовательных приближений, представляя уравнение Ван-дер-Ваальса в виде
![]() .
.
Пренебрегая значениями ![]() и
и ![]() , в первом приближении получим:
, в первом приближении получим:
![]() .
.
Величину объема во второму приближении найдем, подставляя в первую часть исходного уравнения ![]() , т. е.
, т. е.
![]()
![]() .
.
Подобную операцию будем повторять до тех пор, пока ![]() не совпадает с
не совпадает с ![]() .
.
![]() ,
, ![]() ,
, ![]() .
.
Задача 2. Получите и исследуйте выражение для работы, совершаемой киломолем идеального газа при политропическом процессе расширения, в зависимости от показателя политропы ![]() , если теплоемкость процесса постоянна и равна
, если теплоемкость процесса постоянна и равна ![]() , где
, где ![]() .
.
Решение
По первому началу термодинамики
![]() .
.
Количество тепла, получаемого идеальным газом в процессе политропического расширения, равно:
![]() ,
,
а изменение внутренней энергии
![]() .
.
Поэтому
![]() .
.
Но
![]() ,
,
поэтому
![]() .
.
Из полученного выражения видно, что:
при расширенииЗадача 3. Найдите работу, производимую идеальным газом, и количество тепла, получаемого им при совершении кругового процесса (цикла), состоящего из двух изохорных и двух изобарных процессов. Система последовательно проходит следующие состояния:
1) ![]() 2)
2) ![]() 3)
3) ![]() 4)
4) ![]() 5)
5) ![]()
Решение
Изменение внутренней энергии для кругового процесса равно нулю, так как начальное состояние совпадает с конечным. Поэтому работа ![]() , совершаемая газом, и поглощенное им тепло
, совершаемая газом, и поглощенное им тепло ![]() равны друг другу.
равны друг другу.
При изохорных процессах работа равна нулю, а при изобарных она определяется соответственно для изобары с ![]()
![]()
и для второй изобары
![]() .
.
Таким образом,
![]()
Задачи для самостоятельного решения
Сосуд емкостью![]() .
.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 |




