Пусть система в целом замкнута, т. е. ее энергия и число частиц остаются неизменными. Кроме того, положим, что объем тоже сохраняется. Если состояние системы не равновесное, то энтропия каждой фазы будет меняться, а системы в целом увеличиваться. При достижении равновесия полная энтропия достигнет максимума. Соответственно, ее дифференциал будет равен нулю:
![]() .
.
Величины ![]() и
и ![]() найдем из основного термодинамического равенства (17.1):
найдем из основного термодинамического равенства (17.1):
![]()
Учитывая, что ![]() ;
; ![]() ;
; ![]() , для дифференциала полной энтропии имеем:
, для дифференциала полной энтропии имеем:
![]()
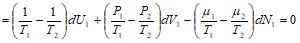 . (43.1)
. (43.1)
Поскольку дифференциалы ![]() независимы, то получим простое условие равновесия:
независимы, то получим простое условие равновесия:
![]() ;
; ![]() ;
; ![]() .
.
Физический смысл этих условий очевиден. Они предопределены тремя способами передачи энергии. Если не совпадают температуры фаз, то энергия передается от одной фазы к другой за счет теплообмена. Если не совпадают давления, то – за счет совершения работы. Наконец, если не совпадают химические потенциалы, то – за счет обмена частицами. Естественно что данный вывод справедлив не только для двухфазных систем, но и для любой системы, состоящей из нескольких подсистем.
Основываясь на полученных выводах, можно найти связь между равновесными значениями параметров. Для простой ![]() - системы, коими являются каждая из фаз, существуют только два независимых параметра. Все остальные параметры могут быть выражены через них. Выразим химический потенциал через интенсивные параметры: температуру и давление. Приравняв химические потенциалы обеих фаз, получим искомую связь:
- системы, коими являются каждая из фаз, существуют только два независимых параметра. Все остальные параметры могут быть выражены через них. Выразим химический потенциал через интенсивные параметры: температуру и давление. Приравняв химические потенциалы обеих фаз, получим искомую связь:
![]() . (43.2)
. (43.2)
Выражение (43.2) определяет неявную зависимость давления от температуры при равновесном состоянии двухфазной системы. Получим дифференциальное уравнение, описывающее эту зависимость. Для этого продифференцируем обе стороны выражения (43.2) и воспользуемся равенством (17.9):
![]() .
.
Отсюда находим полную производную от давления по температуре:
![]() . (44.1)
. (44.1)
На практике удобней пользоваться удельными величинами, приходящимися на один моль вещества: ![]() ,
, ![]() . Здесь
. Здесь ![]() - число Авогадро. Кроме того, удобно выразить разность энтропий через так называемую удельную скрытую теплоту перехода
- число Авогадро. Кроме того, удобно выразить разность энтропий через так называемую удельную скрытую теплоту перехода ![]() , согласно равенству:
, согласно равенству: ![]() . В результате получаем искомое уравнение, которое называется уравнением Клайперона-Клаузиуса:
. В результате получаем искомое уравнение, которое называется уравнением Клайперона-Клаузиуса:
![]() . (44.2)
. (44.2)
Для выяснения физического смысла скрытой теплоты перехода рассмотрим изотермический переход одного моля вещества из одной фазы в другую. При переходе энтропия первой фазы уменьшиться от значения ![]() до нуля, а которой фазы – увеличится от нуля до
до нуля, а которой фазы – увеличится от нуля до ![]() . Суммарная энтропия изменится на
. Суммарная энтропия изменится на ![]() . Согласно равенству (11.3), этому изменению энтропии соответствует количество теплоты, равное:
. Согласно равенству (11.3), этому изменению энтропии соответствует количество теплоты, равное: ![]() . Таким образом, скрытая теплота перехода есть теплота, выделяемая (поглощаемая) при фазовом переходе. Удобство этой величины заключается в том, что она легко измеряется на эксперименте.
. Таким образом, скрытая теплота перехода есть теплота, выделяемая (поглощаемая) при фазовом переходе. Удобство этой величины заключается в том, что она легко измеряется на эксперименте.
Тема: Равновесие трех фаз. Фазовые переходы второго рода.
Для решения уравнения Клайперона-Клаузиуса необходимо знать зависимость скрытой теплоты и объема от температуры и давления. На практике эта зависимость рассчитывается только в простейших случаях. Например, рассмотрим равновесие пара с жидкостью или твердой фазой. Поскольку удельный объем пара намного превосходит удельный объем жидкости (твердой фазы), то последним можно пренебречь. Уравнение (44.2) принимает вид:
![]() .
.
Здесь мы в качестве второй фазы выбрали пар, чтобы величина ![]() была положительной. Аппроксимируем пар идеальным газом. Тогда, согласно уравнению Клайперона-Менделеева, имеем:
была положительной. Аппроксимируем пар идеальным газом. Тогда, согласно уравнению Клайперона-Менделеева, имеем:
![]() ;
; ![]() , или
, или ![]() .
.
В интервале температур, где скрытую теплоту можно считать постоянной, получаем экспоненциальную зависимость давления насыщенного пара от обратной величины температуры:
![]() .
.
В общем случае, даже не решая уравнения (44.2), можно сделать некоторые качественные выводы относительно свойств вещества. Например, при испарении жидкости общий объем системы увеличивается, а ![]() . Следовательно,
. Следовательно, ![]() . Это соответствует хорошо известному факту – с ростом давления растет температура кипения. Аналогичная ситуация имеет место и для твердой фазы. Для большинства веществ температура плавления растет с увеличением давления. Однако существует и обратная ситуация. Например, плотность льда меньше плотности воды, и
. Это соответствует хорошо известному факту – с ростом давления растет температура кипения. Аналогичная ситуация имеет место и для твердой фазы. Для большинства веществ температура плавления растет с увеличением давления. Однако существует и обратная ситуация. Например, плотность льда меньше плотности воды, и ![]() . Поэтому лед можно расплавить, повысив давление.
. Поэтому лед можно расплавить, повысив давление.
Как уже отмечалось, простая ![]() -система имеет два свободных параметра. Поэтому для полифазной
-система имеет два свободных параметра. Поэтому для полифазной ![]() - системы возможно равновесие не только двух, но и трех фаз. Как правило, равновесное состояние трехфазной системы только одно. Оно называется тройной точкой. В этом состоянии температура, давление и химический потенциал должны совпадать для всех трех фаз. Приравнивая выражения, определяющие зависимость химического потенциала от температуры и давления, получим два уравнения, позволяющие найти параметры тройной точки:
- системы возможно равновесие не только двух, но и трех фаз. Как правило, равновесное состояние трехфазной системы только одно. Оно называется тройной точкой. В этом состоянии температура, давление и химический потенциал должны совпадать для всех трех фаз. Приравнивая выражения, определяющие зависимость химического потенциала от температуры и давления, получим два уравнения, позволяющие найти параметры тройной точки:
![]() (45.1)
(45.1)
P
І-крист ІІ-жид.
Pкр
Ртр
ІІІ-газ
Ттр Ткр Т
На ![]() - диаграмме равновесное состояние изображается точкой, в которой сходится три линии, разделяющие пары фаз. В переменных
- диаграмме равновесное состояние изображается точкой, в которой сходится три линии, разделяющие пары фаз. В переменных ![]() тройная точка уже не будет изображаться одной точкой. Ей соответствует отрезок линии, параллельный оси объемов (отрезок ас). Удельные объемы каждой из фаз определяются абсциссами точек
тройная точка уже не будет изображаться одной точкой. Ей соответствует отрезок линии, параллельный оси объемов (отрезок ас). Удельные объемы каждой из фаз определяются абсциссами точек ![]() .
.
![]()
![]()
ЖИД ГАЗ
жидкость-газ
![]()
![]()
Появление критической точки хорошо иллюстрируется ![]() - диаграммой фазового перехода жидкость-газ. При повышении температуры кривые, ограничивающие области однофазных состояний, сближаются, а отрезки прямой, отвечающие фазовым переходам, становятся все короче и короче. Соответственно, сближаются и удельные объемы каждой из фаз, уменьшается разность их энтропий и скрытая теплота перехода. В критической точке кривые сливаются, удельные объемы совпадают, и скрытая теплота перехода равняется нулю. Выше критической точки фазового перехода уже не будет, так как полностью исчезают количественные различия между фазами.
- диаграммой фазового перехода жидкость-газ. При повышении температуры кривые, ограничивающие области однофазных состояний, сближаются, а отрезки прямой, отвечающие фазовым переходам, становятся все короче и короче. Соответственно, сближаются и удельные объемы каждой из фаз, уменьшается разность их энтропий и скрытая теплота перехода. В критической точке кривые сливаются, удельные объемы совпадают, и скрытая теплота перехода равняется нулю. Выше критической точки фазового перехода уже не будет, так как полностью исчезают количественные различия между фазами.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 |




