![]() (13.14)
(13.14)
Данное соотношение содержит только параметры системы и отражает закономерности протекания любого равновесного процесса.
В некоторых случаях по изменению величины свободной энергии можно судить о направлении протекания неравновесных процессов, наподобие того, как это делалось при рассмотрении энтропии. Для этого перепишем основное термодинамическое неравенство (11.6) в виде:
![]() (13.15)
(13.15)
Вели процесс протекает при постоянных значениях ![]() и
и ![]() то имеем:
то имеем:
![]() (13.16)
(13.16)
Следовательно, в таких процессах релаксации свободная энергия будет убывать, и в равновесном состоянии достигнет минимума.
Для полноты картины нам не хватает еще одной функции - функции от характеристических параметров ![]() Эта функция называется потенциалом Гиббса, или просто термодинамическим потенциалом в узком смысле этого термина. Получить его полный дифференциал можно из равенства (13.10), если в нем произвести замену:
Эта функция называется потенциалом Гиббса, или просто термодинамическим потенциалом в узком смысле этого термина. Получить его полный дифференциал можно из равенства (13.10), если в нем произвести замену:![]() В результате получим:
В результате получим:
![]() или
или
![]() где (13.17)
где (13.17)
![]() (13.18)
(13.18)
Как и ранее, найдем полный дифференциал потенциала Гиббса с помощью непосредственного дифференцирования:
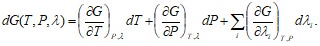
Сравнивая это выражение с (13.17), имеем:
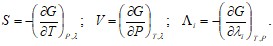 (13.19)
(13.19)
Рассмотрим вторые производные:
![]() (13.20)
(13.20)
Для смешанных производных получаем:
![]() или
или
![]() (13.21)
(13.21)
Потенциал Гиббса также позволяет судить о направлении протекания неравновесных процессов. Если в процессе сохраняются величины ![]() и
и ![]() , то выражение (13.15) можно записать в виде:
, то выражение (13.15) можно записать в виде:
![]() (13.22)
(13.22)
Т. е. потенциал Гиббса убывает в таких процессах, и достигает минимума в равновесном состоянии.
Если сравнить между собой потенциал Гиббса и свободную энергию, то мы видим, что в них параметры ![]() и
и ![]() поменялись ролями. Аналогичная ситуация имеет место по отношению к внутренней энергии и энтальпии.
поменялись ролями. Аналогичная ситуация имеет место по отношению к внутренней энергии и энтальпии.
Термодинамические потенциалы связаны между собой. Знание одних потенциалов позволяет найти значения других. Например, найдем связь между внутренней и свободной энергиями. Из выражений (13.9), (13.11) имеем:
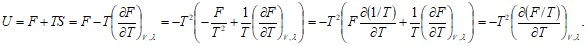 (13.23)
(13.23)
Аналогично связаны между собой энтальпия и потенциал Гиббса.
![]() (13.24)
(13.24)
Эти выражения получили название уравнений Гиббса-Гельмгольца.
Поскольку теплоемкость системы – величина положительная, то при охлаждении ее внутренняя энергия уменьшается. При достижении абсолютного нуля температуры система будет иметь минимальное значение энергии. Т. е. каждая ее часть (и даже каждая ее частица) будет находиться в состоянии с наименьшей энергией. С позиций квантовой физики это означает, что система находится в основном состоянии. Как правило, для реальных систем основное состояние не вырождено. Следовательно, статистический вес равен единице, а энтропия равна нулю. Данный вывод закреплен в так называемой тепловой теореме Нернста:
Энтропия всякого тела при абсолютном нуле равна нулю.
Теорема Нернста является следствием квантовой статистики, где мы имеем дискретный энергетический спектр. Она не может быть доказана в классической статистике с непрерывным энергетическим спектром. Даже в квантовом случае утверждение о не вырожденности основного состояния не является строгим. Поэтому в термодинамике вместо теоремы Нернста используется более «мягкое» утверждение, получившее название третьего начала термодинамики:
Энтропия всех тел при стремлении температуры к абсолютному нулю стремится к некоторому предельному значению, не зависящему от способа охлаждения тела.
Впрочем, данное отличие не является существенным. Так как в термодинамике энтропия определяется с точностью до постоянной, то ничто не мешает нам выбрать ее так, чтобы энтропия обращалась в ноль при ![]() .
.
Третье начало термодинамики не играет столь важную роль, как первые два. Его основное предназначение состоит в том, что оно позволяет получить некоторые особенности поведения систем при низких температурах.
Например, из определения теплоемкости:![]() вытекает:
вытекает:
![]()
Причем здесь не играет роли, какую теплоемкость мы имеем в виду:![]() или
или![]() . Аналогично стремятся к нулю и множество других характеристик. Например, коэффицент теплового расширения. Согласно (13.21):
. Аналогично стремятся к нулю и множество других характеристик. Например, коэффицент теплового расширения. Согласно (13.21):
![]()
Но, при ![]() энтропия является постоянной величиной, не зависящей от давления. Следовательно:
энтропия является постоянной величиной, не зависящей от давления. Следовательно: ![]()
То же самое касается и термического коэффицента изменения давления. На основании (13.14) имеем:
![]()
Так как при абсолютном нуле ![]() , то достаточно бесконечно малого количества теплоты, чтобы повысить температуру системы на конечную величину. Это наталкивает на мысль о невозможности достижения абсолютного нуля температуры. Более детальное рассмотрение процесса охлаждения системы подтверждает это предположение. В самом деле, охладить систему можно двумя способами. Либо используя процесс теплопередачи, либо заставив систему совершать работу. Для первого способа нам необходимо уже иметь систему с нулевой температурой. Если даже предположить, что такая система у нас есть, то первая же бесконечно малая порция теплоты повысит ее температуру до конечного значения. Следовательно, достигнуть абсолютного нуля мы не сможем.
, то достаточно бесконечно малого количества теплоты, чтобы повысить температуру системы на конечную величину. Это наталкивает на мысль о невозможности достижения абсолютного нуля температуры. Более детальное рассмотрение процесса охлаждения системы подтверждает это предположение. В самом деле, охладить систему можно двумя способами. Либо используя процесс теплопередачи, либо заставив систему совершать работу. Для первого способа нам необходимо уже иметь систему с нулевой температурой. Если даже предположить, что такая система у нас есть, то первая же бесконечно малая порция теплоты повысит ее температуру до конечного значения. Следовательно, достигнуть абсолютного нуля мы не сможем.
Иногда третье начало термодинамики формулируют следующим образом:
Невозможно построить вечный двигатель третьего рода.
Под вечным двигателем третьего рода понимается тепловая машина, имеющая КПД равный единице. Согласно выражению КПД=1 при температуре холодильника ![]() , равной нулю. Поскольку абсолютный ноль не достижим, то вечный двигатель третьего рода невозможен.
, равной нулю. Поскольку абсолютный ноль не достижим, то вечный двигатель третьего рода невозможен.
До сих пор мы изучали системы с постоянным числом частиц. Однако в некоторых процессах, таких как химические реакции, процессы диффузии, некоторые фазовые переходы и т. д., число частиц может меняться. Перейдем к рассмотрению подобных процессов.
Естественно, что при изменении числа частиц будет меняться внутренняя энергия системы. В данном случае, наряду с теплообменом и совершением работы, реализуется третий способ изменения энергии. Поскольку энергия – величина аддитивная, то каждая частица данного сорта вносит свой вклад в энергию всей системы. В результате, для случае, когда возможны все три способа обмена энергией, выражение для дифференциала внутренней энергии перепишется в виде:
![]() .
.
Суммирование в последнем слагаемом ведется по всем типам частиц, имеющимся в системе. ![]() характеризует изменение числа частиц сорта
характеризует изменение числа частиц сорта ![]() , а
, а ![]() определяет вклад в энергию одной частицы этого сорта, т. е. представляет собой удельную энергию при
определяет вклад в энергию одной частицы этого сорта, т. е. представляет собой удельную энергию при ![]() . Коэффициент
. Коэффициент ![]() называют химическим потенциалом. Таким образом, у нас появились новые параметры:
называют химическим потенциалом. Таким образом, у нас появились новые параметры: ![]() , которые определяют число частиц данного сорта. В результате изменится выражение для основного термодинамического равенства:
, которые определяют число частиц данного сорта. В результате изменится выражение для основного термодинамического равенства:

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 |




