Изменение энергии и величина совершенной работы равны по модулю и противоположены по знаку:
![]() ,
,
где
![]()
Итак, в системе с постоянным числом частиц внутренняя энергия может меняться либо за счет переданной теплоты, либо за счет совершенной работы. Соотношение между этими тремя величинами можно записать в виде:
![]() .
.
Это математическая запись так называемого первого начала термодинамики. По сути, оно представляет собой закон сохранения энергии для термодинамических процессов. Существует множество различных формулировок этого начала. Одна из них следующая:
Энергия не исчезает и не появляется вновь. Она переходит из одной формы в другую, от одного тела к другому.
Если проинтегрировать равенство, то получим:
![]() , где
, где ![]() ;
; ![]() ;
; ![]() .
.
Величина ![]() определяется только начальным и конечным состоянием системы, поскольку
определяется только начальным и конечным состоянием системы, поскольку ![]() есть полный дифференциал. Если в результате какого-либо процесса система возвращается в исходное состояние (говорят: совершает цикл), то
есть полный дифференциал. Если в результате какого-либо процесса система возвращается в исходное состояние (говорят: совершает цикл), то ![]() . Величины
. Величины ![]() и
и ![]() зависят не только от начального и конечного состояний, но и от пути перехода, т. е. от того, какой именно процесс происходит. Для их вычисления следует знать значения параметров системы в каждом промежуточном состоянии. При совершении цикла
зависят не только от начального и конечного состояний, но и от пути перехода, т. е. от того, какой именно процесс происходит. Для их вычисления следует знать значения параметров системы в каждом промежуточном состоянии. При совершении цикла ![]() и
и ![]() не обязательно будут равны нулю.
не обязательно будут равны нулю.
Используя понятие цикла, можно дать еще одну формулировку первого начала термодинамики:
Невозможно построить вечный двигатель первого рода, т. е., машину, совершающую работу в циклическом процессе, и не заимствующую энергию извне. При ![]() , равном нулю,
, равном нулю, ![]() тоже равно нулю.
тоже равно нулю.
В заключение отметим, что величину ![]() часто удобно представить в виде, аналогичном выражению для элементарной работы:
часто удобно представить в виде, аналогичном выражению для элементарной работы:
![]() ,
,
где С – количество тепла, необходимое для нагревания тела на один градус. Эта величина называется теплоемкостью. Следует заметить, что, в общем случае, теплоемкость не является константной, а зависит от состояния системы. Кроме того, она может зависеть от процесса. Например, для газов различают теплоемкость при постоянном давлении ![]() и при постоянном объеме
и при постоянном объеме ![]() .
.
Совершение работы характеризуется каким-либо меняющимся внешним параметром ![]() . Поэтому в дальнейшем для определения температуры, мы будем пользоваться уточненным выражением:
. Поэтому в дальнейшем для определения температуры, мы будем пользоваться уточненным выражением:
![]() .
.
Как уже говорилось равновесное состояние системы и, следовательно, ее энергия могут быть определены заданием энтропии и внешних параметров: ![]() . Найдем полный дифференциал от этого выражения:
. Найдем полный дифференциал от этого выражения:
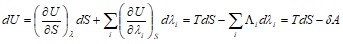 .
.
Это выражение называется основным термодинамическим равенством. Оно справедливо только для равновесных процессов. На основании этого равенства, мы можем определять направление протекания различных процессов, подобно тому, как это делалось для процесса теплопередачи.
Опираясь на основное термодинамическое равенство и первое начало термодинамики, мы можем дать другое определение энтропии. Сравнивая, имеем: ![]() , или
, или
![]() ;
; ![]() .
.
Т. е. мы смогли определить энтропию чисто термодинамическим путем, не используя понятия статистического веса и не опираясь на внутреннюю структуру системы. Именно такое определение энтропии было исходным в термодинамике. Отсюда в частности видно, что в адиабатических процессах энтропия сохраняется, так как ![]() .
.
Отметим, что в термодинамике энтропия определяется с точностью до постоянной ![]() . В дальнейшем мы увидим, из каких соображений выбирается величина этой константы. Этот выбор не имеет принципиального значения, поскольку при изучении различных процессов важно не само значение энтропии, а ее изменение (разность).
. В дальнейшем мы увидим, из каких соображений выбирается величина этой константы. Этот выбор не имеет принципиального значения, поскольку при изучении различных процессов важно не само значение энтропии, а ее изменение (разность).
Ранее уже отмечалось, что ![]() не является полным дифференциалом, а
не является полным дифференциалом, а ![]() не обязательно равен нулю. Однако
не обязательно равен нулю. Однако ![]() уже есть полный дифференциал. Множитель
уже есть полный дифференциал. Множитель ![]() является интегрирующим для
является интегрирующим для ![]() . Для равновесных циклических процессов выражение
. Для равновесных циклических процессов выражение ![]() представляет собой изменение энтропии, а энтропия однозначно определяется состоянием системы. Следовательно
представляет собой изменение энтропии, а энтропия однозначно определяется состоянием системы. Следовательно
![]() .
.
Что же касается неравновесных процессов, то в них энтропия может меняться не только при передаче теплоты, но и за счет своих внутренних причин. Причем, согласно второму началу, это изменение направлено в сторону увеличения. Вследствие этого, основное термодинамическое равенство превращается в неравенство. Перепишем в виде: ![]() . Для неравновесных процессов его следует заменить выражением:
. Для неравновесных процессов его следует заменить выражением:
![]() .
.
То же касается и первого из равенств. Для неравновесных процессов ![]() . А для любых циклических процессов справедливо так называемое неравенство Клаузиуса:
. А для любых циклических процессов справедливо так называемое неравенство Клаузиуса:
![]() .
.
Стимулом развития термодинамики как наука послужила практическая потребность построения различного рода тепловых машин. Т. е. таких машин, которые позволяли бы тепловую энергию тел превращать в полезную работу. Недаром три основных закона термодинамики часто формулируют в виде утверждения о невозможности построения различного рода вечных двигателей.
Как уже говорилось, первое начало термодинамики утверждает невозможность построения вечного двигателя первого рода. Второе начало термодинамики утверждает невозможность построения вечного двигателя второго года. Под вечным двигателем второго рода понимается циклическая тепловая машина, позволяющая получить положительную работу только за счет охлаждения какого-либо тела, без изменения других параметров этого тела или окружающей среды. Такая машина не противоречит первую закону термодинамики, но она противоречит второму закону – закону возрастания энтропии. Действительно, согласно термодинамическому определению энтропии ![]() . При охлаждении тела
. При охлаждении тела ![]() его энтропия будет уменьшаться. Согласно закону возрастания энтропии, это уменьшение должно компенсироваться ее увеличением для окружающей среды. Отсюда же следует, что нельзя получить положительной работы, передавая тепло от тела с меньшей температурой к телу с большей температурой. Энтропия однозначно определяется состоянием тела. И неважно, как тело попало в это состояние: при совершении работы, или же путем теплопередачи. Но в процессе теплопередачи энтропия возрастает и тепло передается от горячего тела к холодному. Обратный процесс приведет к уменьшению суммарной энтропии обеих тел. А это возможно только за счет воздействия третьих тел, чья энтропия будет увеличиваться.
его энтропия будет уменьшаться. Согласно закону возрастания энтропии, это уменьшение должно компенсироваться ее увеличением для окружающей среды. Отсюда же следует, что нельзя получить положительной работы, передавая тепло от тела с меньшей температурой к телу с большей температурой. Энтропия однозначно определяется состоянием тела. И неважно, как тело попало в это состояние: при совершении работы, или же путем теплопередачи. Но в процессе теплопередачи энтропия возрастает и тепло передается от горячего тела к холодному. Обратный процесс приведет к уменьшению суммарной энтропии обеих тел. А это возможно только за счет воздействия третьих тел, чья энтропия будет увеличиваться.
Естественно, что за счет тепловой энергии мы можем получить полезную работу. Но для всякой циклической машины только часть передаваемого тепло можно превратить в работу. Другую часть мы вынуждены передать стороннему телу, чтобы суммарная энтропия не уменьшалось.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 |




