![]() .
.
Отсюда для химического потенциала имеем:
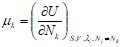
Соответственно, изменится выражение для основного термодинамического неравенства:
![]() .
.
От новых параметров ![]() будут зависеть не только внутренняя энергия системы, но и остальные термодинамические функции: энтропия, энтальпия, свободная энергия, потенциал Гиббса. Дифференциалы этих функций принимают вид:
будут зависеть не только внутренняя энергия системы, но и остальные термодинамические функции: энтропия, энтальпия, свободная энергия, потенциал Гиббса. Дифференциалы этих функций принимают вид:
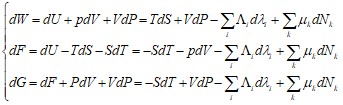
Напомним, что все эти функции – величины аддитивные. Следовательно, они будут являться линейными (добавление каждой частицы данного сорта увеличивает значение функции на одну и ту же величину) и однородными (если число частиц равно нулю, то и значение функции тоже равно нулю) функциями по отношению к параметрам ![]() . В результате, для химического потенциала имеем:
. В результате, для химического потенциала имеем:
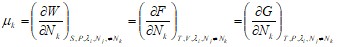
Рассмотрим простейший случай. Пусть простая ![]() - система состоит из частиц одного сорта. Тогда значение термодинамической функции будет равно произведению числа частиц на ее удельное значение:
- система состоит из частиц одного сорта. Тогда значение термодинамической функции будет равно произведению числа частиц на ее удельное значение:
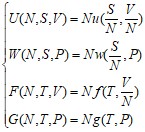
Поскольку термодинамический потенциал Гиббса зависит только от интенсивных параметров, то в результате имеем:
![]() .
.
Т. е. химический потенциал есть ни что иное, как удельный потенциал Гиббса.
Появление новых величин ![]() и
и ![]() позволяет получить новые термодинамические функции. Прежние функции зависели от числа частиц
позволяет получить новые термодинамические функции. Прежние функции зависели от числа частиц ![]() как от параметра, а химический потенциал является производной величиной. Однако можно поступить наоборот – в качестве параметра выбрать
как от параметра, а химический потенциал является производной величиной. Однако можно поступить наоборот – в качестве параметра выбрать ![]() , а
, а ![]() рассматривать как производную величину. Подобную замену мы уже делали в отношении величин
рассматривать как производную величину. Подобную замену мы уже делали в отношении величин ![]() и
и ![]() , или
, или ![]() и
и ![]() . Среди всех таких функций наиболее часто используется так называемый большой термодинамической потенциал Гиббса. Он определяется следующим образом:
. Среди всех таких функций наиболее часто используется так называемый большой термодинамической потенциал Гиббса. Он определяется следующим образом:
![]() .
.
Используя выражения его можно привести к виду:
![]() .
.
Для простоты снова вернемся к случаю ![]() системы, состоящей из одного сорта частиц. На основании равенств и найдем полный дифференциал новой функции:
системы, состоящей из одного сорта частиц. На основании равенств и найдем полный дифференциал новой функции:
![]()
Отсюда имеем:
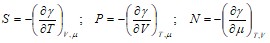 .
.
Тема: Распределение Гиббса.
Квазизамкнутые подсистемы можно в течение некоторого промежутка времени рассматривать как независимые. Тогда к ним применима известная теорема умножения вероятностей: вероятность того, что одна подсистема находится в состоянии ![]() , а другая в состоянии
, а другая в состоянии ![]() , равна произведению вероятностей каждого состояния в отдельности:
, равна произведению вероятностей каждого состояния в отдельности:
![]()
Это утверждение очень просто доказывается с помощью принятого здесь определения вероятности.
![]()
Иначе говоря, функция ![]() , которую называют плотностью вероятности, для двух независимых подсистем равна произведению плотностей вероятности для каждой подсистемы в отдельности. Такая функция именуется мультипликативной.
, которую называют плотностью вероятности, для двух независимых подсистем равна произведению плотностей вероятности для каждой подсистемы в отдельности. Такая функция именуется мультипликативной.
Теперь можно доказать, что ![]() имеет ожидаемую экспоненциальную форму. Логарифм плотности вероятности есть величина аддитивная, т. е.он равен сумме логарифмов этой величины для каждой подсистемы в отдельности:
имеет ожидаемую экспоненциальную форму. Логарифм плотности вероятности есть величина аддитивная, т. е.он равен сумме логарифмов этой величины для каждой подсистемы в отдельности:
![]()
Из теоремы Лиувилля следует, кроме того, что ![]() есть интеграл движения. Этот интеграл движения является, следовательно, аддитивным.
есть интеграл движения. Этот интеграл движения является, следовательно, аддитивным.
Было показано, что имеются следующие аддитивные интегралы движения замкнутой системы: энергия, импульс и момент.
Для того чтобы ![]() был аддитивным интегралом движения, он должен линейно зависеть от энергии, импульса и момента. Если выбрать такую систему отсчета, в которой подсистема как целое не движется и не вращается, то импульс и момент равны нулю и остается только линейная зависимость от энергии:
был аддитивным интегралом движения, он должен линейно зависеть от энергии, импульса и момента. Если выбрать такую систему отсчета, в которой подсистема как целое не движется и не вращается, то импульс и момент равны нулю и остается только линейная зависимость от энергии:
![]()
Коэффициент ![]() должен быть одинаков у всех подсистем большой системы, потому что в противном случае
должен быть одинаков у всех подсистем большой системы, потому что в противном случае ![]() не будет иметь свойств аддитивной функции. Если
не будет иметь свойств аддитивной функции. Если ![]() одинаково у двух подсистем, то для этих подсистем получается:
одинаково у двух подсистем, то для этих подсистем получается:
![]()
Отсюда и видна аддитивность ![]() .
.
Вероятность бесконечно большой энергии должна быть бесконечно мала; поэтому ![]() Введем обозначение
Введем обозначение
![]()
Если подсистемы находятся между собой в равновесии, то смысл величины ![]() такой же, как в предыдущих параграфах (произведение температуры на постоянную Больцмана). Действительно, для идеального газа в качестве отдельной подсистемы можно взять и одну молекулу, и тогда распределение Гиббса
такой же, как в предыдущих параграфах (произведение температуры на постоянную Больцмана). Действительно, для идеального газа в качестве отдельной подсистемы можно взять и одну молекулу, и тогда распределение Гиббса
![]()
![]()
![]()
переходит в распределение Больцмана
![]()
отвечающее равновесным условиям в газе. Введем еще обозначение
![]()
Тогда искомая функция распределения выглядит окончательно так
![]()
На функцию распределения ![]() накладывается условие
накладывается условие
![]()
так как ![]() Это означает просто, что вероятность нахождения подсистемы в каком - либо из всех возможных состояний, совместимых с законами сохранения, равна единице. С помощью условия нормировки величина
Это означает просто, что вероятность нахождения подсистемы в каком - либо из всех возможных состояний, совместимых с законами сохранения, равна единице. С помощью условия нормировки величина ![]() выражается в зависимости от
выражается в зависимости от ![]() (и, как будет показано в следующем параграфе, от некоторых параметров, входящих в энергию Е). Для этого достаточно подставить распределение Гиббса (7.10) в (7.11) и просуммировать по всем возможным состояниям. Тогда множитель
(и, как будет показано в следующем параграфе, от некоторых параметров, входящих в энергию Е). Для этого достаточно подставить распределение Гиббса (7.10) в (7.11) и просуммировать по всем возможным состояниям. Тогда множитель ![]() как постоянная величина выносится за знак суммы и получается следующее равенство для нахождения
как постоянная величина выносится за знак суммы и получается следующее равенство для нахождения ![]() :
:
![]() . (7.12)
. (7.12)

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 |




