3. Основні лінії діаграми:
Ø лінія ліквідус acb, складається із двох галузей, що сходяться в одній крапці;
Ø лінія солідус аdcfb, складається із трьох ділянок;
Ø dm - лінія граничної концентрації компонента В у компоненту А;
Ø fn - лінія граничної концентрації компонента А в компоненту В.
4. Типові сплави системи.
При концентрації компонентів, не перевищуючих граничних значень (на ділянках Аm і nв), сплави кристалізуються аналогічно сплавам твердим розчинам з необмеженою розчинністю, див криву охолодження сплаву I на мал. 5.5 б. При концентрації компонентів, що перевищує граничні значення (на ділянці dcf), сплави кристалізуються аналогічно сплавам механічним сумішам, див. криву охолодження сплаву II на мал.
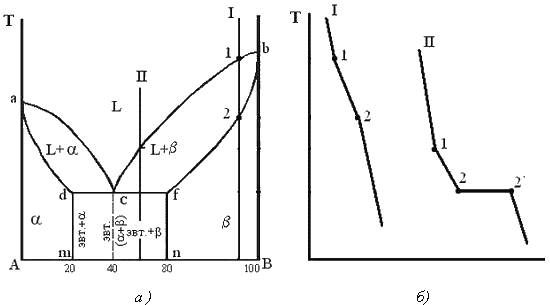
Діаграма стану сплавів з обмеженою розчинністю компонентів у твердому стані (а) і криві охолодження типових сплавів (б)
Сплав з концентрацією компонентів, що відповідає крапці з, є евтектичним сплавом. Сплав складається з дрібнодисперсних кристалів твердих розчинів і, эвт. (кр. тв. р-ра + кр. тв. р-ра)
Кристали компонентів у чистому виді в жодному зі сплавів не присутні.
Діаграма стану сплавів, компоненти яких утворять хімічні сполуки.
Діаграма стану сплавів представлена на мал.
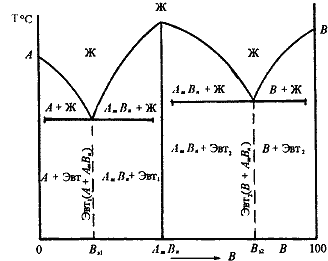
Діаграма стану сплавів, компоненти яких утворять хімічні сполуки
Діаграма стану складна, складається з декількох простих діаграм. Число компонентів і кількість діаграм залежить від того, скільки хімічних сполук утворять основні компоненти системи.
Число фаз і вид простих діаграм визначаються характером взаємодії між компонентами.
Эвт1 (кр. А + кр. AmBn);
Эвт2 (кр. B + кр. AmBn).
Діаграма стану сплавів, що випробовують фазові перетворення у твердому стані (змінна розчинність)
Діаграма стану представлена на мал.
По зовнішньому вигляді діаграма схожа на діаграму стану сплавів з обмеженою розчинністю компонентів у твердому стані. Відмінність у тім, що лінії граничної розчинності компонентів не перпендикулярні осі концентрації. З'являються області, у яких з однорідних твердих розчинів при зниженні температури виділяються вторинні фази.
На діаграмі:
§ df - лінія змінної граничної розчинності компонента В у компоненту А;
§ ek - лінія змінної граничної розчинності компонента А в компоненту В.
Крива охолодження сплаву I представлена на мал.
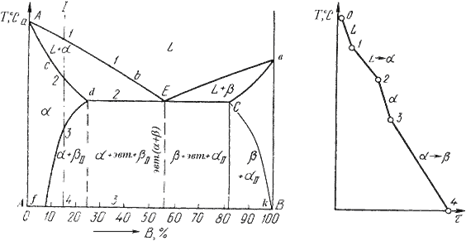
Діаграма стану сплавів, що випробовують фазові перетворення у твердому стані (а) і крива охолодження сплаву (б)
Процес кристалізації сплаву I: до крапки 1 прохолоджується сплав у рідкому стані. При температурі, що відповідає крапці 1, починають утворюватися центри кристалізації твердого розчину. На ділянці 1-2 іде процес кристалізації, що протікає при температурі, що знижується. При досягненні температури відповідній крапці 2, сплав твердіє, при подальшому зниженні температури прохолоджується сплав у твердому стані, що складається з однорідних кристалів твердого розчину. При досягненні температури, що відповідає крапці 3, твердий розчин виявляється насиченим компонентом В, при більше низьких температурах розчинність другого компонента зменшується, тому з розчину починає виділятися надлишковий компонент у вигляді кристалів. За крапкою 3 сплав складається із двох фаз: кристалів твердого розчину і вторинних кристалів твердого розчину.
Зв'язок між властивостями сплавів і типом діаграми стану
Тому що вид діаграми, також як і властивості сплаву, залежить від того, які сполуки або які фази утворили компоненти сплаву, то між ними повинна існувати певний зв'язок. Ця залежність установлена Курнаковим, (див. мал.).
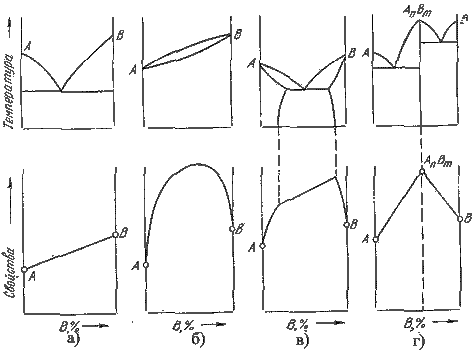
Зв'язок між властивостями сплавів і типом діаграми стану
1. При утворенні механічних сумішей властивості змінюються за лінійним законом. Значення характеристик властивостей сплаву перебувають в інтервалі між характеристиками чистих компонентів.
2. При утворенні твердих розчинів з необмеженою розчинністю властивості сплавів змінюються по криволінійній залежності, причому деякі властивості, наприклад, електроопір, можуть значно відрізнятися від властивостей компонентів.
3. При утворенні твердих розчинів з обмеженою розчинністю властивості в інтервалі концентрацій, що відповідають однофазним твердим розчинам, змінюються за криволінійним законом, а у двофазній області - за лінійним законом. Причому крайні крапки на прямій є властивостями чистих фаз, гранично насичених твердих розчинів, що утворять дану суміш.
4. При утворенні хімічних сполук концентрація хімічної сполуки відповідає максимуму на кривій. Ця крапка перелому, що відповідає хімічній сполуці, називається сингулярною крапкою.
Лекція
Навантаження, напруги й деформації. Механічні властивості.
Фізична природа деформації металів.
Деформацією називається зміна форми й розмірів тіла під дією напруг.
Напруга – сила, що діє на одиницю площі перетину деталі.
Напруги й викликувані ними деформації можуть виникати при дії на тіло зовнішніх сил розтягання, стиску й т. д., а також у результаті фазових (структурних) перетворень, усадки й інших фізико-хімічних процесів, що протікають у металах, і пов'язаних зі зміною об'єму.
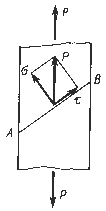 Метал, що перебуває в напруженому стані, при будь-якому виді навантаження завжди випробовує напруги нормальні й дотичні
Метал, що перебуває в напруженому стані, при будь-якому виді навантаження завжди випробовує напруги нормальні й дотичні
Схема виникнення нормальних і дотичних напружень у металі при його навантаженні
Ріст нормальних і дотичних напружень приводить до різних наслідків. Ріст нормальних напруг приводить до тендітного руйнування. Пластичну деформацію викликають дотичні напруження.
Деформація металу під дією напруг може бути пружної й пластичної.
Пружної називається деформація, що повністю зникає після зняття зухвалих її напруг.
При пружному деформуванні змінюються відстані між атомами металу в кристалічній решітці. Зняття навантаження усуває причину, що викликала зміну міжатомної відстані, атоми стають на колишні місця, і деформація зникає. Пружна деформація на діаграмі деформації характеризується лінією ОА
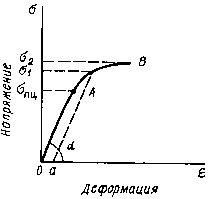
Діаграма залежності деформації металу від діючих напруг
Якщо нормальні напруги досягають значення сил міжатомних зв'язків, то спостерігається тендітне руйнування шляхом відриву (мал.6.3.)

Схема пружної деформації й тендітного руйнування під дією пружних напружень а – ненапружена решітка металу; б – пружна деформація; в, г – тендітне руйнування в результаті відриву
Залежність між пружною деформацією і напругою виражається законом Гука
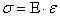
де: Е - модуль пружності.
Модуль пружності є найважливішою характеристикою пружних властивостей металу. По фізичній природі величина модуля пружності розглядається як міра міцності зв'язків між атомами у твердому тілі.
Ця механічна характеристика структурно нечутлива, тобто термічна обробка або інші способи зміни структури не змінюють модуля пружності, а підвищення температури, що змінює міжатомні відстані, знижує модуль пружності.
Пластичними або залишковими називається деформація після припинення дії її напруг, що викликали.
При пластичному деформуванні одна частина кристала переміщається стосовно іншої під дією дотичних напружень. При знятті навантажень зрушення залишається, тобто відбувається пластична деформація У результаті розвитку пластичної деформації може відбутися грузле руйнування шляхом зрушення.
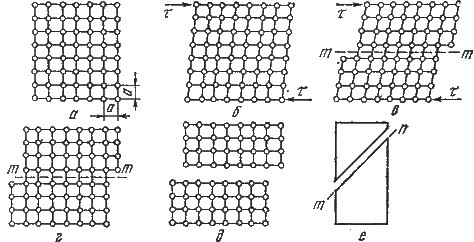
Схема пластичної деформації й грузлого руйнування під дією дотичних напружень а – ненапружена решітка; б – пружна деформація; в – пружна й пластична деформація; г – пластична деформація; д, е – пластичне (грузле) руйнування в результаті зрізу
Природа пластичної деформації.
Метали й сплави у твердому стані мають кристалічна будова, і характер їхньої деформації залежить від типу кристалічної структури й від наявності недосконалостей у цій структурі.
Розглянемо пластичну деформацію в монокристалі.
Пластична деформація може протікати під дією дотичних напружень і може здійснюватися двома способами.
1. Трансляційне ковзання по площинах. Одні шари атомів кристала сковзають по інших шарах, причому вони переміщаються на дискретну величину, рівну цілому числу міжатомних відстаней.
У проміжках між смугами ковзання деформація не відбувається. Тверде тіло не змінює своєї кристалічної будови під час пластичної деформації й розташування атомів в елементарних осередках зберігається
Площинами ковзання є кристалографічні площини з найбільш щільним упакуванням атомів.
Це найбільш характерний вид деформації при обробці тиском.
2. Двійникування - поворот однієї частини кристала в положення симетричне іншої його частини. Площиною симетрії є площина двійникування.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51 52 53 54 55 56 57 58 59 60 61 62 63 |


