3. Сравните основные свойства следующих аминов: изобутиламин; бутанамин-1; 2-метилбутанамин-2; 2-метилпропанамин-1; этандиамин-1,2; 2-метилпропандиамин-1,2; диметиламин; метилэтил-амин; диэтиламин; диметилэтиламин; трипропиламин.
Занятие 5. химические свойства функциональных производных алканов: реакции нуклеофильного замещения
Вопросы для подготовки к занятию
Механизмы реакций SN1 и SN2 на примерах свойств галогеналканов, спиртов, простых эфиров, аминов. Сравнение механизмов. Факторы, влияющие на направление и скорость нуклеофильного замещения. Стереохимия нуклеофильного замещения. Способы установления механизма реакции.
Содержание занятия
1. Обсуждение вопросов по теме занятия.
2. Контроль усвоения темы.
3. Лабораторная работа.
Типовые обучающие вопросы и эталоны ответов на них
Вопрос 1. Какие факторы способствуют протеканию реакции по SN1-механизму, а какие — по SN2:
доступность реакционного центра субстрата, возможность образования стабильного карбокатиона, высокая нуклеофильность реагента, стабильность нуклеофуга, применение протонного растворителя и кислотных катализаторов,применение апротонного растворителя?
Ответ. 1) Доступность реакционного центра субстрата способствует протеканию реакции в том случае, когда взаимодействие этого соединения с нуклеофилом является скоростьопределяющей стадией. Это имеет место при SN2-процессе. SN2-механизм — одностадийный, и на этой единственной стадии происходит взаимодействие субстрата с нуклеофилом, что приводит к образованию и дальнейшему распаду переходного состояния.
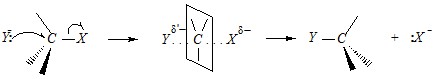
Поэтому чем доступнее реакционный центр (т. е. меньше размеры окружающих его заместителей), тем этот фактор в большей степени способствует протеканию реакции по SN2-механизму и тем выше скорость реакции. Напротив, скорость реакции, протекающей по механизму SN1, зависит только от скорости наиболее медленной первой стадии, в которой нуклеофил участия не принимает.
1) ![]()
2) ![]()
Взаимодействие с нуклеофилом протекает быстро, на второй стадии. Поэтому доступность реакционного центра субстрата на скорость SN1-реакций в целом не влияет.
2) Возможность образования стабильного карбокатиона способствует протеканию реакции в том случае, когда этот карбокатион образуется на лимитирующей (скоростьопределяющей) стадии. Это наблюдается, если реакция протекает по механизму SN1. Чем стабильнее образуется карбокатион, тем легче осуществляется реакция по этому механизму, а значит, образование стабильного карбокатиона способствует протеканию SN1-реакции. В SN2-механизме карбокатион не образуется, поэтому данный фактор не может способствовать протеканию реакции по этому механизму.
3) Высокая нуклеофильность реагента имеет значение в том случае, когда атакующая частица принимает участие в лимитирующей стадии процесса. В реакциях, протекающих по механизму SN1, лимитирующая стадия представляет собой диссоциацию субстрата, в которой нуклеофил участия не принимает. Поэтому высокая активность нуклеофила не может способствовать протеканию реакции по этому механизму. Однако для реакций, протекающих по механизму SN2, нуклеофильная активность реагента может играть решающую роль, так как нуклеофил участвует в лимитирующей стадии процесса.
4) Высокая стабильность аниона уходящей группы (нуклеофуга) должна способствовать протеканию реакции по механизму SN1, так как в лимитирующей стадии SN1-процесса образуются карбокатион и анион уходящей группы. То есть чем стабильнее нуклеофуг, тем легче будет протекать реакция по SN1-механизму. На скорость SN2-реакций природа уходящей группы часто не оказывает существенного влияния. Более важна бывает в этих реакциях нуклеофильная атака.
5) Применение протонного растворителя способствует диссоциации субстрата по SN1-механизму, так как образующийся при этом анион уходящей группы может связываться таким растворителем за счёт образования водородных связей. Аналогичную роль играют и кислотные катализаторы. Но в этом случае возможно и связывание анионов нуклеофуга в нейтральные молекулы, особенно если это анионы слабых кислот. И в том и в другом случае равновесие диссоциации субстрата смещается вправо, и скорость SN1-реакции увеличивается. Однако применение протонного растворителя и кислотных катализаторов для реакций, протекающих по механизму SN2, может уменьшать активность нуклеофильной частицы за счёт частичного или полного её связывания. Поэтому применение протонного растворителя и кислотных катализаторов не будет способствовать протеканию SN2-реакций. Апротонные полярные растворители могут по-разному влиять на скорость SN2-реакций, так как от их применения зависит способность к сольватации исходного субстрата, нуклеофила, переходного состояния и продуктов реакции. Другими словами, апротонные полярные растворители могут способствовать или не способствовать протеканию реакции по SN2-механизму, это зависит от вида переходного состояния. Для SN1-реакций при применении апротонных растворителей более важным оказывается их полярность. Высокополярные растворители способствуют диссоциации, а значит, протеканию реакций по SN1-механизму.
Таким образом, протеканию реакции по SN1-механизму способствуют возможность образования стабильного карбокатиона, стабильность нуклеофуга, применение протонных растворителей и кислотных катализаторов, а также возможно применение апротонных высокополярных растворителей. Протеканию реакции по SN2-механизму способствуют доступность реакционного центра субстрата, высокая нуклеофильность реагента и, как вариант, применение апротонных высокополярных растворителей.
Вопрос 2. Приведите наиболее вероятные механизмы реакций взаимодействия каждого из соединений: изобутилхлорида и трет-бутилхлорида с водным раствором бромоводородной кислоты.
Ответ. В водном растворе бромоводородная кислота находится в диссоциированном виде, поэтому роль нуклеофилов будут играть образующиеся при этой диссоциации бромид-ионы Br-. При взаимодействии изобутилхлорида с бромид-ионом реакция, вероятнее всего, будет протекать по SN2-механизму, так как реакционный центр субстрата доступен для нуклеофильной атаки, но, напротив, молекула исходного изобутилхлорида не способна к диссоциации (это означает, что SN1-механизм невозможен).
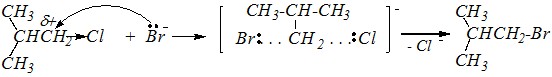
Для взаимодействия трет-бутилхлорида, наоборот, более вероятен SN1-механизм, так как реакционный центр субстрата доступен для нуклеофильной атаки по третичному атому углерода, но молекула субстрата может диссоциировать в протонном высокополярном растворителе (вода) с образованием устойчивого третичного карбокатиона.
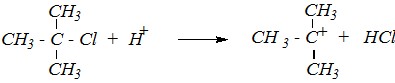
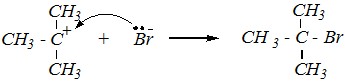
Вопрос 3. Получите по реакции Вильямсона 1-метокси-2,2-диме-тилпропан двумя способами. Какая из этих реакций протекает легче?
Ответ. По реакции Вильямсона простые эфиры получают взаимодействием галогеналканов с алкоголятами щелочных металлов:
R-X + R’-O-Na+ > R-O-R’ + NaX .
Для получения 1-метокси-2,2-диметилпропана
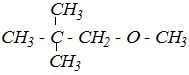
могут быть использованы: а) либо неопентилгалогенид и метилат натрия
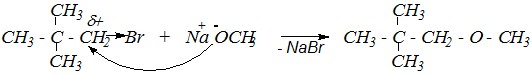 ,
,
б) либо метилгалогенид и 2,2-диметилпропанолят натрия
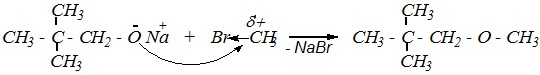 .
.
Это реакции нуклеофильного замещения, в которых разные субстраты (галогеналканы) и разные нуклеофильные частицы (алкоголят-ионы). Легкость протекания реакции зависит от реакционной способности реагентов. Алкоголят-ионы мало отличаются по своей активности (только в основном за счёт различия в подвижности частиц разного размера), так как имеют целочисленный отрицательный заряд. Активность электронейтральных молекул субстрата (неопентилгалогенида и метилгалогенида) различается более существенно. К реакции по SN1-механизму они не способны, потому как при их диссоциации образуются неустойчивые первичные карбокатионы. Значит, наиболее вероятный механизм — SN2. В этом случае метилгалогенид более активен, так как и атом углерода значительно более доступен для нуклеофильной атаки, и эффективный положительный заряд на нём (?'>?) выше, чем на соответствующем атоме углерода неопентилгалогенида. Поэтому реакция (б) — взаимодействие метилгалогенида с 2,2-диметил-пропанолятом натрия будет протекать легче.
Контрольные вопросы и задачи
Приведите SN2-механизм реакции н-бутилового спирта с хлороводородом. Приведите SN1-механизм реакции трет-амилхлорида со щёлочью. Приведите наиболее вероятные механизмы реакций взаимодействия каждого из соединений: неопентилбромида, трет-амилбромида, изоамилбромида, 3-метил-3-бромпентана с водным раствором КОН. Для н-пропилового спирта приведите механизм реакции образования в присутствии концентрированной серной кислоты простого эфира (симметричного). Получите по реакции Вильямсона 2-метоксибутан разными способами, сравните легкость протекания этих реакций и выберите оптимальный.
Лабораторная работа
Оформление этой и всех последующих лабораторных работ следует делать по шаблону, представленному на странице 170.
Получение этилхлорида из этилового спирта
В пробирку насыпьте 2 лопаточки хлорида натрия. Прилейте 5–6 капель этилового спирта (на общем столе). Затем добавьте 3–4 капли концентрированной серной кислоты (в вытяжном шкафу) и нагревайте в пламени спиртовки, не допуская слишком обильного выделения хлороводорода. Время от времени подносите отверстие пробирки к пламени спиртовки. Выделяющийся этилхлорид загорается, образуя колечко зеленого цвета (образование этилхлорида начинается не сразу).
Приведите схему и механизм реакции получения этилхлорида.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 |



