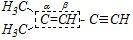
Аналогично предыдущему соединению перечисляются заместители и добавляется слово «этилен». Название по рациональной номенклатуре: ?, ?-диметил-?-ацетиленилэтилен.
Вопрос 2. Приведите механизм реакции взаимодействия бутена-1 и
2-метилбутена-1 с водой в присутствии кислотного катализатора. Какое из этих соединений легче будет вступать в реакцию? В чем различие взаимодействия бутена-1 с концентрированной HCl и с очень разбавленной HCl?
Ответ. Первое, что необходимо сделать, – это убедиться, что данные соединения действительно взаимодействуют с водой по АЕ-механизму. Присутствие кислотного катализатора означает, что в среде содержатся катионы водорода Н+, способные выполнять функцию электрофилов. Бутен-1 и 2-метилбутен-1 — это алкены, а значит, неполярные ?-электронные системы, в которых ?-электрон-ное облако, как правило, доступно для электрофильной атаки. Поэтому механизм взаимодействия можно представить так:
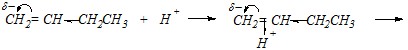
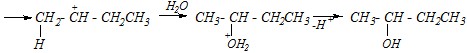
Образующийся на промежуточной стадии втор-бутил-катион
СН3-+СН-СН2СН3 устойчивее альтернативного первичного бутил-катиона +СН2-СН2-СН2СН3 по причине большей делокализации положительного заряда с участием соседних алкильных групп (индуктивный и мезомерный эффекты):
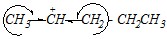
Потому продуктом присоединения будет вторичный спирт.
Аналогичный механизм гидратации можно представить и для
2-метилбутена-1
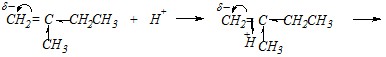
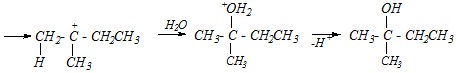
В этом примере будет более полная делокализация положительного заряда в карбокатионе, образующемся на промежуточной стадии (трет-амил-катион). Поэтому карбокатион образуется легче, и гидратация такого алкена протекает быстрее.
При взаимодействии бутена-1 с концентрированной соляной кислотой продукт реакции будет иным, чем при взаимодействии с разбавленной кислотой, так как образующиеся на первой стадии карбокатионы будут преимущественно взаимодействовать не с молекулами воды, а с более активными хлорид-ионами, концентрация которых в данном растворе кислоты будет большой.
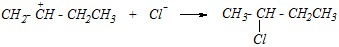
Вопрос 3. Приведите механизм реакции взаимодействия пропена с бромноватистой кислотой (в присутствии каталитических количеств бромоводородной кислоты) и механизм реакции озонолиза этого углеводорода.
Ответ. Бромноватистая кислота в присутствии более сильной, бромоводородной, подвергается протонированию и диссоциирует с образованием бромоний-катиона
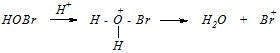 ,
,
который и будет играть роль электрофила в этой реакции.
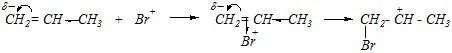
Образовавшийся карбокатион должен далее взаимодействовать с нуклеофильной частицей (анионом или нейтральной молекулой). Так как по условию используются каталитические количества бромоводородной кислоты, то концентрация бромид-ионов невелика. Поэтому карбокатион может взаимодействовать только с молекулами растворителя (воды), находящимися в большом избытке:
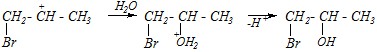
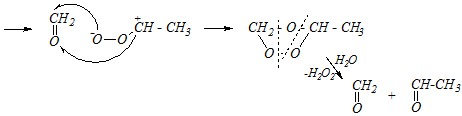
Реакцию озонолиза тоже можно отнести к реакциям электрофильного присоединения, в которых роль электрофила играет молекула озона за счёт одного из концевых атомов кислорода. При присоединении озона к алкену образуется соответствующий озонид, который после перегруппировки и последующего гидролиза распадается на карбонильные соединения.
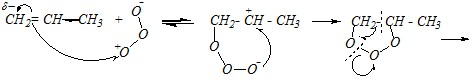
Вопрос 4. Приведите механизм реакции взаимодействия 3-метилбуте-на-1 с бромоводородом в тетрахлорметане в присутствии пероксида водорода.
Ответ. Так как реакция по условиям должна протекать в присутствии пероксида водорода, то, скорее всего, механизм такого превращения не электрофильный, а радикальный. И действительно, тетрахлорметан — неполярный растворитель, поэтому бромоводород диссоциировать в этих условиях не будет, катионов водорода в среде не образуется. Так как электрофильных частиц нет, то и реакция по электрофильному механизму не пойдёт. Но пероксиды являются источниками свободных радикалов, а при взаимодействии их с бромоводородом образуются атомы брома, также являющиеся свободными радикалами:
Н2О2 > 2НО?
НО? + HBr > Н2О + ?Br
Именно эти частицы и атакуют далее молекулы алкена:
![]()
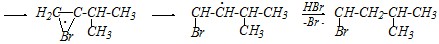
При этом при разрыве ?-связи атом брома присоединяется в данном случае к концевому углеродному атому и, таким образом, образуется в качестве промежуточной частицы более устойчивый углеводородный радикал, который затем превращается в молекулу конечного продукта за счёт отрыва водорода от молекулы бромоводорода.
Вопрос 5. Приведите пример реакции радикального замещения для
5-метилгексена-1. Каковы условия и направление протекания таких реакций?
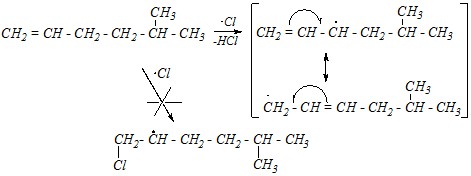
Ответ. Реакции замещения характерны для алканов, а для алкенов более предпочтительными являются реакции присоединения (электрофильного или радикального) по причине более лёгкого разрыва ?-связей. Однако при повышенных температурах (до 400–500°С) реакции радикального замещения начинают конкурировать с реакциями присоединения, в этих условиях энергии молекулы становится достаточно для разрыва как ?-связи, так и ?-связи. При этом при отрыве атома водорода от ?-углеродного атома (по отношению к двойной связи) образуется радикал, стабилизированный р-?-сопряжением, и реакция протекает по пути замещения. В случае реакции присоединения такого стабильного радикала не образуется. Для 5-метилгексена-1 по такому пути будет протекать взаимодействие с газообразным хлором при 500°С:
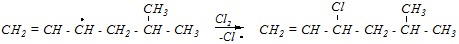
Контрольные вопросы и задачи
Приведите механизм реакции взаимодействия каждого из соединений: а) 2-метилбутена-2, б) 2-метилбутена-1, в) 4-метил-пентена-2, г) пентена-1, д) 2,4-диметилпентена-2, е) 2,4-диметил-гексена-1, ж) 2-метилпропена, з) 4-метилпентена-1 — со следующими реагентами: 1) с водой в присутствии кислотного катализатора, 2) с водным раствором бромоводородной кислоты в отсутствие пероксидов, 3) с бромоводородом в апротонном растворителе в присутствии пероксидов, 4) с бромной водой,
5) с этанолом в присутствии кислотного катализатора. Какое из этих соединений легче будет вступать в реакцию? Приведите механизм озонолиза для 2-метилбутена-2 и для
пентена-2. Приведите механизм AE - и SR-реакций взаимодействия с хлором для каждого из следующих алкенов: а) 2,4-диметилгексена-1; б) 4-ме-тилпентена-1; в) 2,2,5,5-тетраметилгексена-3. Укажите условия.
Занятие 9. диены, полиены, алкины:
особенности строения и свойств
Вопросы для подготовки к занятию
Строение, изомерия и особенности свойств алленов. Особенности строения сопряжённых диенов. Реакции диенового синтеза. Особенности полимеризации сопряжённых диенов. Особенности строения алкинов. Кислотные свойства алкинов. Возможность протекания реакций нуклеофильного присоединения и электрофильного замещения.
Содержание занятия
1. Обсуждение вопросов по теме занятия.
2. Контроль усвоения темы.
Типовые обучающие вопросы и эталоны ответов на них
Вопрос 1. Какие соединения образуются при присоединении хлороводорода (1 и 2 моль) к бутадиену-1,2 (1 моль) в отсутствие пероксидов? Приведите механизм реакции.
Ответ. Бутадиен-1,2 относится к диеновым углеводородам с кумулированными двойными связями. Присоединение хлороводорода в отсутствие пероксидов — это реакция электрофильного присоединения, в которой электрофилом является полярная молекула хлороводорода. Так же, как и в случае алкенов, первоначально образующийся ?-комплекс превращается в ?-комплекс, являющийся карбокатионом. При этом концевая двойная связь оказывается более полярной, и, соответственно, присоединение протона от молекулы хлороводорода происходит к концевому углеродному атому:
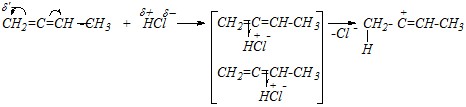
Присоединение первой молекулы хлороводорода завершается взаимодействием образовавшегося карбокатиона с хлорид-ионом:
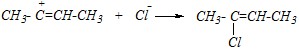
При определении направления присоединения второй молекулы HCl к образовавшемуся продукту необходимо учесть влияние атома хлора на распределение электронной плотности на двойной связи (р-?-сопряжение), и поэтому протон от молекулы хлороводорода присоединяется к атому углерода с б?льшим отрицательным зарядом.
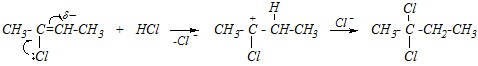
Вопрос 2. Какое соединение преимущественно образуется при взаимодействии 4-метилпентадиена-1,3 с очень разбавленной HCl?
Ответ. В разбавленной соляной кислоте присутствуют катионы Н+, и поэтому данная реакция — это электрофильное присоединение, где электрофилом является протон. В 4-метилпентадиене-1,3 двойные связи сопряжены (?-?-сопряжение), и из-за влияния двух метильных групп электронная плотность будет локализоваться на противоположном конце молекулы диена:
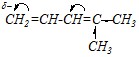

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 |



