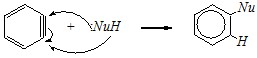 .
.
Однако если в ароматическом кольце помимо атома хлора присутствует другая электроноакцепторная группировка, способствующая замещению атома хлора, то становится возможной нуклеофильная атака по углероду, связанному с хлором. Такой акцептор должен находиться в орто - или пара-положении к атому хлора. Это механизм ароматического бимолекулярного замещения (SN2аром):
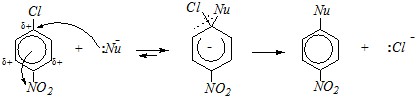
Вопрос 4. Какое из соединений будет легче вступать в реакцию нуклеофильного замещения: 1-фенил-1-хлорпропан или 1-фенил-2-хлорпропан? Приведите механизмы кислотного гидролиза каждого из этих соединений.
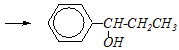
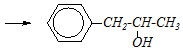
Ответ. В молекулах 1-фенил-1-хлорпропана или 1-фенил-2-хлорпропана атом хлора находится в боковой цепи, но в первом соединении — у ?-атома, а во втором — у ?-атома углерода:
 .
.
И в том, и в другом случае атом хлора способен подвергаться нуклеофильному замещению, подобно тому, что наблюдается в алифатических соединениях. В этих молекулах атом хлора связан с вторичным углеродным атомом углеродной цепи. Такие реакционные центры мало доступны для нуклеофильной атаки по бимолекулярному механизму (SN2). А для осуществления замещения по мономолекулярному механизму необходима диссоциация субстрата и образование устойчивого карбокатиона. В случае ?-хлорпроиз-водного такое замещение возможно и даже довольно легко осуществимо, так как вследствие диссоциации этого соединения образуется карбокатион, стабилизированный за счёт р-?-сопряжения:
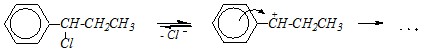
Кислая среда способствует связыванию отщепляющегося аниона и ещё в большей степени будет ускорять процесс замещения, втом числе и реакцию гидролиза:
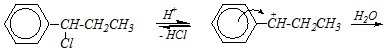
Для 1-фенил-2-хлорпропана примерно одинаково трудно осуществляются и SN1, и SN2-реакции. Однако кислая среда способствует протеканию реакции по SN1-механизму, поэтому наиболее вероятным здесь будет мономолекулярное замещение:
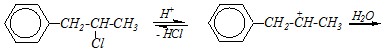
Стабильность карбокатиона здесь примерно такая же, как и у обычного вторичного алифатического, поэтому ?-хлорпроизводное будет легче вступать в реакцию нуклеофильного замещения.
Контрольные вопросы и задачи
Проведите сульфирование: а) этилбензола, б) бензойной кислоты. Рассмотрите механизм реакции сульфирования на примере этилбензола. Объясните, почему группа - СООН является
м-ориентантом и обладает дезактивирующим действием. Сравните строение и реакционную способность галогенозамещённых углеводородов ароматического и алифатического рядов. Найдите сходство и объясните различие в поведении хлорбензола, этилхлорида и винилхлорида. Разберите механизмы реакций нуклеофильного замещения в ароматическом кольце на примере ароматических галогенопроизводных.
Занятие 27. ароматические сульфокислоты и их производные.
ароматические нитросоединения
Вопросы для подготовки к занятию
Номенклатура сульфокислот и их производных. Строение сульфогруппы. Кислотные свойства аренсульфокислот: сравнение с кислотными свойствами органических и неорганических кислот; влияние заместителей в ароматическом кольце на кислотные свойства сульфокислот. Электрофильное замещение в ароматическом кольце сульфокислот: замещение атома водорода и замещение сульфогруппы. Нуклеофильное замещение сульфогруппы в ароматическом кольце. Нуклеофильное замещение в сульфогруппе: условия и возможность протекания реакции в сравнении с карбоновыми кислотами. Реакции восстановления аренсульфокислот и их производных. Производные аренсульфокислот: особенности строения и химического поведения хлорангидридов, амидов и эфиров аренсульфокислот.
Строение нитробензола. Природа акцепторного влияния нитрогруппы в ароматическом кольце. Физические свойства нитросоединений. Реакции комплексообразования. Электрофильное замещение в ароматическом кольце нитроаренов: скорость реакции и возможность её протекания. Нуклеофильное замещение нитрогруппы и атома водорода. Реакции восстановления нитрогруппы. Сравнение химического поведения нитроаренов с нитрогруппой в боковой цепи: кислотные и нуклеофильные свойства.
Содержание занятия
1. Обсуждение вопросов по теме занятия.
2. Контроль усвоения темы.
Типовые обучающие вопросы и эталоны ответов на них
Вопрос 1. В каком случае при электрофильном замещении в бензольном кольце будет происходить замещение водорода, а в каком — сульфогруппы?
Ответ. Замещение атома водорода в бензольном кольце по электрофильному механизму в общем протекает легче, чем сульфогруппы, что определяется сравнением стабильности катионов уходящих групп Н+ и +SO3Н. Поэтому во всех случаях, когда у атомов углерода ароматического кольца имеются атомы водорода, которые могут быть замещены электрофильной частицей, реакция пойдёт именно по этому направлению. Для замещения сульфогруппы имеются принципиально две возможности: 1) когда электрофильной частицей является катион водорода — это реакция десульфирования:
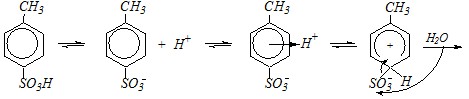
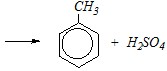
2) в молекуле уже имеется несколько заместителей, в том числе и сульфогруппы, и ни один из них не направляет электрофильную частицу к свободному атому углерода для замещения водородного атома; например:
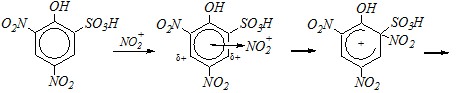
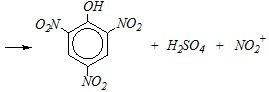
Вопрос 2. Как можно из п-толуолсульфокислоты получить п-нитротолуол? Поясните. Приведите механизм превращения.
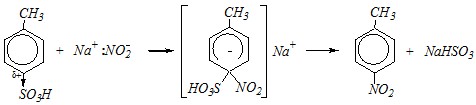
Ответ. Замещением по электрофильному механизму такое превращение осуществить не удастся, так как атом водорода замещается легче, и будет протекать нитрование по 2-му положению:
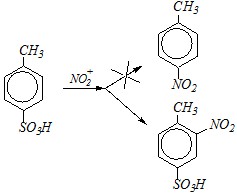
Однако сульфогруппу можно заместить по нуклеофильному механизму при сплавлении с нитритами:
Вопрос 3. Какими способами можно из бензолсульфокислоты получить тиофенол? Приведите схемы и, по возможности, механизмы превращений. Поясните.
Ответ. Превращение бензолсульфокислоты в тиофенол
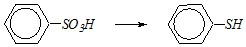
можно осуществить либо нуклеофильным замещением, либо восстановлением сульфогруппы. В первом случае необходимо провести сплавление с сульфидом натрия:
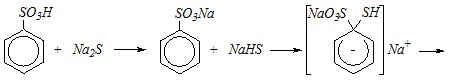
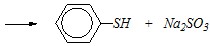
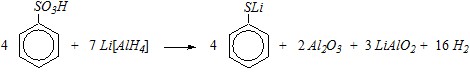
во втором случае — подействовать сильным восстановителем, например, тетрагидроалюминатом лития Li[AlН4]:
Вопрос 4. Гидролиз эфиров аренсульфокислот может протекать как по бимолекулярному, так и по мономолекулярному механизму. Приведите мономолекулярный механизм гидролиза этилтозилата (этил-п-толуолсульфоната). Возможно ли здесь протекание реакции в кислой среде?
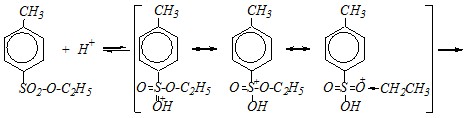
Ответ. Гидролиз эфиров аренсульфокислот протекает по механизму, промежуточному между SN1 и SN2. Кислая среда будет способствовать протеканию реакций по SN1-механизму, как и во всех случаях нуклеофильного замещения у насыщенного атома углерода. За счёт протонирования этил-п-толуолсульфоната в его молекуле ещё в большей степени поляризуется С–О связь.
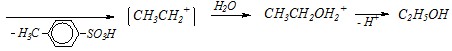
Вопрос 5. В чём различие химического поведения мета - и пара-динитробензолов? Поясните на примере а) нитрования (SE-реакция) и б) взаимодействия со щёлочью (SN-реакция).
Ответ. Нитрогруппа в ароматическом кольце обладает электроноакцепторным эффектом, главным образом за счёт ?-?-сопряжения. При этом значительно понижается электронная плотность в орто - и пара-положениях бензольного кольца по отношения к нитрогруппе. Если в бензольном кольце две нитрогруппы находятся в мета-положении друг к другу, то они оказывают согласованное влияние на бензольное кольцо. Если же нитрогруппы находятся в
о - или п-положении, то их влияние будет несогласованным.
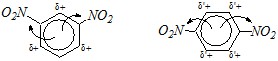
м-динитробензол п-динитробензол
Поэтому, несмотря на то, что в бензольном кольце
м-динитробензола электронная плотность сильно понижена, распределение электронной плотности неравномерное, и 5 положение может подвергаться электрофильной атаке. Так, известно, что м-динитробензол может вступать в реакцию нитрования, хотя и в очень жёстких условиях:

А на атомах углерода п-динитробензола электронная плотность понижена одинаково сильно, её распределение равномерно, и ни один из углеродных атомов п-динитробензола не способен подвергаться электрофильной атаке нитроний-катиона. Это соединение не вступает в реакцию нитрования и другие SE-реакции.
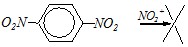
Для нитробензолов более характерными являются реакции нуклеофильного замещения из-за сильно пониженной электронной плотности. При этом более предпочтительным является замещение нитрогруппы, а не атома водорода по причине большей устойчивости NO2?-аниона по сравнению с гидрид-анионом Н?. В молекуле
м-динитробензола активированными для нуклеофильной атаки являются положения 2, 4 и 6, и поэтому замещаться может только атом водорода, находящиеся в одном из этих положений, причём преимущественно в положении 2, где наибольшей степени понижена электронная плотность:

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 |



