FeBr3 + Br2 > Br+[FeBr4]? > FeBr4? + Br+
Образовавшаяся электрофильная частица Br+ может атаковать молекулой этилбензола по бензольному кольцу, что приводит к продуктам электрофильного замещения:

При бромировании на свету без катализатора может протекать только замещение по радикальному механизму, так как молекулы брома в этих условиях претерпевают гомолитическую диссоциацию:
Br2 > 2 Br ?
Замещение протекает по алкильной боковой цепи, причём всегда по ?-углеродному атому, за исключением тех случаев, когда у этого атома отсутствуют С–Н-связи.
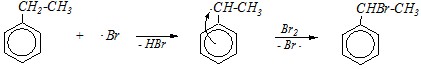
Промежуточный алкильный радикал стабилизирован за счёт р-?-сопряжения, которое возможно только в том случае, если неспаренный электрон находится у ?-углеродного атома.
Присутствие металлического железа при проведении радикальных процессов недопустимо, так как в реакционной среде будет образовываться кислота Льюиса
Fe + Br2 > FeBr3,
которая будет инициировать электрофильное замещение.
Вопрос 4. Установите структуру исходного ароматического углеводорода, если при его озонолизе была получены 2-оксопропаналь и этандиаль в мольном соотношении 1:2.
Ответ. Для того, чтобы привести схему озонолиза ароматического углеводорода, надо представить бензольное кольцо в его структуре в виде чередующихся двойных связей. Тогда для моноалкилбензола в общем виде это будет выглядеть так:
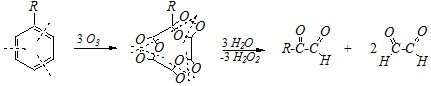
Продуктами данной реакции являются
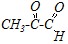 и
и 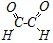
в том же мольном соотношении. Поэтому R = CH3 , а исходный ароматический углеводород — толуол.
Контрольные вопросы и задачи
Перечислите все электрофильные частицы и сравните их активность в реакциях а) нитрования, б) сульфирования, в) галогенирования, г) ацилирования, д) алкилирования. Из бензола и изопропилхлорида в присутствии хлорида алюминия получите монозамещенный гомолог бензола. Приведите механизм этой реакции. Для полученного алкилбензола приведите схемы превращений при а) окислении KMnO4, б) бромировании в присутствии железа, в) бромировании при нагревании на свету. Из бензола получите этилбензол, используя в качестве одного из исходных веществ а) этилен, б) этанол. Для одного из взятых реагентов а) или б) рассмотрите механизм реакции. Для этилбензола напишите схемы реакций: а) окисления, б) сульфирования, в) бромирования в условиях радикального замещения. Какие углеводороды получатся при алкилировании толуола пропиловым спиртом в присутствии серной кислоты? Объясните, почему группа - СН3 обладает активирующим действием и является преимущественно о - и п-ориентантом. Для одного из диалкилзамещенных бензола приведите схему окисления перманганатом калия. Приведите механизм алкилирования толуола изобутилхлоридом в присутствии хлорида алюминия. Какое соединение будет основным продуктом этой реакции? Какое превращение будет протекать при нагревании изобутилбензола на хлориде алюминия при 470 К? Приведите его механизм и поясните. Установите в каждом случае структуру исходного ароматического углеводорода, если при его озонолизе с последующим гидролизом была получена смесь карбонильных соединений следующего состава (в скобках указаны их мольные соотношения):а) бутандион, 2-оксопропаналь, этандиаль (1:2:3); б) бутандион, 2-оксопропаналь, этандиаль (1:4:1); в) пентандион-2,3, 2-оксо-бутаналь, этандиаль (1:1:1); г) 2-оксопропандиаль, 2,3-диоксо-бутаналь, 2-оксопропаналь, этандиаль, этаналь (1:1:1:3:2).
Занятие 25. алициклические и ароматические углеводороды
Содержание занятия
1. Контрольная работа.
Вопросы для подготовки к контрольной работе
Алициклические углеводороды: номенклатура, строение, свойства. Особенности поведения малых циклов. Терпены, терпеноиды, каротиноиды — тривиальные названия, нахождение в природе, биологическая роль. Стероиды как неомыляемые липиды. Классификация стероидов. Пространственное строение стероидов. Важнейшие представители разных групп стероидов и их медико-биологическое значение. Бензол, его строение и свойства. Ароматичность. Реакции присоединения, окисления, изомеризации. Механизм реакций электрофильного замещения. Электрофильные частицы и условия их образования. Частные случаи реакций и их особенности (нитрование, сульфирование, галогенирование, ацилирование, алкилирование, нитрозирование, карбоксилирование, азосочетание). Ароматические углеводороды. Свойства ароматического кольца в сравнении с бензолом. Свойства боковых углеводородных цепей в молекулах аренов: реакции замещения, окисления, присоединения, дегидрирования.Занятие 26. Влияние заместителей в бензольном кольце. галогенарены
Вопросы для подготовки к занятию
Электронные эффекты заместителей в бензольном кольце: индуктивный и мезомерный; их влияние на распределение электронной плотности в бензольном кольце и на скорость электрофильных реакций. Заместители I и II рода. Факторы, влияющие на направление реакций электрофильного замещения. Роль стерического (пространственного) фактора.
Классификация и номенклатура (радикало-функциональная, заместительная) галогенаренов. Строение арилгалогенидов: особенности распределения электронной плотности в ароматическом кольце и особенности влияния галогенов в бензольном кольце на скорость и направление электрофильных реакций. Электрофильное замещение в ароматическом кольце арилгалогенидов. Нуклеофильное замещение в ароматическом кольце арилгалогенидов: механизмы ариновый (ЕА) и SN2аром. Взаимодействие арилгалогенидов с металлами. Свойства галогенаренов с атомом галогена в боковой цепи: реакции электрофильного и нуклеофильного замещения.
Содержание занятия
1. Обсуждение вопросов по теме занятия.
2. Контроль усвоения темы.
Типовые обучающие вопросы и эталоны ответов на них
Вопрос 1. В чём различие во влиянии на бензольное кольцо заместителей - СООСН3 и - ООССН3? Каков суммарный электронный эффект (донорный или акцепторный) заместителя в каждом из ароматических соединений? Какова ориентация каждого из этих заместителей по отношению к вступающему электрофилу?
Ответ. Данные ароматические соединения представляют собой изомерные сложные эфиры, однако бензольное кольцо каждого из них соединено с разными по природе заместителями.
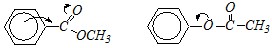
метилбензоат фенилацетат
В первом соединении, метилбензоате, заместитель понижает электронную плотность на ароматическом кольце за счёт –I и –М (?-?-сопряжение) эффектов, поэтому суммарный эффект акцепторный; и является м-ориентантом (реакции электрофильного замещения протекают преимущественно по мета-положению). Второе соединение, фенилацетат, является производным фенола и воздействует на кольцо за счёт атома кислорода, имеющего неподелённую пару электронов (р-?-сопряжение). Этот эффект — донорный мезомерный (+М), и он превосходит –I-эффект, проявляемый этим заместителем по отношению к бензольному кольцу. Поэтому суммарный эффект донорный, и заместитель является о-п-ориентантом (засчёт +М-эффекта), то есть направляет вступающие в бензольное кольцо электрофильные частицы в о - и п-положения.
Вопрос 2. Какими электронными эффектами обладают атомы галогенов (F, Cl, Br, I) по отношению к бензольному кольцу? Каков суммарный электронный эффект (донорный или акцепторный) для каждого из галогенов?
Ответ. Атомы галогенов в галогенобензолах проявляют –I-эффект за счёт их большей электроотрицательности по сравнению с атомом углерода, несмотря на то, что в случае йода электроотрицательности атомов С и I близки — здесь основную роль играет поляризуемость связи C–I. Кроме индуктивного, для атомов галогенов характерен мезомерный эффект за счёт неподелённой электронной пары (одной из трёх внешних) — это р-?-сопряжение (+М-эффект).
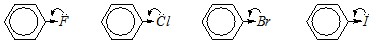
Во всех случаях величина индуктивного эффекта по модулю больше величины мезомерного эффекта. Так, фтор наиболее электроотрицателен, и донорный эффект (мезомерный) его незначителен. Электроотрицательность от хлора к йоду уменьшается хотя и значительно, но в том же ряду сильно увеличиваются размеры орбиталей внешнего уровня (на котором находится неподелённая пара электронов), поэтому взаимодействие такой орбитали с р-орбита-лями атомов углерода бензольного кольца будет всё менее эффективным. Другими словами, одновременно с уменьшением
–I-эффекта атома галогена (от фтора к йоду) происходит и уменьшение +М-эффекта. Уменьшение индуктивного эффекта связано с понижением электроотрицательности в ряду галогенов (фтор — йод); уменьшение электронодонорного мезомерного эффекта связано с возрастанием несоответствия геометрической конфигурации внешних р-орбиталей атомов углерода и галогена (также от фтора к йоду). Поэтому суммарный электронный эффект во всех случаях акцепторный.
Вопрос 3. Почему в одних случаях атом хлора в бензольном кольце замещается по механизму SN2аром., а в других — по ЕА-механизму?
Ответ. Так как атом хлора относится к относительно слабым электроноакцепторам в бензольном кольце (он проявляет акцепторный индуктивный, но донорный мезомерный эффекты), то в результате его влияния ни на одном из углеродных атомов ароматического кольца не возникает значительного положительного заряда, достаточного для осуществления нуклеофильной атаки. Значительно меньших энергетических затрат требует отрыв катиона водорода и последующий выброс хлорид-аниона (ароматичность кольца при этом сохраняется) — это ариновый механизм (ЕА):
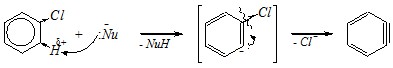

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 |



