Контрольные вопросы и задачи
Напишите структурные формулы следующих соединений:
а) гидразона 10-бром-2-антраценкарбальдегида; б) 8-ацетил-1-фенантренкарбонилхлорида. Сравните ароматический и непредельный характер бензола, нафталина, антрацена и фенантрена. Приведите примеры реакций, подтверждающих это. Какое из соединений — антрацен или фенантрен — будет легче окисляться раствором KMnO4? Объясните. Какое из соединений — антрацен или фенантрен — будет легче гидрироваться? Какие продукты образуются при взаимодействии с холодной концентрированной азотной кислотой и с концентрированной азотной кислотой при нагревании до 100°С антрацена, фенантрена? Как будет взаимодействовать антрахинон-9,10 а) с нитрующей смесью, б) с олеумом, в) с хлорметаном в присутствии хлорида алюминия. Приведите механизмы реакций. Приведите механизм взаимодействия антрацена с хлором на свету: а) с 1 молем, б) с избытком. Какие продукты образуются при действии газообразного хлора на 9-аминоантрацен? Реакцией Вюрца–Фиттига получите 2,3,6,7-тетраметилантрацен, используя любые галогенарены. Рассмотрите механизм реакции. Для продукта реакции приведите схемы: а) окисления, б) сульфирования, в) бромирования в условиях радикального замещения.
Занятие 34. полициклические ароматические соединения
Содержание занятия
1. Контрольная работа.
Вопросы для подготовки к контрольной работе
Нафталин, антрацен, фенантрен: строение, сравнение ароматичности. Ароматический и диеновый характер молекул. Химические свойства нафталина, антрацена, фенантрена: реакции присоединения, окисления, электрофильного замещения. Примеры присоединения водорода, галогенов, галогеноводородов. Особенности протекания реакций. Реакции окисления нафталина, антрацена, фенантрена и их производных. ?-Нафтиламин, нафтолы. Особенности химического поведения: реакции замещения, окисления. Нафтохинон: строение, свойства, получение. Биохимическое значение многоядерных конденсированных углеводородов и их производных.Занятие 35. пятичленные гетероциклы с одним гетероатомом
Вопросы для подготовки к занятию
Пятичленные азото-, кислородо - и серосодержащие насыщенные и ароматические гетероциклические соединения. Строение фурана, пиррола, тиофена. Кислотно-основные свойства фурана, пиррола, тиофена; ацидофобность; реакции электрофильного замещения, присоединения, окисления, расширения цикла, замены гетероатома. Индол: особенности строения, химического поведения. Медико-биологическое значение пятичленных гетероциклов и их производных.
Содержание занятия
Обсуждение вопросов по теме занятия. Контроль усвоения темы.Типовые обучающие вопросы и эталоны ответов на них
Вопрос 1. Докажите наличие у пиррола кислотно-основных свойств.
Ответ. Пиррольный атом азота, связанный с атомом водорода, может служить центром кислотности. Пиррол ведет себя как слабая NH-кислота. Поэтому протон будет отщепляться только при действии только сильных оснований, таких, как амид натрия NaNH2 или гидроксид калия KOH (при 130°C). Щелочные металлы также могут замещать атом водорода у пиррольного атома азота.
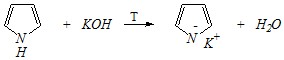
пиррил-калий
Пиррольный атом азота не склонен присоединять протон, т. е. не является центром основности. Это объясняется тем, что неподелённая пара электронов пиррольного атома азота находится на негибридной p-орбитали и участвует в сопряжении:
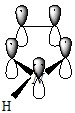
Пиррол в сильнокислой среде неустойчив. Такая неустойчивость в сильнокислой среде называется ацидофобность (что означает «кислотобоязнь»). Ацидофобность связана с присоединением протона в большинстве случаев к ?-углеродному атому, разрушением ароматической системы и дальнейшим превращением активной диеновой системы:
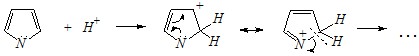
Происходит «осмоление» (олигомеризация и полимеризация).
Вопрос 2. Приведите механизмы превращений фурана, тиофена под действием а) холодной концентрированной серной кислоты,
б) пиридин-сульфотриоксида. Объясните направление реакции в каждом случае.
Ответ. Фуран и тиофен взаимодействуют с сильными кислотами, в случае фурана происходит «осмоление» (олигомеризация и полимеризация), тиофеновое кольцо к разрушению под действием холодных кислот устойчиво. Фуран ацидофобен. Ацидофобность связана с присоединением протона в большинстве случаев к ?-углеродному атому, разрушением ароматической системы и дальнейшим превращением активной диеновой системы:
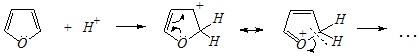
Сульфировать серной кислотой можно только тиофен:
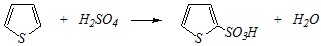
2-тиофенсульфокислота
Для сульфирования фурана по причине его ацидофобности используют пиридин-сульфотриоксид:
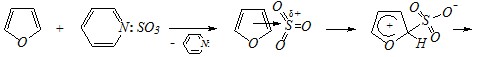
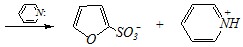
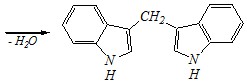
Вопрос 3. Взаимодействие индола с формальдегидом протекает по схеме:
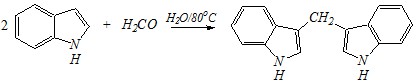
Приведите механизм и объясните направление этого превращения.
Ответ. По отношению к индолу как к субстрату данное взаимодействие представляет собой реакции электрофильного замещения, в которые последовательно вступают сначала одна, а затем другая молекула индола:
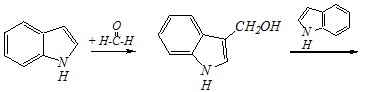
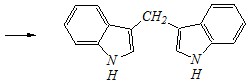
Как и другие реакции электрофильного замещения, взаимодействие с альдегидами протекает по ?-положению ввиду большей устойчивости образующегося в этом случае ?-комплекса:
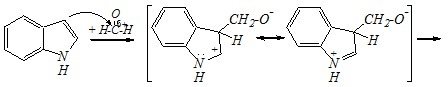
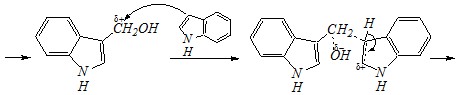
Контрольные вопросы и задачи
Укажите, по каким критериям пиррол, фуран и тиофен относятся к ароматическим соединениям? Объясните причину неравномерного распределения электронной плотности в кольце. Объясните причины наличия кислотных свойств у пиррола и индола. Могут ли они вступать в реакцию Чугаева–Церевитинова? Поясните. Обладают ли эти соединения основными свойствами? Приведите механизмы превращений тиофена под действием а) холодной концентрированной серной кислоты, б) холодного серного ангидрида, в) комплекса серного ангидрида с донором. Объясните направление реакции в каждом случае. Какое соединение образуется в результате взаимодействия пиррола с гидридом натрия и затем с йодметаном? Приведите механизм декарбоксилирования пирролкарбоновых кислот при нагревании. Приведите реакции с участием фуранов, подтверждающие более низкую ароматичность фурана по сравнению с тиофеном и пирролом (реакции, приводящие к образованию неароматических продуктов). Существуют ли 2-гидроксифураны? Ответ мотивируйте. Какие фенилгидразоны необходимы для проведения синтеза следующих индолов по реакции Фишера: 3-метилиндола, 2-метил-3-этилиндола, 3-этил-2-фенилиндола? Приведите необходимые схемы и механизмы превращений.
Занятие 36. пятичленные гетероциклы с двумя гетероатомами
Вопросы для подготовки к занятию
Строение диазолов, оксазола, изоксазола, тиазола, изотиазола. «Пиррольный» и «пиридиновый» атомы азота. Ароматичность в сравнении пятичленными гетероциклами с одним гетероатомом и бензолом. Кислотно-основные свойства имидазола и пиразола, реакции электрофильного замещения, реакции алкилирования. Медико-биологическое значение пятичленных гетероциклов и их производных. Бензимидазол и бензотиазол: особенности строения, химического поведения; медико-биологическое значение.
Содержание занятия
Обсуждение вопросов по теме занятия. Контроль усвоения темы.Типовые обучающие вопросы и эталоны ответов на них
Вопрос 1. Приведите механизм реакции сульфирования пиразола. Объясните направление реакции. Как будет реагировать пиразол с разбавленной серной кислотой?
Ответ. Механизм реакции сульфирования — электрофильное замещение. Сульфирование происходит при воздействии концентрированной серной кислоты:
3 H2SO4 > H2S2O7 + H3O+ + HSO4?
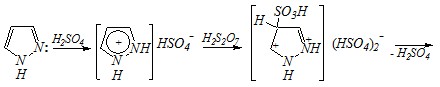
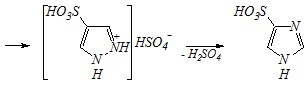
4-пиразолсульфокислота
В водном растворе серной кислоты:
H2SO4 + H2O > H3O+ + HSO4?
Разбавленная серная кислота не сульфирует. В результате присоединения протона образуются стабильный катион:
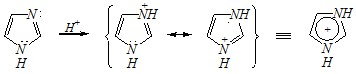
катион пиразолия
Вопрос 2. Почему оксазол и тиазол значительно менее активны в электрофильных реакциях, чем диазолы? Предложите механизм сульфирования тиазола.
Ответ. Оксазол не подвергается нитрованию и сульфированию. Причину можно видеть в значительно меньшем электронодонорном эффекте атома кислорода в этом гетероцикле, чем пиррольного азота, например в имидазоле. Это проявляется не только в молекулярной форме, но и в протонированном состоянии. По аналогичной причине тиазол не вступает в реакцию нитрования.
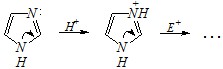
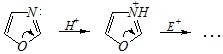
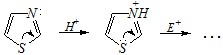
Однако тиазол может быть подвергнут сульфированию (в жёстких условия, в присутствии HgSO4). Причиной осуществления такой реакции в случае тиазола может быть взаимодействие мягкого осн?вного центра (атом серы) в его молекуле с мягким кислотным центром, каким является катион Hg+. Это исключает протонирование на первой стадии и делает молекулу более реакционноспособной. Возможный механизм:

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 |



