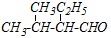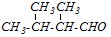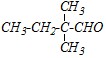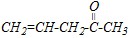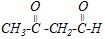Ответ. Окисление альдегидов протекает легко за счёт наличия подвижного атома водорода в альдегидной группе. В качестве окислителей обычно применяют влажный оксид серебра, раствор перманганата калия или фелингову жидкость. Качественной реакцией на альдегиды (для отличия их от кетонов) обычно считается реакция серебряного зеркала — взаимодействие альдегидов с гидроксидом диамминсеребра (реактивом Толленса). Из уксусного альдегида, таким образом, получается уксусная кислота (в виде аммонийной соли):
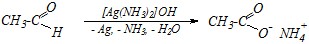 .
.
В отличие от альдегидов кетоны подвергаются действию окислителей в жёстких условиях. Так, диоксид селена окисляет
?-метиленовую группу до карбонильной. Поэтому из гексанона-3 получится соответствующие изомерные ?-дикетоны:
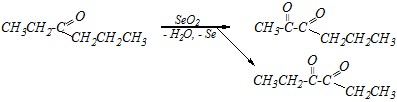
А действие сильных окислителей (например, хромовой смеси) при нагревании приводит к окислению одного из ?-углеродных атомов и разрыву C-C-связи по обе стороны от карбонильной группы:

При этом из каждого осколка образуется молекула карбоновой кислоты, и получается смесь трёх кислот (в общем случае — смесь четырёх кислот).
Вопрос 4. Какова должна быть структура соединений, чтобы реакции альдольной и кротоновой конденсации для них были возможны? Приведите механизм этих реакций для изовалерианового альдегида.
Ответ. Альдольная и кротоновая конденсации характерны для альдегидов и кетонов, имеющих ?-водородные атомы. При альдольной конденсации происходит присоединение одной молекулы карбонильного соединения к другой молекуле; образуется альдегидоспирт (альдоль). При кротоновой конденсации из двух молекул карбонильного соединения образуется молекула непредельного альдегида или кетона; процесс сопровождается выделением молекулы воды.
Реакции обычно проводят в присутствии оснований, однако возможен и кислотный катализ. В качестве оснований для катализа используют 5–10%-й раствор щёлочи. Реакция начинается с отрыва протона от ?-углеродного атома изовалерианового альдегида:
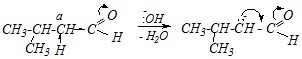
При этом образуется карбониевый анион, стабилизированный р-?-сопряжением. Дальнейшее превращение происходит за счёт проявления им нуклеофильных свойств по отношению ко второй молекуле альдегида:
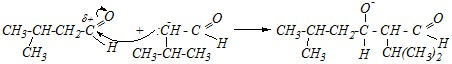
Образовавшийся анион отрывает протон от молекулы воды, сам превращаясь в молекулу альдоля:
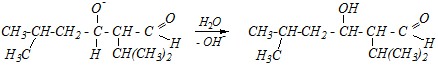
Дальнейшее превращение альдоля также связано с отрывом
?-водородного атома от того же атома углерода (находящегося между функциональными группами) под действием щёлочи, а затем происходит отщепление гидроксид-иона от образовавшегося карбониевого аниона:
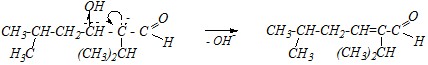
Вопрос 5. Каковы будут продукты реакции Канниццаро, если в неё вступают два альдегида: муравьиный и трихлоруксусный? Приведите механизм.
Ответ. Это реакция диспропорционирования альдегидов, в которой одна молекула окисляется до кислоты, а другая восстанавливается до спирта. Реакция протекает при участии концентрированного водного раствора щёлочи (40–50%) и характерна для альдегидов, не содержащих ?-водородных атомов. В противном случае в этих условиях будет проходить альдольная (и кротоновая) конденсация с участием ?-водородных атомов.
Реакция начинается с обратимого присоединения гидроксид-иона по двойной связи C=О. И если реакция Канниццаро протекает в смеси двух альдегидов, то атаке гидроксид-анионом будет подвергаться альдегид, более реакционноспособный по отношению к нуклеофилам. Так, если одним из альдегидов является трихлоруксусный альдегид, то гидроксид-ион взаимодействует с карбонильным атомом углерода именно этого альдегида за счёт значительного положительного заряда на этом атоме:
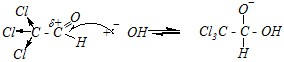 ,
,
а затем от образовавшегося аниона происходит отрыв гидрид-иона и его взаимодействие с карбонильным атомом углерода молекулы муравьиного альдегида:
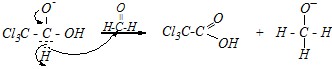 .
.
По завершении нуклеофильной атаки происходит быстрая миграция протона от молекулы карбоновой кислоты к алкоголят-иону:
Cl3C–COOH + CH3O? > Cl3C–COO? + CH3OH
Контрольные вопросы и задачи
Назовите:
Приведите AN-механизм реакции присоединения воды, метанола, синильной кислоты, аммиака, метиламина, гидросульфита натрия к следующим карбонильным соединениям: 1) пропаналю, 2) 2-метил-бутаналю, 3) пентанону-2, 4) 3-метилбутанону-2. В каких случаях возможно применение кислотного катализатора, в каких случаях возможно применение основного катализатора? Приведите возможные схемы окисления и восстановления следующих альдегидов и кетонов: 1) пропаналя, 2) бутанона-2,
3) пентанона-3. Приведите механизм альдольной конденсации для 2,3-диметил-бутаналя. Приведите механизм реакции Канниццаро для 2,2-диметил-бутаналя. Как протекает реакция бромирования в кислой и щелочной среде бутанона-2?
Лабораторная работа
Опыт 1. Отношение формальдегида и ацетона
к окислению гидроксидом диамминсеребра
Для получения «серебряного зеркала» необходимо сначала подготовить пробирки. Возьмите две пробирки и в каждую из них поместите по 5 мл 10%-го раствора гидроксида натрия NaOH и осторожно кипятите в течение 1–2 мин., а затем тщательно ополосните их дистиллированной водой. В подготовленные пробирки вносят по 5 капель 5%-го раствора нитрата серебра AgNO3, добавляют приблизительно по 1 мл воды и затем прибавляют по каплям при встряхивании 10%-й водный раствор аммиака до полного его растворения выпавшего осадка. Затем в первую пробирку прибавьте 2 капли 40%-го формалина, а во вторую — 2 капли ацетона и опустите пробирки на несколько минут в водяную баню. Отметьте все изменения, происходящие в пробирках.
Напишите уравнение реакции «серебряного зеркала». Чем объясняется выпадение осадка черного цвета в первой пробирке?
Объясните, почему во второй пробирке не наблюдается выпадение осадка.
Опыт 2. Открытие ацетона переводом его в йодоформ
Эта реакция используется в клинических лабораториях и имеет практическое значение для диагностики сахарного диабета.
В пробирку поместите 1 каплю раствора йода в йодиде калия и прибавьте почти до обесцвечивания по каплям 10%-й раствор гидроксида натрия. К обесцвеченному раствору добавьте 1 каплю ацетона. При слабом нагревании от тепла рук выпадает желтовато-белый осадок с характерным запахом йодоформа.
Приведите схему реакции образования йодоформа.
Занятие 12. системы ?-связей
Содержание занятия
1. Контрольная работа.
Вопросы для подготовки к контрольной работе
Номенклатура непредельных углеводородов. Механизм реакций электрофильного присоединения. Влияние структуры субстрата на направление протекания реакции. Стереоселективность электрофильного присоединения. Примеры электрофильного присоединения воды, галогенов, галогеноводородов, борана, озона. Особенности реакций АЕ-присоединения по тройной связи. Особенности реакций АЕ-присоединения к диеновым углеводородам. Реакции 1,2- и 1,4-присоединения к сопряжённым диенам. Особенности полимеризации сопряжённых диенов. Механизм реакций радикального присоединения. Примеры реакций. Реакции каталитического гидрирования и комплексообразования. Реакции радикального замещения в ряду непредельных углеводородов: хлорирование и пероксидное окисление. Алкены: особенности изомерии. Примеры реакций АЕ и АR. Изомеризация, полимеризация, теломеризация. Реакции окисления. Строение, изомерия и особенности свойств алленов. Особенности строения и химических свойств сопряжённых диенов. Реакции диенового синтеза. Особенности строения алкинов и реакций присоединения по тройной связи. Кислотные свойства алкинов. Возможность протекания реакций нуклеофильного присоединения и электрофильного замещения. Классификация функциональных производных непредельных углеводородов. Строение субстратов винильного и аллильного типа. Галогеналкены и простые эфиры винильного типа: особенности реакционной способности в SN и АЕ-реакциях. Виниловый спирт, его эфиры и полимеры на их основе. Понятие о кето-енольной таутомерии. Особенности реакционной способности в SN-реакциях соединений аллильного типа: аллилгалогенидов, аллилового и пропаргилового спиртов. Классификация оксосоединений. Строение оксогруппы. Реакции нуклеофильного присоединения к альдегидам и кетонам, механизм, роль катализатора. Сравнение реакционной способности оксогруппы альдегидов и кетонов. Реакции конденсации оксосоединений. Реакции замещения в углеводородном радикале альдегидов и кетонов. Реакции окисления и восстановления. Особенности окисления кетонов. Полимеризация карбонильных соединений. Параформ. Особенности ?, ?-ненасыщенных альдегидов. Дикарбонильные соединения: строение, свойства. Таутомерия ?-дикарбонильных соединений. Ацетилацетон и его свойства.Занятие 13. предельные монокарбоновые кислоты и их производные
Вопросы для подготовки к занятию
Номенклатура карбоновых кислот и их производных. Строение карбоксильной и ацильной групп. Кислотные и основные свойства карбоновых кислот и производных. Реакции нуклеофильного замещения в ряду карбоновых кислот и их ацильных производных, механизм, роль катализатора. Сравнение их реакционной способности. Другие реакции карбоновых кислот, их солей, амидов (реакции с участием ?-водородных атомов — Гелля–Фольгарда–Зелин-ского, декарбоксилирование, перегруппировка по Гофману). Особенности получения и химического поведения нитрилов. Жиры как сложные эфиры глицерина: строение, состав. Общая характеристика карбоновых кислот, входящих в состав жиров. Общее представление о строении и физиологической роли фосфатидов.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 |