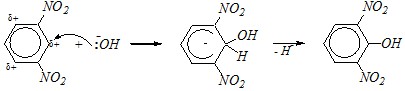
В молекуле п-динитробензола активированными для нуклеофильной атаки являются все углеродные атомы бензольного кольца (по причине несогласованного влияния нитрогрупп) и, прежде всего, 1 и 4 атомы (у которых имеются нитрогруппы). Поэтому замещаться будет одна из нитрогрупп (она находится в п-положении к другой нитрогруппе):
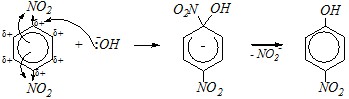
Замещение нитрогруппы протекает в более мягких условиях, чем атома водорода: для этого используются водные растворы щелочей, а для замещения водорода необходимо нагревание с твёрдой щёлочью.
Контрольные вопросы и задачи
Сравните кислотные свойства следующих соединений: п-нитро-бензолсульфокислоты, бензолсульфокислоты, п-хлорбензол-сульфокислоты, о-толуолсульфокислоты, воды. Объясните. Какое из предложенных соединений наиболее легко десульфируется: бензолсульфокислота, п-хлорбензолсульфокислота, о-то-луолсульфокислота, п-нитробензолсульфокислота. Поясните. Приведите механизм реакции. Объясните, почему для ароматических сульфокислот возможны реакции замещения сульфогруппы как по электрофильному, так и по нуклеофильному пути. Сравните условия протекания этих реакций. Какие продукты образуются при взаимодействии п-изопропил-бензолсульфокислоты а) с концентрированной серной кислотой, б) с избытком нитрующей смеси, в) с кипящей очень разбавленной соляной кислотой? Приведите механизмы реакций. Приведите три уравнения реакций хлорирования п-толуолсуль-фокислоты: а) хлором в присутствии железа, б) хлором на свету,
в) пентахлоридом фосфора (V). Приведите механизмы этих реакций. Приведите механизм нуклеофильного замещения для 1,2,3-три-нитробензола при взаимодействии с гидроксидом натрия. Какая нитрогруппа заместится в первую очередь и сколько нитрогрупп заместится всего при избытке нуклеофильного реагента? Поясните. Приведите механизм реакции. Какие продукты образуются при взаимодействии ?, п-динитро-толуола а) с нитрующей смесью, б) с разбавленным водным раствором щёлочи? Приведите механизмы реакций.
Занятие 28. фенолы и ароматические спирты. Хиноны
Вопросы для подготовки к занятию
Строение фенола и бензилового спирта. Природа влияния заместителя в ароматическом кольце. Физические свойства фенолов. Кислотно-основные и нуклеофильные свойства фенолов и спиртов. Характерные реакции, отличающие эти два класса соединений. Электрофильное замещение в ароматическом кольце фенолов: скорость, глубина протекания реакций; реакции со слабыми электрофилами. Нуклеофильное замещение гидроксогруппы. Реакции окисления и восстановления. Фенолы и их производные. Простые эфиры фенолов. Хиноны: получение и особенности свойств. Нахождение в природе хинонов. Медико-биологическое значение фенолов и их производных.
Содержание занятия
1. Обсуждение вопросов по теме занятия.
2. Контроль усвоения темы.
Типовые обучающие вопросы и эталоны ответов на них
Вопрос 1. Какой продукт будет образовываться при взаимодействии п-гидроксибензилового спирта с разбавленным водным раствором щелочи? Приведите схему реакции.
Ответ. Молекула п-гидроксибензилового спирта содержит две гидроксильные группы обладающие разным характером: фенольную и спиртовую. У спиртов кислотные свойства выражены слабее, чем у воды, и поэтому они не реагируют со щелочами. Фенолы, наоборот, дают соли при взаимодействии с водными растворами щелочей. Причина этого — р-?-сопряжение, в котором участвует неподелённая электронная пара кислорода и ?-электронная система бензольного кольца, приводящее к большей поляризации связи О–Н :
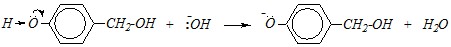
Вопрос 2. В чём различие взаимодействия фенола а) с концентрированными серной и азотной кислотами, б) с разбавленными серной и азотной кислотами (при нагревании)? Приведите схемы превращений.
Ответ. При взаимодействии с концентрированной серной кислотой происходит сульфирование фенола, причём недостаток реагента селективно приводит к образованию орто - или пара-изомера в зависимости от температуры:
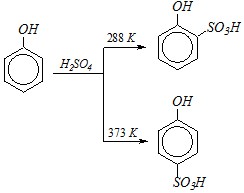
Образования различных структурных изомеров при разной температуре объясняется обратимостью реакции сульфирования и большей термодинамической стабильностью п-изомера, который накапливается в реакционной среде при повышенной температуре.
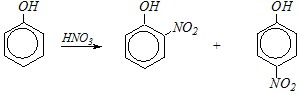
Действие концентрированной азотной кислоты на фенол приводит к электрофильному нитрованию, происходит введение одной, двух и трёх нитрогрупп в молекулу фенола. При недостатке реагента возможно образование мононитропроизводных, но реакция протекает неселективно, что приводит к получению смеси орто - и пара-изомеров:
Разбавленная серная кислота сульфирующими свойствами не обладает и может участвовать только в протонировании. Но основность фенолов выражена крайне слабо, и протонированию (с образованием солей) они не подвергаются.
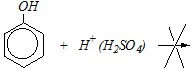
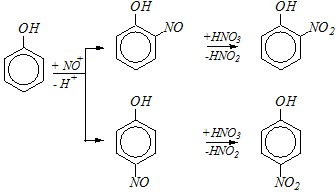
Разбавленная азотная кислота, аналогично серной, также не обладает нитрующими свойствами: в ней не образуется необходимый для нитрования нитроний-катион. Однако при нагревании происходит разложение азотной кислоты до диоксида азота NO2, из которого в реакционной среде образуется нитрозо-катион, и протекает нитрозирование фенола с последующим окислением образовавшегося нитрозофенола:
2 NO2 > NO+ + NO3?
Вопрос 3. Как реагируют фенолы с альдегидами? Рассмотрите механизм реакции на примере взаимодействия 2,6-диметилфенола с этаналем.
Ответ. За счёт наличия в ароматическом кольце гидроксогруппы, которая является сильным электронодонором, фенолы легко вступают в реакции SE и могут взаимодействовать со слабыми электрофилами, например, с альдегидами. Поэтому реакция с этаналем — это типичная реакция электрофильного замещения, в которой
2,6-диметилфенол является субстратом, а этаналь — электрофилом. С другой стороны, по отношению к альдегидам это реакция нуклеофильного присоединения, в которой нуклеофилом является молекула фенола. Таким образом, механизм этой реакции можно квалифицировать и как SE, и как AN, в зависимости от того, что считать субстратом, а что — нуклеофилом. С учётом того и другого механизм реакции можно описать в следующем виде:
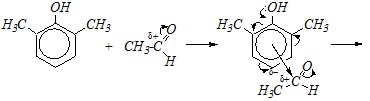
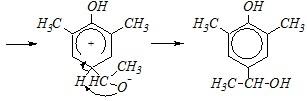
Вопрос 4. Приведите механизмы реакций алкилирования фенола бромэтаном а) в щелочной среде, б) в присутствии кислотного катализатора.
Ответ. В щелочной среде молекула фенола превращается в фенолят-ион. Отрицательный заряд этого иона в какой-то степени делокализован по всей частице, но преимущественно локализован на атоме кислорода. Таким образом, нуклеофильность такой частицы высокая и, главным образом, за счёт атома кислорода; нуклеофильная атака осуществляется атомом кислорода:
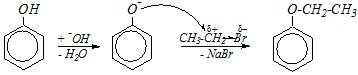
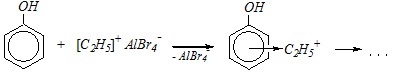
Однако в кислой среде молекула фенола практически не ионизирована (диссоциация подавлена), и за счёт делокализации неподелённой электронной пары атома кислорода избыточный отрицательный заряд возникает на орто - и пара-атомах бензольного кольца. Кислая среда (или, как вариант, кислотный катализатор) молекулу субстрата (в данном случае, бромэтана), облегчая, тем самым, образование углерод-углеродных связей. В результате осуществляется алкилирование в бензольное кольцо по Фриделю-Крафтсу:
![]()
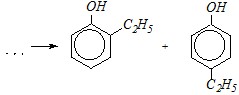
Вопрос 5. В чём различие ацилирования фенола в обычных условиях без катализатора и в присутствии кислотного катализатора? Приведите механизмы реакций.
Ответ. В обычных условиях (или в присутствии карбонатов) происходит ацилирование по атому кислорода. В реакцию вступает фенолят-ион, образующийся при диссоциации молекулы фенола (карбонаты способствуют отрыву протона от молекулы фенола и, тем самым, увеличивают концентрацию фенолят-иона):
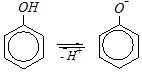
или
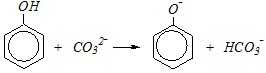
Дальнейшее взаимодействие фенолят-иона с ангидридами или галогенангидридами карбоновых кислот — это типичное нуклеофильное замещение, характерное для ацильных производных карбоновых кислот:
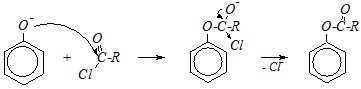
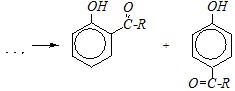
При применении кислот Льюиса (среда кислая) ацилирование протекает по атомам углерода бензольного кольца, потому что как и в случае алкилирования (см. предыдущий вопрос) диссоциация фенола подавлена, но активированы о - и п-положения ароматического кольца. Это типичная реакция Фриделя-Крафтса в ароматическом ряду:
![]()
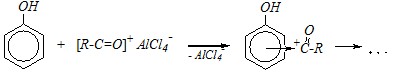
Контрольные вопросы и задачи
Сравните кислотные свойства следующих соединений: фенол,
п-нитрофенол, п-хлорфенол, о-нитрофенол, м-нитрофенол. Объясните. Сравните реакционную способность в реакциях электрофильного нитрования следующих соединений: м-крезол, резорцин, фенол, бензиловый спирт, 1-фенилэтанол-1. Объясните. Приведите механизмы реакций. Приведите механизмы реакций взаимодействия с бромной водой следующих соединений: о-крезол, анизол, фенил-трет-бутиловый эфир. Приведите механизмы реакций метилирования в щелочной среде а) п-крезола, б) гидрохинона, в) п-нитрофенола. Сравните их реакционную способность. Объясните. Приведите механизмы реакций ацилирования пирокатехина а) изомасляным ангидридом, б) муравьино-уксусным ангидридом, в) янтарным ангидридом в обычных условиях без катализатора. Какие продукты могут образоваться при а) взаимодействии бензилового спирта с концентрированной соляной кислотой, б) взаимодействии бензилового спирта с концентрированной серной кислотой? Приведите схемы реакций и названия веществ. Какой продукт преимущественно будет образовываться при
а) метилировании гидрохинона избытком йодметана в щелочной среде, б) взаимодействии гидрохинона с броматом калия? Приведите схемы реакций и названия веществ.
Занятие 29. ароматические амины и их производные.
азо - и диазосоединения

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 |



