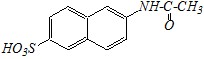
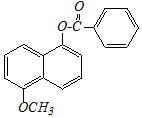
Нафталин обладает меньшей ароматичностью, чем бензол. Энергия делокализации нафталина (255 кДж/моль) меньше, чем для двух молекул бензола (301 кДж/моль), и поэтому нафталин более реакционноспособен, чем бензол. Большую реакционную способность нафталина можно также объяснить, если рассматривать одно из колец как ароматическое, а другое — как диеновую систему:

Нафталин проявляет более ненасыщенный характер, чем бензол, легче чем бензол вступает в реакции присоединения.
Вопрос 2. В чём различие реакций сульфирования и нитрования нафталина?
Ответ. Это типичные реакции электрофильного замещения, и преимущественным направлением их протекания должно быть образование ?-производных (см. учебник, гл.11.2.2.1). Сульфирование при 60°С действительно приводит к образованию 1-нафталинсульфокислоты:
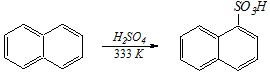
Однако повышение температуры вызывает увеличение скорости не только прямой, но и обратной реакции (сульфирование обратимо!), и реакции образования 2-нафталинсульфокислоты:
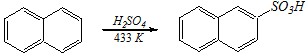
Этот продукт термодинамически более стабилен и с течением времени при проведении реакции при повышенных температурах будет накапливаться в реакционной смеси. Дальнейшее сульфирование в этих условиях (при продолжительном нагревании) приведёт к образованию смеси 2,6- и 2,7-нафталиндисульфокислот:
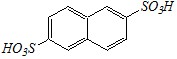
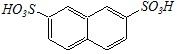
2,6-нафталиндисульфокислота 2,7-нафталиндисульфокислота
Нитрование, в отличие от сульфирования — необратимая реакция. Поэтому при мононитровании преимущественно образуется ?-нитропроизводные (1-нитронафталин), а при введении второй нитрогруппы — смесь ?, ??-динитропроизводных (1,5- и 1,8-динитронафталинов):
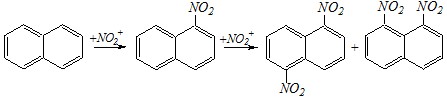
1,5-динитронафталин 1,8-динитронафталин
При этом, введение второй электрофильной частицы и при сульфировании, и при нитровании происходит во второе (незамещённое) кольцо, так как сульфо - и нитрогруппы являются сильными электроноакцепторами и тем самым дезактивируют замещённое кольцо для электрофильной атаки.
Вопрос 3. Приведите механизм превращения нафталина в 1-бромнафталин. Объясните.
Ответ. Эта реакция:
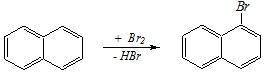
протекает без катализатора и начинается как присоединение к диеновой системе (1,4-присоединение). Однако затем следует процесс отщепления, вызванный образованием более устойчивой ?-?-сопряжённой системы:
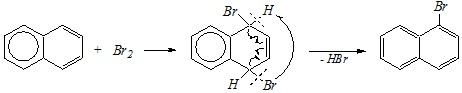
При этом, в ходе протекания этих реакций ароматичность второго кольца не нарушается, поэтому и условия должны быть аналогичными условиям присоединения к диеновым углеводородам.
Вопрос 4. В чём различие хлорирования нафталина и 1-аминонафталина?
Ответ. Хлорирование нафталина — это электрофильная реакция. Если катализатор не используется, то она начинается как электрофильное присоединение, и затем протекает отщепление (см. выше, аналогично бромированию). При использовании хлорида алюминия в качестве катализатора протекает электрофильное замещение — в любом случае продукт монохлорирования будет одним и тем же — 1-хлорнафталин. Дальнейшее хлорирование приведёт в конечном итоге к продукту исчерпывающего хлорирования — перхлорнафталину:
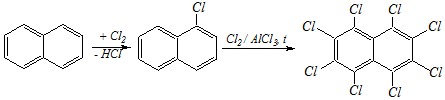
Хлорирование ?-нафтиламина сопровождается окислением и помимо обычного электрофильного замещения (путь а) протекает образование хинонов (путь b), аналогичное для аминобензолов (см. учебник, гл. 10.5.7):
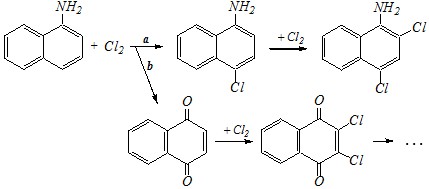
Доля продуктов окисления зависит от условий проведения реакции.
Контрольные вопросы и задачи
Назовите по заместительной номенклатуре ИЮПАК:
а) |
| б) |
|
а) нафталина, б) 1-нитронафталина, в) нафтохинона-1,4,
г) 5-метилнафтохинона-1,4. Какие продукты образуются при действии газообразного хлора на 1-аминонафталин? Приведите схемы превращения ?-нафтиламина при действии на него а) оксида хрома (VI) в присутствии кислотного катализатора, б) кислорода на ванадиевом катализаторе. Приведите механизм взаимодействия ?-нафтиламина с 1 молем концентрированной серной кислоты при нагревании и с избытком H2SO4 в тех же условиях. Приведите механизм взаимодействия ?-нафтола а) с разбавленной азотной кислотой, б) с бромной водой. Какие продукты образуются при действии на ?-нафтол в) раствора гидроксида натрия, г) хромовой смеси?
Лабораторная работа
Опыт 1. СУЛЬФИРОВАНИЕ НАФТАЛИНА
В сухую пробирку поместите 1 лопаточку нафталина. Нагрейте пробирку до расплавления нафталина. Затем дайте ей остыть и добавьте к затвердевшему нафталину 10 капель концентрированной серной кислоты (в вытяжном шкафу). Осторожно нагрейте пробирку в пламени спиртовки, постоянно встряхивая о достижения полной однородности смеси. Затем дайте смеси остыть, добавьте к ней 10 капель воды и снова слегка нагрейте. При охлаждении выделяются кристаллы ?-нафталинсульфокислоты.
Занятие 33. полициклические ароматические соединения. антрацен. фенантрен
Вопросы для подготовки к занятию
Строение антрацена и фенантрена. Ароматический и диеновый характер молекул. Реакции присоединения к молекулам антрацена и фенантрена. Радикальный и электрофильный характер реакций. Примеры присоединения водорода, галогенов, галогеноводородов. Особенности протекания реакций. Электрофильное замещение в молекулах антрацена и фенантрена. Направление реакции. Примеры реакций (нитрование, сульфирование, галогенирование). Реакции окисления антрацена и фенантрена.
Содержание занятия
Обсуждение вопросов по теме занятия. Контроль усвоения темы.Типовые обучающие вопросы и эталоны ответов на них
Вопрос 1. Приведите схемы реакций хлорирования антрацена и фенантрена. Что можно сказать о механизмах этих реакций?
Ответ. Хлор присоединяется к внутренней диеновой системе с образованием 9,10-дигидро-9,10-дихлорантрацена. Реакция идёт уже при 0°С, однако в дальнейшем отщепляется молекула хлороводорода с образованием 9-хлорантрацена.
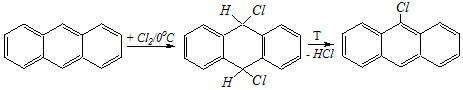
9,10-дигидро-9,10-дихлорантрацен 9-хлорантрацен
При хлорировании фенантрена образуется продукт присоединения 9,10 дихлор-9,10-дигидрофенантрен, при нагревании которого образуется 9-хлорфенантрен.
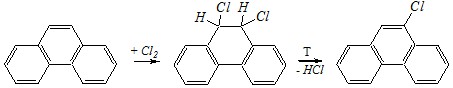
9,10 дихлор-9,10-дигидрофенантрен 9-хлорфенантрен
Присоединение может протекать по электрофильному или радикальному механизму в зависимости от условий проведения реакций.
Вопрос 2. Объясните, почему нитрование антрацена приводит исключительно к 9-нитроантрацену, а фенантрен нитруется неселективно.
Ответ. Образование 9-нитроантрацена связано с тем, что в электрофильных реакциях антрацена образующийся ?-комплекс обладает большей ароматичностью, чем исходная молекула, так как в нём можно выделить два бензольных цикла (а в антрацене только один из трёх циклов является ароматическим):
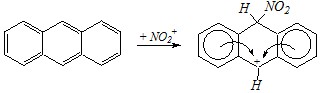
Другими словами, образование такого карбокатиона сопровождается значительным понижением энергии системы и делает его существенно выгодным. По этой причине все электрофильные агенты направляются в антрацене, прежде всего, в 9 положение. Однако именно при нитровании такой продукт будет не просто преобладающим среди прочих, а исключительным ввиду необратимости этой реакции.
Электрофильные реакции в 9 положение фенантреновой системы не сопровождаются сколько-нибудь значительным изменением ароматичности, образование ?-комплекса не является энергетически выгодным процессом. Поэтому нитрование в 9 положение хотя и является преимущественным направлением, но не исключительным: возможны реакции в 1, 2, 3 и 4 положения:
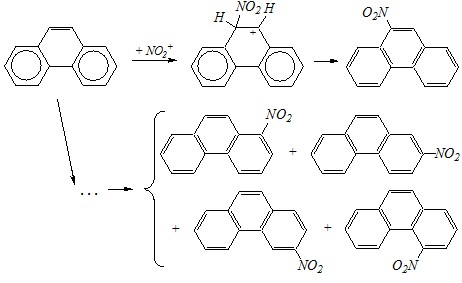
Вопрос 3. В чём проявляется различие при взаимодействии с электрофильными частицами а) антрацена и б) антрахинона-9,10?
Ответ. Антрацен легко взаимодействует с электрофилами по причине большей стабильности промежуточного ?-комплекса по сравнению с исходной молекулой (например, при нитровании — см. предыдущий вопрос), образуя 9-замещённые антрацены.
Антрахинон-9,10 можно представить системой, состоящей из двух бензольных колец, соединённых кетонными группами:
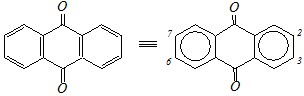
Каждая из этих карбонильных групп, как заместитель в бензольном кольце, является электроноакцептором, понижая электронную плотность в орто - и пара-положениях и затрудняя взаимодействие с электрофилами. В целом, на каждое бензольное кольцо карбонильные группы оказывают несогласованное действие, и в меньшей степени электронная плотность оказывается пониженной на 2, 3, 6, 7 атомах антрахинона-9,10 за счёт меньшего влияния акцепторного индуктивного эффекта. Поэтому взаимодействие будет возможно только с активными электрофилами (это реакции нитрования, сульфирования и хлорирования) и преимущественно во 2 положение.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 |