Вопросы для подготовки к занятию
Классификация и оптическая изомерия аминокислот. Химические свойства в сравнении со свойствами аминов и карбоновых кислот. Кислотно-осн?вные свойства аминокислот. Изоэлектрическая точка. Особенности химического поведения аминокарбоновых кислот: поведение при нагревании, образование пептидов. Важнейшие природные аминокислоты, входящие в состав белков и их значение.
Содержание занятия
1. Обсуждение вопросов по теме занятия.
2. Контроль усвоения темы.
3. Лабораторная работа.
Типовые обучающие вопросы и эталоны ответов на них
Вопрос 1. В чём различие взаимодействия лизина и аспарагиновой кислоты с избытком сильной кислоты или щёлочи? Приведите схемы превращений в ионном и молекулярном виде.
Ответ. Лизин относится к диаминомонокарбоновым кислотам, а аспарагиновая кислота — к моноаминодикарбоновым:

лизин аспарагиновая кислота
С сильными кислотами будет осуществляться протонирование по всем аминогруппам. Поэтому одна молекула лизина может провзаимодействовать с двумя молекулами одноосновной кислоты (например, HCl), а аспарагиновая — с одной молекулой
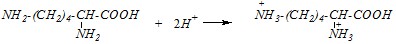
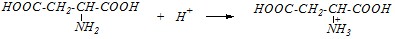
или в молекулярном виде
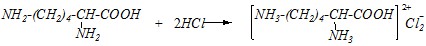
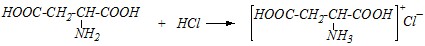
Со щелочами взаимодействие протекает по всем карбоксильным группам, а так как в молекуле лизина только одна такая функциональная группа, а в молекуле аспарагиновой кислоты — две, то лизин может провзаимодействовать только с одной молекулой однокислотной щёлочи, а аспарагиновая кислота — с двумя:
![]()
![]()
или в молекулярном виде
![]()
![]()
Вопрос 2. Каков механизм взаимодействия аминокислот с азотистой кислотой и какой практический смысл имеет эта реакция?
Ответ. Взаимодействие аминокислот с азотистой кислотой — это реакция нитрозирования первичных алифатических аминов, приводящая к образованию гидроксикислот и выделению азота.
NH2-CH(R)-COOH + HNO2 > HO-CH(R)-COOH + H2O + N2^
Реакция протекает в присутствии сильных кислот как катализаторов, происходит нитрозирование по первичной аминогруппе, поэтому механизм можно представить в следующем виде:
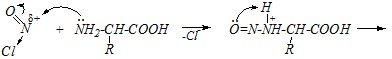
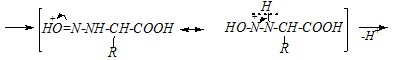
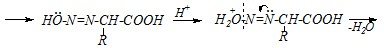
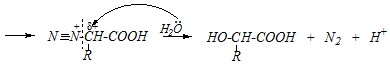
По объёму выделившегося азота можно проводить количественное определение аминокислот.
Вопрос 3. Приведите уравнение реакции взаимодействия треонина с избытком уксусным ангидридом.
Ответ. Треонин — это гидроксиаминокарбоновая кислота, то есть помимо карбоксильной и аминогрупп в молекуле имеется ещё спиртовая гидроксогруппа. За счёт этого ацилированию уксусным ангидридом может подвергаться как аминогруппа, так и гидроксогруппа. При этом за счёт большей нуклеофильности аминогруппа будет ацетилироваться в первую очередь, а затем уже реакция пойдёт по гидроксильной группе. Поэтому взаимодействие треонина с избытком уксусного ангидрида можно представить так:
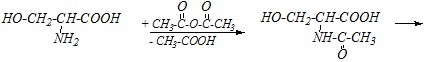
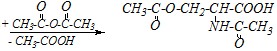
Вопрос 4. Приведите уравнение реакции взаимодействия аспарагиновой кислоты с избытком этилового спирта в присутствии кислотного катализатора.
Ответ. Аспарагиновая кислота — это аминодикарбоновая кислота, и реакция со спиртами возможна только по карбоксильным группам. Аминогруппа алкилированию спиртами не подвергается. В результате происходит образование сложноэфирных групп — реакция этерификации:
![]()
Реакционная способность карбоксильных групп в молекуле аспарагиновой кислоты между собой различается незначительно, поэтому можно считать, что этерификация протекает не селективно, а, значит, практически одновременно по обеим группам.
Лабораторная работа
Опыт 1. Реакция глицина с нингидрином
В пробирку поместите 4 капли 1%-го раствора глицина и 2 капли 0,1%-го раствора нингидрина. Содержимое пробирки осторожно нагрейте до появления сине-красной окраски. Напишите уравнение и механизм реакции взаимодействия глицина с нингидрином.
Опыт 2. Реакция глицина с формальдегидом
В пробирку поместите 5 капель 1%-го раствора глицина и добавьте 1 каплю индикатора метилового красного. Раствор окрашивается в жёлтый цвет (нейтральная среда). К полученной смеси добавьте равный объем формалина. Отметьте появление красной окраски (кислая среда). Данная реакция под названием «формольное титрование» используется для количественного определения карбоксильных групп в ?-амино-кислотах. Напишите уравнение и механизм реакции взаимодействия глицина с формальдегидом.
Контрольные вопросы и задачи
Приведите схемы превращений и механизмы реакций взаимодействия а) 2-аминопропановой кислоты, б) 2,6-диамино-гексановой кислоты, в) 2-амино-3-гидроксибутановой кислоты с 1 молем каждого из следующих реагентов: 1) гидроксид натрия (водный раствор), 2) бромметан, 3) уксусный ангидрид, 4) метанол в кислой среде. Приведите механизм взаимодействия орнитина с избытком азотистой кислоты в присутствии HCl. Предложите способ направленного получения дипептида Лиз-Сер из двух ?-аминокислот. Какие аминокислоты можно получить по методу Штреккера-Зелинского из а) пропаналя, б) бутанона-2, в) 2-метилбутаналя? Приведите схемы превращений.Занятие 18. карбоновые кислоты и их производные
Содержание занятия
1. Контрольная работа.
Вопросы для подготовки к контрольной работе
Номенклатура карбоновых кислот и их производных. Оптическая изомерия гидрокси - и аминокарбоновых кислот. Строение карбоксильной и ацильной групп. Кислотные свойства моно-, дикарбоновых кислот, непредельных кислот, замещённых (гидрокси-, оксо-, амино-) карбоновых кислот. Кислотно-осн?вные свойства аминокислот. Изоэлектрическая точка. Реакции нуклеофильного замещения в ряду карбоновых кислот и их ацильных производных, механизм, роль катализатора. Сравнение их реакционной способности. Нуклеофильное замещение в дикарбоновых кислотах и их производных. Свойства циклических ангидридов и имидов. Жиры как сложные эфиры глицерина: строение, состав. Общая характеристика карбоновых кислот, входящих в состав жиров. Фосфатиды: строение, физиологическая роль. Особенности получения и химического поведения нитрилов. Химические свойства непредельных и замещённых карбоновых кислот: свойства карбоксильной группы, непредельного фрагмента и заместителя. Реакции присоединения к непредельным монокарбоновым кислотам и реакции замещения в радикале. Реакции декарбоксилирования и декарбонилирования оксокар-боновых кислот. Поведение дикарбоновых кислот, гидроксикислот, аминокислот при нагревании. Образование пептидов из ?-аминокарбоновых кислот. Природные гидрокси-, оксокислоты и их значение. Важнейшие природные аминокислоты, входящие в состав белков и их значение. Малоновый и ацетоуксусный эфиры: строение, кето-енольная таутомерия, СН-кислотность, особенности химического поведения (нуклеофильные свойства, кислотное и кетонное расщепление). Синтезы на основе малонового и ацетоуксусного эфиров: получение моно - и дикарбоновых кислот, моно - и дикарбонильных соединений, оксокислот и других соединений.Занятие 19. Углеводы. Классификация и строение моносахаридов
Вопросы для подготовки к занятию
Углеводы, их классификация. Моносахариды: классификация, номенклатура. Проекционные формулы Фишера. Стереоизомерия моносахаридов. цикло-оксо-таутомерия. Формулы Колли-Толленса и Хеуорса. Номенклатура циклических форм. Конформации пиранозного кольца. Производные моносахаридов.
Содержание занятия
Обсуждение вопросов по теме занятия. Контроль усвоения темы.Типовые обучающие вопросы и эталоны ответов на них
Вопрос 1. Приведите для ?, D-глюкопиранозы строение её аномера.
Ответ. ?, D-Глюкопираноза — представитель гексоз. В химии моносахаридов диастереомеры, различающиеся конфигурацией только одного углеродного атома, называются эпимерами. Если речь идёт о различии в конфигурации гликозидного атома углерода, то тогда диастереомеры называются аномерами. У альдоз таким углеродным атомом является С1. Аномеры являются частным случаем эпимеров. В молекуле ?, D-глюкопиранозы атом углерода С1 имеет конфигурацию, совпадающую с конфигурацией её «концевого» хирального центра С5, т. е. атома, определяющего принадлежность к стереохимическому ряду. При различных способах написания стереохимических формул углеводородов конфигурация С1 в ?-ано-мере изображается таким образом, что полуацетальная гидроксильная группа в формуле Колли–Толленса располагается справа от линии углеродной цепи, в формуле Хеуорса—под плоскостью пиранозного цикла (если это D-стереоизомер), в конформационной формуле занимает аксиальное положение.
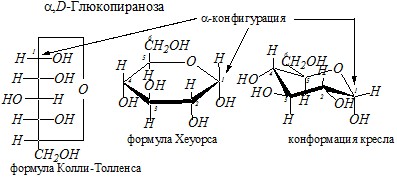
Аномером ?, D-глюкопиранозы является ?, D-глюкопираноза, отличающаяся от рассмотренного ?-аномера противоположной конфигурацией хирального атома углерода С1. Соответственно полуацетальная гидроксильная группа у ?-аномера располагается слева от линии углеродной цепи в формуле Колли–Толленса, над плоскостью пиранозного цикла — в формуле Хеуорса и занимает экваториальное положение в конформационной формуле.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 |



