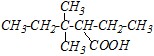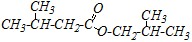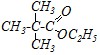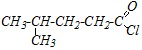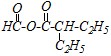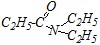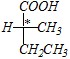Содержание занятия
1. Обсуждение вопросов по теме занятия.
2. Контроль усвоения темы.
3. Лабораторная работа.
Типовые обучающие вопросы и эталоны ответов на них
Вопрос 1. Дайте названия для следующих двух соединений по заместительной номенклатуре:
1) | 2) |
Приведите также для них другие возможные названия.
Ответ. В молекуле первого соединения присутствует единственная функциональная группа - СООН, поэтому родоначальная структура должна обязательно включать атом углерода карбоксильной группы, и нумерация углеродной цепи должна начинаться с этого атома углерода.
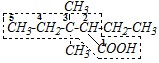
Основа названия составляется как производное соответствующего углеводорода — пентана — с добавлением суффикса с окончанием - овая и слова «кислота». Полное название будет включать перечисление заместителей, не попавших в родоначальную структуру, в виде приставок по алфавиту с указанием локантов: 3,3-диметил-2-этилпентановая кислота. Среди других возможных названий — это название по рациональной номенклатуре: данная карбоновая килота рассматривается как замещённая уксусная — этил-трет-амилуксусная кислота; и полутривиальное название: как замещённая валериановая кислота — ?-этил-?, ?-диметилвалериановая кислота.
Второе соединение представляет собой сложный эфир. Поэтому для названия по заместительной номенклатуре необходимо к названию углеводородного радикала спиртового остатка добавить название ацилата кислоты. Этот эфир является производным изобутилового спирта и изовалериановой (3-метилбутановой) кислоты. Поэтому его название будет изобутил-3-метилбутаноат. Среди других названий — это полутривиальные названия изобутил-изовалерат, изовалериано-изобутило-вый эфир, изобутиловый эфир изовалериановой кислоты и название по рациональной номенклатуре изобутиловый эфир ?-метилмасляной кислоты.
Вопрос 2. Сравните кислотные свойства этановой кислоты, этанамида и этанамина.
Ответ. Этановая кислота, этанамид и этанамин представляют собой производные одного углеводорода — этана:
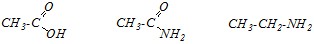
Молекулы этановой кислоты, этанамида и этанамина содержат разные функциональные группы, причём в первом соединении кислотным центром является атом кислорода, а во втором и третьем веществе – атом азота. В молекуле этановой кислоты на атом кислорода, являющийся кислотным центром, оказывает сильное электроноакцепторное влияние карбонильный фрагмент >C=O, увеличивающий полярность связи О–Н в гидроксильной группе за счёт р-?-сопряжения и уменьшающий эффективный отрицательный заряд на кислотном центре:
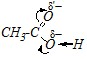
Аналогично в молекуле этанамида на атом азота, являющийся кислотным центром, оказывает сильное электроноакцепторное влияние карбонильный фрагмент >C=O. В результате увеличивается полярность связи N–Н за счёт р-?-сопряжения и уменьшается эффективный отрицательный заряд на кислотном центре:
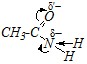
Всё это способствует отрыву протона и проявлению этим соединением более сильных кислотных свойств, чем этанамином, в молекуле которого отсутствует р-?-сопряжение:
![]()
Поэтому кислотные свойства у этанамина в меньшей степени выражены, чем у этановой кислоты и этанамида.
Однако в молекуле этанамида по сравнению с этановой кислотой кислотным центром является менее электроотрицательный атом азота, поэтому полярность связи N–H меньше, чем О–H, и эффективный заряд на атоме азота, являющемся кислотным центром, также меньше, чем на атоме кислорода в этановой кислоте.
Таким образом, кислотность этанамида меньше, чем этановой кислоты, и весь ряд уменьшения кислотных свойств можно представить следующим образом:
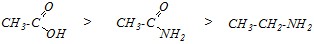
Вопрос 3. Чем отличаются условия и механизм реакций образования сложного эфира при взаимодействии спирта с а) этаноилхлоридом, б) этановой кислотой и в) этанамидом?
Ответ. Наиболее реакционноспособными ацильными производными карбоновых кислот по отношению к нуклеофилам являются галогенангидриды. Их представителем из числа перечисленных в задании является этаноилхлорид. Высокая реакционная способность галогенангидридов объясняется преобладанием акцепторного индуктивного эффекта атома галогена над донорным мезомерным (и, как следствие, бо?льшим положительным зарядом на карбонильном атоме углерода, являющимся реакционным центром) и стабильностью галогенид-иона, являющимся анионом уходящей группы. Нуклеофильное замещение в ряду галогенангидридов протекает достаточно быстро при обычных условиях. Механизм реакции здесь может быть SN1 или SN2.
SN1-механизм:
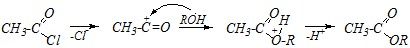
SN2-механизм:
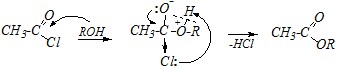
Реакционная способность карбоновых кислот при взаимодействии со спиртами ниже, чем ацилгалогенидов, а амидов – ещё ниже. Поэтому реакция образования сложного эфира из этановой кислоты или этанамида протекает медленнее и только в присутствии кислотного катализатора:
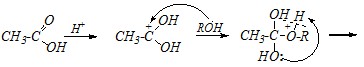
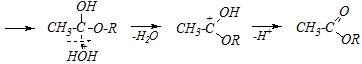
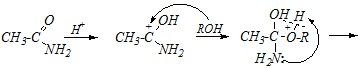
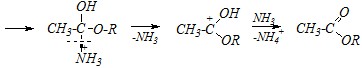
Причина низкой реакционной способности карбоновых кислот и их амидов заключается в донорном эффекте гидроксильной и амино-групп, что стабилизирует промежуточный карбокатион и затрудняет нуклеофильную атаку. Для активирования таких субстратов, как карбоновые кислоты и, особенно, амиды, реакцию проводят обычно при нагревании.
Вопрос 4. Каковы механизмы превращения 2-метилбутаноата аммония а) при нагревании; б) при взаимодействии с ацетилхлоридом?
Ответ. 2-Метилбутаноат аммония — соль слабой кислоты и слабого основания. Поэтому в равновесии с ионной формой вещества существует и молекулярная:
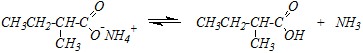
Образующиеся аммиак и карбоновая кислота вступают друг с другом в реакцию нуклеофильного замещения. Нагревание приводит к увеличению нуклеофильной активности аммиака и ускорению реакции распада ионного соединения.
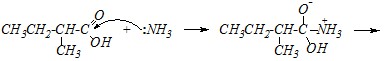
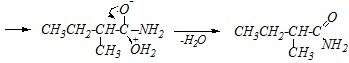
Ацетилхлорид — высокоактивное по отношению к нуклеофилам ацильное производное уксусной кислоты. Его взаимодействие с солью другой карбоновой кислоты приведёт к нуклеофильному замещению, в котором роль нуклеофила будет играть 2-метилбутаноат-анион:
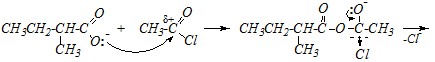
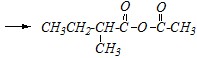
Продуктом реакции является смешанный ангидрид уксусной и ?-метилмасляной кислот — этаноил-2-метилбутаноат.
Контрольные вопросы и задачи
Приведите все возможные названия для данных соединений:
Какие общие свойства спиртов и карбоновых кислот можно отметить? Приведите примеры. Поясните. Как будет протекать взаимодействие 2,2-диметилпропановой кислоты с хлором на свету; с пентахлоридом фосфора; с пропанолом-2 в кислой среде; при нагревании с пентаоксидом дифосфора? Приведите механизмы реакций. Как следует проводить реакцию, чтобы переэтерифицировать метиловый эфир карбоновой кислоты в бутиловый и наоборот? Приведите механизм реакции взаимодействия 2,2-диметил-бутаноилхлорида с метанолом; с избытком аммиака. Почему при пиролизе кальциевых и влажных натриевых солей карбоновых кислот образуются разные продукты? Сравните механизмы реакций.
Лабораторная работа
Открытие уксусной кислоты
В пробирку поместите по 3 капли уксусной кислоты и воды. К раствору добавьте 2–3 капли 10%-го раствора гидроксида натрия до полной нейтрализации уксусной кислоты. После этого добавьте 2–3 капли 1%-го раствора FeCl3. Появляется жёлто-красное окрашивание ацетата железа (III).
Подогрейте раствор до кипения. Выделяется красно-бурый осадок нерастворимого в воде гидроксида диацетата железа (III) (CH3COO)2FeOH. Раствор над осадком становится бесцветным.
Занятие 14. дикарбоновые и непредельные кислоты и их производные
Вопросы для подготовки к занятию
Номенклатура и строение непредельных кислот. Реакции присоединения к непредельным монокарбоновым кислотам и реакции замещения в радикале. Общая характеристика высших непредельных карбоновых кислот, входящих в состав жиров.
Номенклатура дикарбоновых кислот и их производных; особенности их химического поведения: кислотные свойства, нуклеофильное замещение в ацильных группах, поведение при нагревании. Свойства циклических ангидридов и имидов.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 |