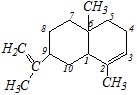
В названии сначала перечисляются заместители с помощью приставок, затем слово «бицикло», и в квадратных скобках указывается число атомов углерода в каждом цикле между узловыми (общими для двух циклов) атомами (в порядке уменьшения). После этого пишется название углеводорода, соответствующего общему числу атомов в бициклической системе. Двойная связь указывается при помощи суффикса «ен». Полное название — 2,6-диметил-9-пропен-2?-илбицикло[4,4,0]децен-2.
В молекуле бициклического альдегида миртеналя сначала нумеруется больший цикл так, чтобы альдегидная группа получила меньший номер. Затем нумеруются другие атомы между узловыми в бициклической системе. Здесь меньший номер получает атом с заместителями.
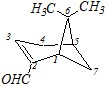
Полное название составляется аналогично предыдущему примеру: 6,6-диметилбицикло[3,1,1]гептен-2-аль-2 .
Вопрос 2. Какая конформация цис-1,4-диметилциклогексана является чрезвычайно энергетически невыгодной? В виде каких конформеров должно существовать это соединение?
Ответ. Крайне невыгодной должна быть конформация циклогексана в виде «ванны» с аксиальным расположением обоих цис-метильных группировок у 1 и 4 углеродных атомов кольца.
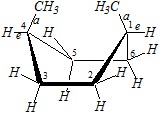
Эта конформация является одной из заслонённых форм, и данный конформер обладает наиболее высокой энергией за счёт взаимного отталкивания пространственно сближенных заместителей по сравнению, например, с конформацией «ванна», имеющей экваториальное расположение заместителей.
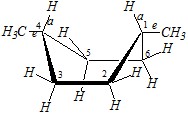
Данное соединение должно существовать в виде конформера «кресло», так как именно для такого конформационного изомера должен наблюдаться минимум энергии:
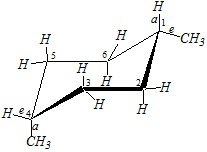
Вопрос 3. Как будут взаимодействовать а) метилциклопропан и
б) циклопентен с разбавленной соляной кислотой? Каковы механизмы этих реакций?
Ответ. Метилциклопропан является соединением, содержащим малый цикл, характеризующийся высокой энергией напряжения
(115 кДж/моль). Для таких соединений характерны реакции присоединения с раскрытием кольца. В частности под действием соляной кислоты будет происходить электрофильная атака катиона водорода по ?-связям с последующим гетеролитическим разрывом и образованием наиболее устойчивого карбокатиона (из возможных):
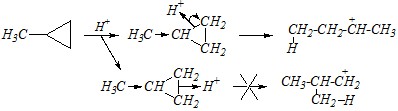
Образовавшийся карбокатион взаимодействует затем с хлорид-ионами или с молекулами воды (если кислота очень разбавленная):
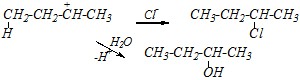
Циклопентен является соединением, содержащим нормальный цикл. Такие циклы устойчивы к раскрытию. Поэтому для циклопентена будут характерны реакции, аналогичные алифатическим углеводородам. В частности, так как в молекуле циклопентена имеется двойная связь, то это, прежде всего, реакции присоединения по двойной связи (как для алкенов) с сохранением углеродного скелета:
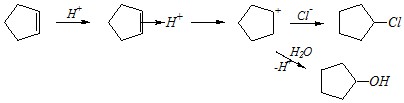
Вопрос 4. Как будут происходить взаимодействие циклобутана с водородом при нагревании на платиновом катализаторе и с хлором при нагревании на свету?
Ответ. В молекуле циклобутана угловое напряжение существенно меньше, чем в циклопропане: валентный угол составляет 88° (но и в плоском циклобутане он был бы почти таким же — 90°). Поэтому реакции раскрытия цикла для него не протекают ни под действием галогенов, ни под действием галогеноводородов; четырёхчленное кольцо разрушается только гидрированием на платине при значительном нагревании
![]() .
.
А взаимодействие с хлором при нагревании на свету приведёт к радикальному замещению водорода, аналогично алканам:
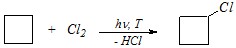
Контрольные вопросы и задачи
Приведите наиболее стабильные конформации соединений:
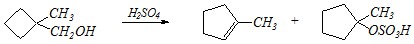
а) цис-1,2-диметилциклогексан, б) транс-1,2-диметилцикло-гексан, в) транс-1,3-диметилциклогексан, г) транс-1,4-диметил-циклогексан. Приведите механизмы реакций взаимодействия метилциклопропана со следующими веществами: а) с водородом на никелевом катализаторе, б) с бромом, в) с бромоводородом. Какие соединения будут реагировать с бромоводородом: а) этилциклопропан, б) метилциклобутан, в) 1-метилциклобутен, г) циклогексан, д) циклопентен? Приведите механизмы возможных реакций. Приведите механизм следующего превращения:
Лабораторная работа
Опыт 1. Доказательство непредельности терпенов
В пробирку поместите 2 капли бромной воды и 1 каплю скипидара, встряхните. Отметьте изменения, происходящие в пробирке. Напишите схему и приведите механизм взаимодействия ?-пинена (составная часть скипидара) с бромной водой.
Опыт 2. Окисляемость терпенов
В пробирку поместите 1 каплю 2% раствора перманганата калия и 5 капель воды, добавьте 1 каплю скипидара и встряхните. Отметьте изменения, происходящие в пробирке. Напишите схему взаимодействия ?-пинена с перманганатом калия в нейтральной среде.
Занятие 24. бензол. арены
Вопросы для подготовки к занятию
Строение молекулы бензола. Ароматичность. Механизм реакций электрофильного замещения. Особенности и закономерности реакций нитрования, сульфирования, галогенирования, алкилирования и ацилирования. Механизм образования электрофильных частиц, роль катализаторов. Реакции присоединения, изомеризации и окисления бензола.
Номенклатура, изомерия аренов. Строение аренов. Химические свойства аренов: реакции электрофильного замещения, реакции боковых цепей, дегидрирование, окисление.
Содержание занятия
1. Обсуждение вопросов по теме занятия.
2. Контроль усвоения темы.
Типовые обучающие вопросы и эталоны ответов на них
Вопрос 1. Сравните условия и селективность реакции нитрования бензола и толуола.
Ответ. Реакция нитрования бензола по схеме
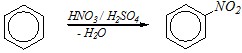
протекает при использовании смеси концентрированных азотной и серной кислот при температуре 50–60°С в течение 40–50 мин. В результате образуется только нитробензол; дальнейшее нитрование с образованием м-динитробензола в этих условиях практически не протекает по причине низкой реакционной способности нитробензола в реакциях SE.
Нитрование толуола протекает легче, чем бензола. Эту реакцию проводят обычно при более низкой температуре (25–30°С) и/или за более короткий промежуток времени. При этом мононитрование приводит к образованию смеси трёх изомерных продуктов, в которой преобладают о - и п-изомеры. Это объясняется распределением электронной плотности в ароматическом кольце под влиянием +М-эффекта метильной группы.
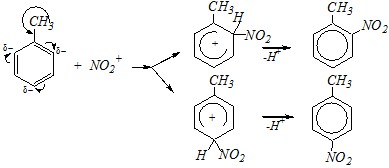
Вопрос 2. Сравните влияние метильной и втор-изоамильной групп как заместителей в бензольном кольце на скорость и направление реакций электрофильного замещения.
Ответ. В молекуле метилбензола, как и в молекуле втор-изоамилбензола
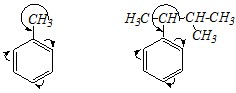
алкильный заместитель оказывает суммарный электронодонорный (+М и +I) эффект на бензольное кольцо. Однако вклад мезомерного эффекта (?-?-сопряжение) в общий электронный эффект значительно больше индуктивного, поэтому необходимо сравнивать воздействие алкильных групп только за счёт ?-?-сопряжения. В метильной группе три С–Н-связи могут находиться в сопряжении с
?-электронным секстетом бензольного кольца, а у ?-углеродного атома в молекуле втор-изоамилбензола имеется только одна
С–Н-связь, поэтому и в сопряжении с ?-электронным секстетом кольца может участвовать только одна С–Н-связь. Таким образом, электронодонорный эффект метильной группы оказывается больше, чем втор-изоамильной (эффект Натана–Бейкера).
Метильная и втор-изоамильная группы являются о-п-ориен-тантами в бензольном кольце по отношению к вступающему электрофилу. Однако необходимо иметь в виду, что о - и п-ориентация определяет лишь преимущественное направление реакции электрофильного замещения в алкилбензолах, то есть замещение идёт в эти положения бензольного кольца преобладающим образом, но не исключительно. Обычно образуется смесь всех трёх изомеров (орто-, мета-, пара-), но они находятся в разных соотношениях. У втор-изоамильного радикала сила о-п-ориентирующего влияния ослабевает по сравнению с метильным радикалом, то есть доля о - и п-изомеров несколько уменьшается, но увеличивается относительное количество продукта м-замещения. Кроме того, по пространственным причинам в молекуле втор-изоамилбензола о-положение экранировано заместителем (значительно бoльшим по размерам, чем в молекуле метилбензола). Поэтому преимущественное направление электрофильного замещения в молекуле втор-изоамилбензола — в п-положение, а в молекуле метилбензола — в о - и п-положения с преобладанием продукта о-замещения (за счёт того, что в молекуле два орто-положения и только одно пара-положение).
Вопрос 3. Чем отличаются реакции бромирования этилбензола, проведённые в темноте в присутствии FeBr3 и на свету в отсутствие даже следов железа?
Ответ. Бромид железа (III) является типичной кислотой Льюиса. Молекулы брома, взаимодействуя с FeBr3, образуют электрофильные частицы, которыми могут быть либо катионы Br+, либо комплексы Br+[FeBr4]? в зависимости от растворителя:

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 |



