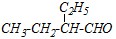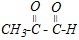Ответ. Винилхлорид и аллилхлорид — непредельные галогенопроизводные, сильно отличающиеся своей активностью в реакциях нуклеофильного замещения галогена.
В винилхлориде благодаря (+М)-эффекту возникает частичная двоесвязанность галогена с углеродом.
![]()
Поэтому винилхлорид будет инертен к нуклеофильным реагентам в обычных условиях, и при его взаимодействии с йодоводородной кислотой возможно лишь электрофильное присоединение по двойной углерод-углеродной связи. Электрофилом является катион Н+.
CH2=CH-Cl + H+I? > CH3-CHICl
Так как аммиак не проявляет электрофильных свойств, а может быть только нуклеофилом, то взаимодействие его с винилхлоридом протекать не будет.
Для аллилхлорида, напротив, легко протекают реакции нуклеофильного замещения (особенно легко в протонных высокополярных растворителях, когда возможна диссоциация субстрата) за счёт образования устойчивого карбокатиона:
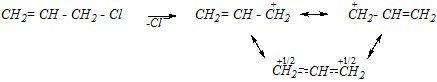
Поэтому аллилхлорид будет легко вступать в реакции нуклеофильного замещения галогена с йодоводородом и аммиаком:
CH2=CH-CH2-Cl + H+I? > CH2=CH-CH2-I
CH2=CH-CH2-Cl + 2NH3 > CH2=CH-CH2-NH2 + NH4Cl.
С избытком йодоводорода затем возможна и реакция присоединения по двойной связи.
Вопрос 2. Какое соединение образуется при взаимодействии винилбромида с водой в кислой среде?
Ответ. Винилгалогениды несколько более реакционноспособны по отношению к электрофилам, чем этилен, и при этом наблюдается чёткая ориентация в электрофильном присоединении. Протон присоединяется согласно распределению электронной плотности:
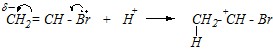
Дальнейшее присоединение молекулы воды приводит к образованию бромзамещённого спирта, характеризующегося повышенной кислотностью и легко отщепляющего молекулу бромоводорода.
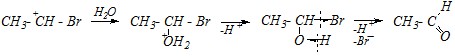
Продуктом реакции является карбонильное соединение (уксусный альдегид).
Вопрос 3. Почему не существует виниловый спирт (не удаётся выделить его в чистом виде), но известны его простые и сложные эфиры?
Ответ. Виниловый спирт CH2=CH-OH, как и все спирты такого типа, по правилу Эльтекова–Эрленмейера изомеризуется в карбонильное соединение. Причина этого — в повышенной кислотности данного спирта по сравнению с насыщенными спиртами, что можно объяснить как распределением электронной плотности в самой молекуле спирта, так и стабильностью алкоголят-аниона за счёт
р-?-сопряжения:
![]()
При присоединении протона к атому углерода образуется связь
С–Н. А СН-кислоты значительно менее сильные, менее способны к диссоциации, чем ОН-кислоты, которые образуются при протонировании атома кислорода в еноле. Константы кислотности этих двух реакционых центров различаются на 5–8 порядков, и поэтому такие соединения, в том числе и виниловый спирт, существуют преимущественно в карбонильной форме.
Эфиры винилового спирта (простые и сложные) не содержат подвижного атома водорода, и в обычных условиях они не перегруппировываются в производные карбонильных соединений, например, винилэтиловый эфир и винилацетат.

винилэтиловый эфир винилацетат
Вопрос 4. В чём причины высокой основности аллилового спирта?
Ответ. Проявление осн?вных свойств для спиртов — это способность к взаимодействию с протоном и/или способность к отщеплению гидроксид-иона. Для аллилового спирта (и спиртов этого типа) отщепление гидроксогруппы в виде аниона легко объясняется устойчивостью образующегося карбокатиона: аллильный катион стабилизирован р-?-сопряжением. Протонирование же способствует диссоциации молекулы аллилового спирта.
![]()
Таким образом, аллиловый спирт должен обладать повышенной способностью к протонированию, так как этот процесс приводит к образованию устойчивого катиона.
Контрольные вопросы и задачи
Приведите SN1 и SN2-механизмы реакций взаимодействия каждого из соединений: а) 4-метил-1-хлорпентена-2, б) 3-бром-2-метил-пропена-1, в) 3-метилбутен-2-ола-1 — со следующими реагентами: 1) с аммиаком, 2) с йодоводородной кислотой, 3) с водой. Приведите AE-механизм реакции взаимодействия 2-бром-пропена-1 и 3-метил-1-хлорбутена-1 со следующими реагентами: 1) с водой, 2) с бромоводородной кислотой, 3) с бромной водой, 4) с метанолом в присутствии кислотного катализатора. Чем отличается взаимодействие с галогеноводородными кислотами 3-бром-2-метилпропена-1 и 1-бром-2-метилпропена-1? По каким механизмам протекает взаимодействие каждого из бромалкенов с галогеноводородными кислотами? Приведите SR-механизм реакции хлорирования каждого из соединений: а) 4-метил-1-хлорпентена-1, б) 4-метил-1-хлор-пентена-2, в) 3-бром-2-метилпропена-1, г) 3-метил-1-хлор-пентена-1. Укажите условия проведения этой реакции.
Занятие 11. алифатические альдегиды и кетоны
Вопросы для подготовки к занятию
Классификация оксосоединений. Строение оксогруппы. Реакции нуклеофильного присоединения, механизм, роль катализатора. Сравнение реакционной способности оксогруппы альдегидов и кетонов. Реакции замещения в углеводородном радикале. Реакции окисления и восстановления. Особенности окисления кетонов. Полимеризация карбонильных соединений.
Содержание занятия
1. Обсуждение вопросов по теме занятия.
2. Контроль усвоения темы.
3. Лабораторная работа.
Типовые обучающие вопросы и эталоны ответов на них
Вопрос 1. Дайте все возможные названия:
Ответ. Первое вещество является насыщенным алифатическим альдегидом, для названия которого применяются заместительная и рациональная номенклатуры. По заместительной номенклатуре должна быть выбрана родоначальная структура, включающая атом углерода альдегидной группы, при этом нумерация начинается с альдегидной группы:
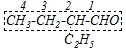
К названию углеводорода из четырёх атомов углерода добавляется суффикс - аль. Заместитель «этил» присутствует в названии в качестве приставки. Таким образом, название этого соединения по заместительной номенклатуре: 2-этилбутаналь. По рациональной номенклатуре любой альдегид может быть назван как замещённый уксусный. Для этого выделим в структуре данного альдегида фрагмент уксусного
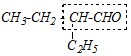 ,
,
который связан с двумя этильными радикалами. Поэтому полное название альдегида по рациональной номенклатуре — диэтилуксусный альдегид.
Молекула второго соединения содержит альдегидную и кетонную группы. Назвать его можно только по заместительной номенклатуре. При этом старшей функциональной группой из них является альдегидная, и для её названия используется суффикс - аль. Название кетонной группа в присутствии альдегидной образуется путём добавления приставки оксо-. Нумерацию углеродных атомов в соединении определяет старшая (альдегидная) группа.
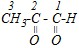
Таким образом, название соединения 2-оксопропаналь.
Вопрос 2. В чём различие механизма взаимодействия ацетона с метанолом в кислой, щелочной и нейтральной среде? Приведите образование соответствующего полуацеталя и ацеталя.
Ответ. Взаимодействие карбонильных соединений со спиртами — это реакция нуклеофильного присоединения, в которой нуклеофилом является молекула спирта или алкоголят-ион, в зависимости от среды. В нейтральной среде с ацетоном взаимодействуют молекулы воды по схеме:
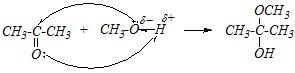
Образовавшееся производное кетона, относящееся к полуацеталям (или, правильнее, к полукеталям), может дальше взаимодействовать со второй молекулой метанола. Но это уже реакция нуклеофильного замещения гидроксогруппы в замещённых спиртах; при этом получаются полные ацетали (кетали):
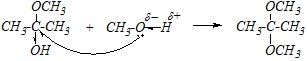
В кислой среде нуклеофилом является также молекула спирта, однако реакция протекает легче, так как происходит первичное (быстрое и обратимое) протонирование молекулы субстрата (ацетона) с образованием карбокатиона, реакционная способность которого по отношению к нуклеофилам значительно выше, чем нейтральных молекул.
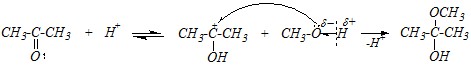
И дальнейшее превращение в ацеталь (кеталь) в кислой среде протекает легче:
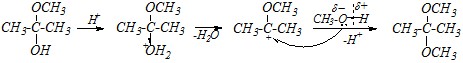
В щелочной среде взаимодействие кетонов со спиртами также протекает легче, чем в нейтральной среде, но за счёт того, что нуклеофильной частицей здесь будет алкоголят-анион. Однако в данном случае образуется только полуацеталь (полукеталь). Дальнейшее нуклеофильное замещение не происходит, по-видимому, потому, что щелочная среда не способствует протеканию реакций по SN1-механизму.
![]()
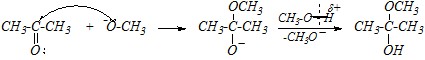
Вопрос 3. В чём различие реакций окисления альдегидов и кетонов? Поясните на примере ацетальдегида и гексанона-3.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 |