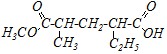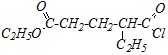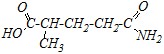Содержание занятия
1. Обсуждение вопросов по теме занятия.
2. Контроль усвоения темы.
3. Лабораторная работа.
Типовые обучающие вопросы и эталоны ответов на них
Вопрос 1. По какому направлению преимущественно будут протекать реакции радикального замещения в а) кротоновой и б) пентен-3-овой кислоте?
Ответ. Кротоновая, или бутен-2-овая, и пентен-3-овая кислоты — это непредельные карбоновые кислоты:
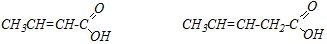
кротоновая кислота пентен-3-овая кислота,
причём кротоновая кислота относится к ?, ?-ненасыщенным, то есть в её молекуле имеется ?-?-сопряжённый фрагмент, включающий углерод-углеродную ?-связь и ?-связь карбонильной группы. В молекуле пентен-3-овой кислоты ?-связи разделены насыщенным атомом углерода, и сопряжения между ними нет.
Реакции радикального замещения, инициируемые светом или высокой температурой, обычно протекают через образование наиболее стабильного из возможных углеводородного радикала. Типичным примером может служить реакция хлорирования. В случае кротоновой кислоты реакция идёт по четвёртому атому углерода; при этом образуется радикал, в котором р-орбиталь с неспаренным электроном включается в цепь имеющегося сопряжения и удлиняет её:
![]()
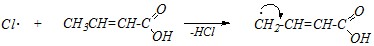
Такой радикал будет очень стабильным, что можно подтвердить также граничными структурами:
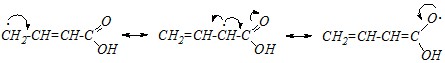
В молекуле пентен-3-овой кислоты имеется два насыщенных атома углерода (второй и пятый), однако только радикальная атака по пятому атому углерода приведёт к образованию стабильного промежуточного радикала с длинной цепью ?-р-?-сопряжения:
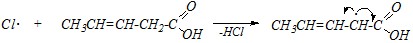
Превращение промежуточных углеводородных радикалов, образованных из кротоновой и пентен-3-овой кислот, протекает аналогично другим реакциям радикального хлорирования:
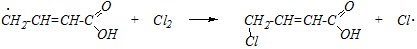
4-хлорбутен-2-овая кислота
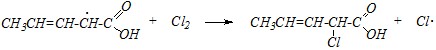
2-хлорпентен-3-овая кислота
Вопрос 2. Дайте название по заместительной номенклатуре следующим соединениям:
1) |
| 2) |
|
3) |
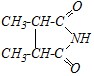
| 4) |
|
Ответ. 1) Дикарбоновые кислоты образуют два ряда сложных эфиров: нейтральные и кислые. Первое соединение относится к кислым эфирам. Кислые эфиры называются аналогично эфирам монокарбоновых кислот — к названию алкильного остатка спирта добавляется название аниона кислоты (ацилата), но наличие атома водорода в одной из карбоксильных групп обозначается приставкой гидро-, помещаемой после названия спиртового остатка. Заместители в углеводородной цепи обозначают приставками, указывая локантами их положение и перечисляя в алфавитном порядке. Нумерация углеводородной цепи проводится с учётом старшинства функциональных групп. Название: Метилгидро-4-метил-2-этилпентандиоат.
2) Второе соединение как функциональное производное дикарбоновой кислоты — это неполный галогенангидрид, содержащий ещё сложноэфирную группу, которая в названии имеет приоритет перед галогенокарбонильной. Поэтому для обозначения последней используется приставка галогенокарбонил. В данном случае хлоркарбонильная группа находится у четвертого атома углеводородной цепи остатка гексановой кислоты. Поэтому название: Этил-4-хлоркарбонилгексаноат.
3) Третье вещество относится к неполным амидам, причём карбоксильная группа имеет приоритет в названии. В таком случае амидная группа обозначается приставкой аминокарбонил - (или карбамоил - — как ацильного остатка карбаминовой кислоты NH2-COOH) с указанием её положения в углеродной цепи. Все приставки перечисляются в алфавитном порядке с указанием их положения локантами. Название: 4-Аминокарбонил-2-метилбутановая кислота или 4-Карбамоил-2-метилбутановая кислота.
4) Названия имидов образуют от соответствующих карбоновых кислот путём замены словосочетания - карбоновая кислота на - кар-боксимид. Двумя локантами указывают положение в углеродной цепи двухвалентного заместителя –CO-NH-CO–. Название: 2,3-Бу-танкарбоксимид.
Вопрос 3. Каков механизм взаимодействия янтарного ангидрида с избытком этанола в кислой среде?
Ответ. Янтарный ангидрид, как ацильное производное дикарбоновой кислоты, образует со спиртами сложные эфиры, причём с избытком этанола продукт реакции будет содержать две сложноэфирные группы:
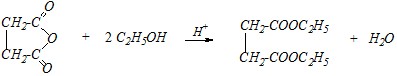
Механизм всей реакции в целом включает нуклеофильное замещение сначала в ангидридной группе, а затем, при участии второй молекулы этанола, — в карбоксильной группе:
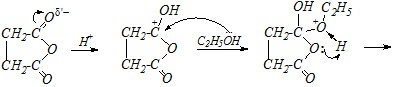
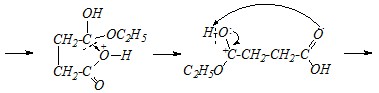
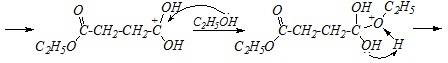
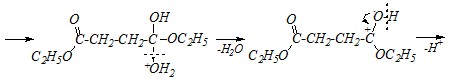
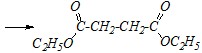
Вопрос 4. Какие продукты образуются при взаимодействии гидрооксалата натрия с избытком концентрированной серной кислоты при нагревании. Приведите схемы превращений.
Ответ. Первая стадия взаимодействия гидрооксалата натрия с серной кислотой — это обменная реакция с образованием щавелевой кислоты:
НООС-CООNa + Н2SO4 > НООС-CООН + NaНSО4
Дальнейшее нагревание приводит к декарбоксилированию щавелевой кислоты и превращению её в муравьиную кислоту:
НООС-CООН ![]() НСООН + СО2 ,
НСООН + СО2 ,
а муравьиная кислота при нагревании с концентрированной серной дегидратируется с образованием монооксида углерода:
HCOOН ![]() CO + Н2О.
CO + Н2О.
Поэтому суммарное уравнение превращения гидрооксалата натрия при нагревании с серной кислотой будет:
НООС-CООNa + Н2SO4 ![]() NaНSО4 + СО2 + СО + Н2О
NaНSО4 + СО2 + СО + Н2О
Контрольные вопросы и задачи
Приведите возможные превращения гидросукцината аммония при нагревании. Приведите механизм реакции взаимодействия янтарного ангидрида с этиламином (при мольном соотношении реагентов 1:1). Приведите механизм реакции полного гидролиза малонилдихлорида. Приведите механизм реакции взаимодействия диэтилоксалата с избытком разбавленной соляной кислоты.
Лабораторная работа
Опыт 1. Открытие щавелевой кислоты
в виде кальциевой соли
В пробирку поместите лопаточку щавелевой кислоты и прибавьте 4–5 капель воды до полного растворения. Пипеткой возьмите одну каплю раствора и нанесите на предметное стекло. Добавьте к ней 1 каплю раствора хлорида кальция. Выпадает кристаллический осадок.
Напишите схему реакции образования оксалата кальция.
С кристаллами оксалата кальция можно встретиться при клиническом исследовании мочи. Они имеют форму почтовых конвертов и хорошо видны под микроскопом.
Опыт 2. Окисление олеиновой кислоты раствором перманганата калия
В пробирку поместите 2 капли олеиновой кислоты, добавьте 2 капли 5%-го раствора Na2CO3 и 2 капли 2%-го раствора KMnO4. Встряхните пробирку несколько раз. Отметьте, какие изменения происходят с первоначальной фиолетовой окраской раствора.
Занятие 15. Гидроксикарбоновые кислоты. Оксокарбоновые кислоты
Вопросы для подготовки к занятию
Классификация и оптическая изомерия гидроксикислот. Химические свойства в сравнении со свойствами спиртов и карбоновых кислот. Особенности химического поведения гидроксикарбоновых кислот: кислотные свойства, поведение при нагревании. Классификация и номенклатура оксокислот. Химические свойства в сравнении со свойствами альдегидов, кетонов и карбоновых кислот. Особенности химического поведения оксокарбоновых кислот: кислотные свойства, поведение при нагревании, реакции декарбоксилирования и декарбонилирования. Природные гидроксикислоты и оксокислоты, их значение.
Содержание занятия
1. Обсуждение вопросов по теме занятия.
2. Контроль усвоения темы.
Типовые обучающие вопросы и эталоны ответов на них
Вопрос 1. Как будет взаимодействовать яблочная кислота с избытком водного раствора щёлочи. Дайте название продукту реакции.
Ответ. Яблочная кислота является двухосновной трёхатомной кислотой, т. е. содержит две карбоксильные группы и одну спиртовую гидроксогруппу. Со щелочами протекают обменные реакции только по карбоксильным группам с образованием солей. Спиртовые гидроксильные группы в реакции со щелочами не вступают. Поэтому для полной нейтрализации 1 моль яблочной кислоты потребуется 2 моль щелочи:
![]()
2-гидроксибутандиоат натрия,
оксисукцинат натрия,

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 |