Методические рекомендации предназначены для студентов медико-биохимических и фармацевтических специальностей медицинских вузов. Могут быть полезны также и студентам химических специальностей других вузов и факультетов.
© , 2008
© Северный государственный
медицинский университет, 2008
Весь изучаемый материал по органической химии распределён по главам, соответствующим тематике лабораторно-практических и семинарских занятий, а также занятиям по органическому синтезу. Основой для изучения органической химии служат учебники и учебные пособия, приведённые в списке литературы, и лекции по органической химии, читаемые на данном факультете.
лабораторно-практические
и семинарские занятия
Занятие 1. Классификация органических веществ. Электронные эффекты заместителей
Вопросы для подготовки к занятию
Состав органических веществ. Основные органогены. Классификация органических соединений. Важнейшие функциональные группы. Структурная изомерия. Гибридизация атомных орбиталей на примере различных валентных состояний атома углерода. Основные характеристики ковалентной связи (энергия, длина, полярность, поляризуемость): ?-, ?-, ?-связи. Электронные эффекты заместителей. Различные типы сопряжённых систем.
Содержание занятия
1. Обсуждение вопросов по теме занятия.
2. Контроль усвоения темы.
Типовые обучающие вопросы и эталоны ответов на них
Вопрос 1. Какие атомы или атомные группировки обладают положительным, а какие – отрицательным индуктивным эффектом:
-F, - Br, - CН2СH2F, -+NH3, - OC2H5, - К, - СаBr, - CH2CH2CH3 ?
Ответ. Положительным индуктивным эффектом (+I-эффектом) обладают атомы и атомные группировки, менее электроотрицательные по сравнению с атомом углерода, а также алкильные группы (насыщенные углеводородные заместители). Среди перечисленных такими являются атом калия К, группировка, в которой первый атом — атом кальция - СаBr, и заместитель - CH2CH2CH3.
Отрицательным индуктивным эффектом (–I-эффектом) обладают атомы и атомные группировки, более электроотрицательные по сравнению с атомом углерода. Сюда относятся случаи, когда первый атом в группировке заместителя – это атом более электроотрицательного элемента: - F, - Br, - OC2H5, а также углеводородные заместители, содержащие электроотрицательные атомы: - CН2СH2F. Положительный заряд на одном из атомов заместителя резко увеличивает его электроотрицательность, поэтому аммонийная группа - NH3+ обладает наибольшим (по модулю) –I-эффектом.
Вопрос 2. Что такое сопряжение и в каких случаях оно возникает?
Ответ. Сопряжением называется явление образования единой
?-электронной системы в молекуле, свободном радикале или ионе путём бокового перекрывания негибридных p-орбиталей трёх или более соседних атомов, оси симметрии которых параллельны. Следовательно, оно характерно для соединений, содержащих негибридные p-орбитали в непрерывной цепи атомов. (Возможно также сверхсопряжение, в котором могут участвовать p-орбитали только одного или двух атомов углерода). В зависимости от природы перекрывающихся орбиталей различают два основных вида сопряжения: ?-? - и р-?-сопряжения. В первом случае — это перекрывание двух (или нескольких) ?-связей, разделённых ординарной связью, например, в бутадиене-1,3 или акролеине. Во втором случае — это перекрывание орбитали ?-связи с вакантной p-орбиталью соседнего с ней атома или с p-орбиталью с неподелённой парой электронов или с неспаренным электроном.
Вопрос 3. Какие электронные эффекты проявляет аминогруппа в каждом из следующих соединений: CH3–CH=CH-NH2 (I) и CH2=CH-CH2-NH2 (II)?
Ответ. В молекуле пропенил-1-амина (I) CH3–CH=CH-NH2 аминогруппа обладает отрицательным индуктивным эффектом, так как азот более электроотрицателен по сравнению с атомом углерода. Однако мезомерный эффект, проявляемый этой функциональной группой, будет донорный, т. е. положительный за счёт того, что рz-орбиталь с неподелённой парой электронов азота может участвовать в сопряжении с орбиталями ?-связи (р-?-сопряжение). Схематично это можно показать следующим образом:
![]() –I, +М.
–I, +М.
В молекуле аллиламина (II) CH2=CH-CH2-NH2 возможно только проявление индуктивного эффекта аминогруппой по отношению к углеводородной части молекулы. Сопряжение, подобное тому, что наблюдается в соединении (I), здесь невозможно поскольку аминогруппа и атомы углерода, участвующие в образовании ?-связи, разделены насыщенным атомом углерода (подчёркнуто):
![]() –I.
–I.
Контрольные вопросы и задачи
Какие атомы или атомные группировки обладают положительным, а какие — отрицательным индуктивным эффектом:
1) - CH2F, 2) - Li, 3) - NH2, 4) - CHF2, 5) - CF3, 6) - I, 7) - Si(CH3)3,
8) - CH3, 9) - Na, 10) - CH2OH, 11) - CCl3, 12) - SH, 13) - NO2,
14) - PH3+, 15) - MgBr, 16) - NO2, 17) - CHCl2, 18) - CF3, 19) - Cl,
20) - BH3, 21) - CH=O, 22) - OH, 23) -C2H5, 24) - CdCl, 25) - CH2Cl, 26) - CH2CH2CH2CH3 ? Какие атомы или атомные группировки могут проявлять положительный, а какие — отрицательным мезомерный эффект:
1) - F, 2) - CH=O, 3) - NH2, 4) - OCH3, 5) - COOH, 6) - COCl, 7) - NO2, 8) - Br, 9) - CH=CH-Cl, 10) - O-CH=O?
Занятие 2. Стереоизомерия
Вопросы для подготовки к занятию
Пространственное строение органических соединений. Понятие о пространственной изомерии. Оптическая изомерия. Хиральность молекул. Проекционные формулы Э. Фишера. Абсолютная и относительная конфигурации. Стереохимическая номенклатура Кана-Ингольда-Прелога (R-, S-номенклатура). Понятие об D-, L-стереохимических рядах. Геометрическая изомерия (относительно плоскости двойной связи и плоскости цикла). Конформации органических молекул. Факторы, влияющие на стабилизацию предпочтительной конформации. Проекционные формулы Ньюмена. Конформации бутана, циклогексана, 2-хлорэтанола.
Содержание занятия
1. Обсуждение вопросов по теме занятия.
2. Контроль усвоения темы.
Типовые обучающие вопросы и эталоны ответов на них
Вопрос 1. Какие атомы углерода являются хиральными центрами в следующих структурах: а) СН3-СНCl-СН2Cl, б) СН3-СНF-СНCl-СН3?
Ответ. Хиральным центром может быть асимметрический атом, находящийся в центре тетраэдра (в данном случае это sp3-гибридизованный атом углерода). Асимметрический атом должен образовывать ?-связи с четырьмя разными атомными группировками.
Первая из перечисленных структур (а) СН3-СНCl-СН2Cl имеет в своём составе только один такой атом углерода. Этот атом находится в середине углеродной цепи:
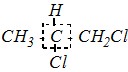
Два других углеродных атома имеют в своём окружении одинаковые группы. (В данном случае каждый из них связан с двумя или тремя атомами водорода.)
Вторая из перечисленных структур (б) СН3-СНF-СНCl-СН3 имеет в своём составе два атома углерода, образующие ?-связи с четырьмя разными атомными группировками:
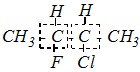
Таким образом, в первом случае (а) имеется один хиральный центр, ответственный за наличие оптических изомеров, а во втором случае (б) — два хиральных центра.
Вопрос 2. Изобразите при помощи формул Фишера оптические изомеры с общей структурной формулой СН3-СНCl-СН2-СН3. Определите абсолютную конфигурацию одного из них.
Ответ. Находим в структурной формуле асимметрический атом углерода, являющийся хиральным центром. Это второй атом в углеродной цепи:
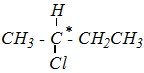
В проекционных формулах Фишера углеродная цепь должна располагаться вертикально. В данном случае нет принципиальной разницы, какая из атомных группировок (-СН3 или - СН2СН3) будет изображена вверху, а какая — внизу. Два других (неуглеродных) атома у хирального центра располагаются в формуле Фишера слева и справа от него. Химический символ асимметрического атома углерода не изображается. Тогда проекционные формулы двух оптических изомеров будут отличаться расположением неуглеродных атомов относительно хирального центра:
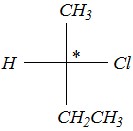
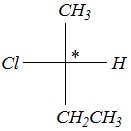
Для определения абсолютной конфигурации одного из этих изомеров (например, первого) представим схему получения проекционной формулы Фишера из пространственной формулы. В пространстве горизонтальные связи хирального центра С–Н и C–Cl расположены на переднем плане, а углеродная цепь — на заднем плане от асимметрического атома углерода:
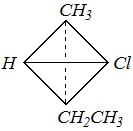
Полученный тетраэдр необходимо повернуть так, чтобы самая младшая группа (по Кану-Инголду-Прелогу) оказалась наиболее удалённой от наблюдателя. Самая младшая здесь — это атом водорода. В результате получим:
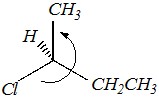
Тогда остальные группы располагаются по старшинству в указанном изогнутой стрелкой порядке. Получается движение против часовой стрелки. Это соответствует S-изомеру.
Вопрос 3. При помощи формул Ньюмена изобразите конформеры вещества
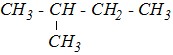
относительно связи С2–С3 . Какие из них являются заслонёнными, а какие — заторможенными?
Ответ. Для того, чтобы изобразить конформеры относительно данной углерод-углеродной связи, представим пространственное расположение групп у атомов углерода при данной связи и затем поместим наблюдателя слева так, чтобы один из атомов углерода этой связи заслонял другой.
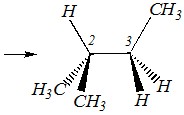
Получим изображение, в котором оба атома углерода (и связь между ними) спроецируются в точку, а три оставшиеся связи каждого из этих атомов углерода будут располагаться под углами 120° друг к другу. При этом ближайший к наблюдателю атом углерода обозначается точкой, а удалённый – окружностью. Связи этих атомов в проекционной формуле проводятся соответственно из точки и от окружности:

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 |



