В5 (вариант 148) Дифракционная решетка, имеющая 100 штрихов на 1 мм, расположена параллельно экрану на расстоянии 2,5 м от него и освещается нормально падающим пучком света длиной волны 600 нм. Определите расстояние между вторыми дифракционными максимумами справа и слева от центрального (нулевого). Ответ выразите в сантиметрах (см). Считать sin a » tg a.
Сначала запишем данные условия задачи.
N=100, ℓ=1 мм =10-3 м, S=2,5 м, l=600 нм = 6×10-7 м, k=2
О2О’2 — ?
Условие для максимумов дифракции дифракционной решетки в случае нормального падения лучей света ![]() , где
, где ![]() – порядок дифракционной картины. В случае нормального падения света на решетку, максимумы соответствующих положительных и отрицательных порядков расположены симметрично от центрального (нулевого) порядка (точка О’ на экране Э). Таким образом, необходимо определить расстояние О2О’2, которое и соответствует расстоянию между положительным порядком +2 (в точке О2) и –2 (в точке О’2). Данное расстояние легко определить из прямоугольного треугольника ОО2О’2.
– порядок дифракционной картины. В случае нормального падения света на решетку, максимумы соответствующих положительных и отрицательных порядков расположены симметрично от центрального (нулевого) порядка (точка О’ на экране Э). Таким образом, необходимо определить расстояние О2О’2, которое и соответствует расстоянию между положительным порядком +2 (в точке О2) и –2 (в точке О’2). Данное расстояние легко определить из прямоугольного треугольника ОО2О’2.
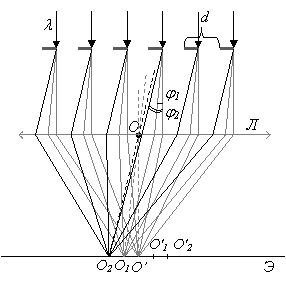 Лучи, проходя сквозь дифракционную решетку, за счет явления дифракции отклоняются от прямолинейного распространения, заходя в область геометрической тени. Для максимумов первого порядка они отклоняются от первоначального направления на угол j1. А для второго – на угол j2 в обе стороны. В целях упрощения рисунка эти направления выделены только влево. Так как для каждого из порядков имеем дело с параллельным пучком света, то лучше всего эти лучи сфокусировать на экране с помощью линзы Л.
Лучи, проходя сквозь дифракционную решетку, за счет явления дифракции отклоняются от прямолинейного распространения, заходя в область геометрической тени. Для максимумов первого порядка они отклоняются от первоначального направления на угол j1. А для второго – на угол j2 в обе стороны. В целях упрощения рисунка эти направления выделены только влево. Так как для каждого из порядков имеем дело с параллельным пучком света, то лучше всего эти лучи сфокусировать на экране с помощью линзы Л.
Для правильного геометрического построения воспользуемся вспомогательным лучом (побочной оптической осью) ОО2, проходящим через центр линзы параллельно лучам, идущим под углом j2. Точка пересечения этого луча с фокальной плоскостью линзы, где установлен экран, есть точка О2 – точка, в которой сойдутся все лучи, распространяющиеся до линзы под углом j2. Таким образом, из построения делаем вывод, что угол j2 равен углу О2ОО’ прямоугольного треугольника с соответствующими обозначениями.
Необходимо найти катет О2О’, так как искомое расстояние между вторыми дифракционными максимумами равно этому удвоенному расстоянию О2О’2=2 О2О’. Из условия задачи расстояние от решетки до экрана равно S. Если решетка расположена практически вплотную к линзе, то это расстояние можно принять за ОО’. Из определения тангенса угла
![]() или
или ![]() .
.
Примем во внимание, что sin a » tg a для малых углов. Значит,
![]() .
.
Значение этого синуса можно подставить в основную формулу для дифракционной решетки ![]() ,
,
![]() , или
, или ![]() .
.
Остается определить период d решетки
![]() .
.
Теперь можно выразить из последних двух формул расстояние О2О’
![]() .
.
Окончательно получаем О2О’2=2 О2О’ или
О2О’2=2 ![]() .
.
Подставим численные значения ![]() .
. ![]() .
.
Теперь рассмотрим последнюю часть и задание С5, имеющее наименьшую решаемость. Это задание комбинированное, на знание законов электромагнетизма (сила Ампера) и механического момента сил. Само по себе подобное сочетание уже представляет трудность. Но особая трудность – момент сил, который проходят в курсе средней школы в 7 классе при изучении правила рычага. В старших классах эта тема больше не затрагивается и решение задач на упомянутую тему, как правило, не практикуется. Еще одно важное замечание заключается в том, что по определению сила Ампера действует на элемент тока (бесконечно малый элемент). А это означает, что при решении данной задачи, где присутствует три участка проводника с током, расположенных под разными углами к вектору магнитной индукции ![]() , необходимо применять интегрирование для каждого участка. Проверка этого задания показала, что выпускники школ или не приступали к решению этого задания (в большинстве случаев), или пытались при решении применить равенство сил Ампера и силы тяжести. Что абсолютно недопустимо при вращательном движении! Здесь необходимо говорить только о равенстве моментов.
, необходимо применять интегрирование для каждого участка. Проверка этого задания показала, что выпускники школ или не приступали к решению этого задания (в большинстве случаев), или пытались при решении применить равенство сил Ампера и силы тяжести. Что абсолютно недопустимо при вращательном движении! Здесь необходимо говорить только о равенстве моментов.
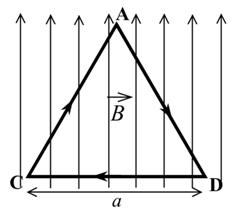
С5 (вариант 133) На непроводящей горизонтальной поверхности стола лежит проводящая жёсткая рамка из однородной тонкой проволоки, согнутой в виде равностороннего треугольника ADC со стороной, равной а (см. рисунок). Рамка, по которой течет ток I, находится в однородном горизонтальном магнитном поле, вектор индукции которого ![]() перпендикулярен стороне CD. Каким должен быть модуль индукции магнитного поля, чтобы рамка начала поворачиваться вокруг стороны CD, если масса рамки m?
перпендикулярен стороне CD. Каким должен быть модуль индукции магнитного поля, чтобы рамка начала поворачиваться вокруг стороны CD, если масса рамки m?
Ниже предлагается решение из критериев к этому варианту.
Образец возможного решения
По рамке течет ток ![]() . Пусть модуль вектора магнитной индукции равен
. Пусть модуль вектора магнитной индукции равен ![]() . На стороны рамки действует сила Ампера.
. На стороны рамки действует сила Ампера.
На сторону AD: ![]() , где
, где ![]() ;
;
На сторону AC: ![]() ;
;
На сторону CD: ![]() .
.
Суммарный момент этих сил относительно оси CD:
![]() .
.
Момент силы тяжести: ![]() . Условия отрыва:
. Условия отрыва: ![]() ,
, ![]() . Отсюда
. Отсюда ![]() . Допускается ответ в виде равенства.
. Допускается ответ в виде равенства.
Как видно из приведенного короткого образца решения, школьникам необходимо было продемонстрировать не только знания по физике – знание основных законов и их применение, но также и знания по алгебре и геометрии. А именно, знание тригонометрических формул приведения и умение вычислять плечо каждой из найденных сил, согласно приведенному чертежу. Конечно, в данном решении не представлено даже направление силы Ампера, которая, согласно школьному определению, находится по «правилу левой руки». В нашем случае на проводники AC и AD действующие силы Ампера направлены из плоскости чертежа, а сила Ампера, действующая на CD – за плоскость. Относительно оси, проходящей через эту же сторону, момент этой силы равен нулю. Как и равен нулю момент силы тяжести проводника CD относительно этой же оси. Поэтому в решении и используются только моменты сил Ампера, действующих на AC и AD и моменты сил тяжести этих же проводников, направленных за плоскость чертежа. А чтобы рамка была повернута относительно стороны CD, необходимо условие, при котором суммарный момент сил Ампера со стороны AC и AD был больше или равен суммарному моменту сил тяжести, действующих на эти же стороны.
Увы, именно это стало камнем преткновения для подавляющего большинства выпускников. Значит, при проведении подготовки к выпускным экзаменам, преподавателям необходимо должным образом обратить внимание на эти вопросы.
К сожалению, не на высоте оказались и решения комбинированных заданий на применение законов сохранения импульса и Ньютона. Речь идет о задании С2.
Рассмотрим одно из таких заданий, которое имеет самую наименьшую решаемость.
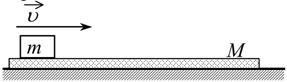 С2 (вариант 194) На гладкой горизонтальной плоскости находится длинная доска массой М= 2 кг. По доске скользит шайба массой т = 0,5 кг. Коэффициент трения между шайбой и доской m = 0,2. В начальный момент времени скорость шайбы равна
С2 (вариант 194) На гладкой горизонтальной плоскости находится длинная доска массой М= 2 кг. По доске скользит шайба массой т = 0,5 кг. Коэффициент трения между шайбой и доской m = 0,2. В начальный момент времени скорость шайбы равна ![]() а доска покоится. В момент t = 0,8 с шайба перестает скользить по доске. Чему равна начальная скорость шайбы
а доска покоится. В момент t = 0,8 с шайба перестает скользить по доске. Чему равна начальная скорость шайбы ![]() ?
?
Ниже предлагается один из возможных вариантов решения по предлагаемым критериям.
Образец возможного решения
1. Внешние силы, действующие на систему тел «доска – шайба», направлены по вертикали и в сумме равны нулю. Импульс системы тел «доска – шайба» относительно Земли сохраняется:
![]()
где u – скорость шайбы и доски после того, как шайба перестала скользить по доске.
2. Сила трения, действующая на доску со стороны шайбы, постоянна
![]()
Под действием этой силы доска движется с ускорением
![]()
и достигает скорости u за время
![]()
Отсюда
![]()
Ответ: ![]()
Меньше всего в этой задаче были сделаны ошибки в записи закона сохранения импульса. Можно с уверенностью утверждать, что в большинстве своем школьниками эта тема усваивается неплохо. Самое большое затруднение вызвало определение ускорения доски. Много выпускников, приступавших к решению этого задания, определили ускорение шайбы, что совершенно делать не нужно. Отсюда – непонимание физического процесса и, как следствие, неверное решение задачи. Здесь важно правильно выбрать систему отсчета. Школьниками предлагались варианты решения, связанные с выбором системы отсчета «доска». Некоторым удалось правильно довести до логического завершения свои решения, за что им были выставлены максимальные первичные баллы.
Выводы по анализу решаемости заданий повышенного
(часть «В») и высокого (часть «С») уровней сложности
Необходимо отметить, что содержание всех задач частей «В» и «С», включенных в варианты ЕГЭ в последние годы, соответствуют программе школьного курса физики и отражают все разделы этого курса. Тем самым, это позволяет проверить усвоение всех разделов физики участниками ЕГЭ при решении задач повышенного и высокого уровней.
Выше было отмечено, что задание на применение момента сил при вращении рамки с током, немного выбивается из требований школьной программы, но оно позволило тем самым выявить наиболее способных учащихся.
Подводя итоги анализа решаемости задач повышенного и высокого уровней сложности, отметим, что
а) средняя решаемость заданий части «B» школьного этапа ЕГЭ в 2009 г. составила 39,08%, в 2008 г. составила 39,65 %. В 2007 г. – 39,47 %, что несколько выше, чем в 2006 г. – 35,90 %.
Это практически стабильный показатель за последние годы.
б) средняя решаемость заданий части «С» школьного этапа ЕГЭ в 2009 г. составила 15,37%, в 2008 г. составила 21,32 %, в 2007 г. – 18,16 %, что также несколько выше, чем в 2006 г. – 14,69 %.
К сожалению, это не высокий показатель решаемости. Даже, несмотря на то, что физику по-прежнему выбирают только те учащиеся, которые мотивированы на поступление в высшие учебные заведения на технические специальности, их общая подготовка по предмету всё же невысока. Это отмечают и преподаватели вузов, которые ведут занятия на первом и втором курсах по предмету «Общая физика». Им приходится достаточно много проводить дополнительных занятий и консультаций, чтобы преодолеть разрыв по данному предмету между знаниями, полученными в школе, и знаниями, требуемыми по стандарту для студентов.
Впервые во всех вариантах был соблюден принцип равнотрудности заданий. То есть, в каждом варианте задание с одинаковым номером соответствовало одной теме и, более того, одному типу задания. Единственное, что немного выбивалось из этого определения, так это задания С5 на вращение рамки с током в магнитном поле. Задачи с квадратной рамкой оказались более решаемы, нежели задачи с треугольной рамкой. Многих подвело элементарное незнание или неумение применять тригонометрические формулы. И, кстати, в последнее время неумение применять математические преобразования при решении задач по физике является краеугольным камнем для учащихся.
Заключение
Подводя итоги прошедшего этапа ЕГЭ по физике, необходимо отметить, что впервые все варианты отличались одинаковым подбором заданий. Учащиеся находились практически в одинаковых условиях, а это немаловажный фактор при оценивании знаний выпускников.
Облегчением при решении оказалось и то, что некоторые задания повторялись практически полностью или приближенно из материалов предыдущих лет. Учителями школ проделана работа по подготовке учащихся по предшествующим заданиям и это не могло не сказаться на лучших результатах.
Однако остается проблема, когда учащиеся практически неплохо справляются с базовыми заданиями, но никак не решают повышенный и высокий уровень заданий. И таких учащихся много. Это наводит на мысль, что нормального понимания законов физики у таких выпускников нет. Репродуктивный способ мышления, заложенный в базовый уровень, является преобладающим у таких учащихся. А элементарного творческого подхода к решению не присутствует. Небольшое количество часов, ставшее всеобщей тенденцией в среднем образовании, привело к потере интереса к физике со стороны учащихся и, как следствие, к ее плохому пониманию.
Еще нужно отметить и тот факт, что учителя, заинтересованные в более высоких результатах своих учеников, с введением ЕГЭ были вынуждены повышать свою квалификацию по курсу физики. И это не может не радовать. Но еще остаются и те, кому это не под силу ввиду различных причин.
Успех нашего образования во многом зависит от того, насколько глубоко школьные преподаватели владеют своим собственным предметом, так как именно они являются основным звеном передачи знаний ученикам. Чем выше знания предоставляют учителя своим учащимся, тем выше становятся и их знания, а это напрямую определяет и результаты ЕГЭ по физике.
Анализ результатов ЕГЭ – 2009 по химии в Томской области
Председатель ПК ГЭК ЕГЭ по химии в Томской области
Введение
В 2009 г. единый государственный экзамен вышел на качественно новый уровень, так как эксперимент закончился и все учащиеся средних образовательных заведений сдавали экзамены по обязательным предметам (математике и русскому языку) только в форме ЕГЭ. Химия являлась предметом по выбору, необходимость сдачи экзамена по которому, определялась нацеленностью учащегося на поступление в высшее учебное заведение на специальность химического профиля. В Томске, одном из немногих в России вузовском городе, такие специальности есть в пяти высших учебных заведениях: государственном университете, политехническом, медицинском и педагогическом университетах, а также в Северской технологической академии. Химию в качестве экзамена, сдаваемого в форме ЕГЭ, выбрали 489 учеников, из них явилось на экзамен в июне в 2009 г. 393 человека. Столь малочисленное участие школьников в сдаче ЕГЭ по химии может быть объяснено двумя объективными причинами. Во-первых, в Томске разрешено проведение олимпиады по химии, которая является альтернативой ЕГЭ, и, во-вторых, это связано с все более очевидной тенденцией преимущественного выбора учащимися гуманитарного направления образования. В пользу последнего утверждения говорят цифры: в 2009 году физику в Томской области сдавали 1950 человек, а естествознание - в два раза больше - 3413. Особенно остро вырисовывается проблема школьного химического образования. В связи с сокращением числа часов, отводимых на изучение химии, учащиеся не могут получить полноценных знаний и все меньше выбирают данный предмет в качестве экзамена по выбору для поступления на профильные специальности: химические и химико-технологические (не медико-биологические).
Технология проверки результатов ЕГЭ осталась неизменной, для проверки выполнения заданий части С билетов ЕГЭ была создана экспертная комиссия из 15 человек, в состав которой вошли как школьные учителя, так и преподаватели высших учебных заведений. Анализ работы комиссии показал, что в целом достигнуты неплохие результаты, всего 17 работ из 393 вышло на третью проверку, что свидетельствует об объективности, адекватности и равноценности выработанных подходов всеми экспертами.
Характеристика контрольно-измерительных материалов
ЕГЭ по химии в 2009 году
Согласно Порядку проведения единого государственного экзамена (Приказ Министерства образования и науки Российской Федерации от 01.01.01 г. N 57) целью ЕГЭ является обеспечение объективной оценки качества подготовки лиц, освоивших образовательные программы среднего (полного) общего образования, с использованием заданий стандартизированной формы.
При проведении ЕГЭ по химии используется система контрольных измерительных материалов (КИМ), в состав которой вошли:
1) кодификатор контролируемых элементов содержания,
2) спецификация экзаменационной работы,
3) демонстрационный вариант КИМ;
4) единые по структуре и содержанию варианты экзаменационной работы;
Формирование всех элементов системы КИМ осуществляется на основе нормативных документов для общеобразовательных учреждений, реализующих программы среднего (полного) общего образования.
Кроме того, при формировании системы КИМ учитывался существующий в практике преподавания химии опыт оценки учебных достижений обучаемых в рамках различных форм контроля знаний и реально достигаемый в условиях массовой школы уровень подготовки выпускников по химии.
Контрольные измерительные материалы призваны обеспечить возможность проанализировать, насколько выпускники, участники ЕГЭ по химии, достигли уровня обученности, предусмотренного требованиями стандарта к общеобразовательной подготовке по данному предмету.
В этой связи при разработке контрольных измерительных материалов для единого государственного экзамена по химии большое внимание уделяется способам оценки усвоения каждым экзаменующимся системы знаний, включенной в обязательный минимум содержания образования.
Данная система представляет собой совокупность элементов знаний о веществе, химической реакции, методах познания и применения веществ и реакций и рассматривается как инвариантное ядро содержания всех действующих программ по химии для общеобразовательных учреждений. Уровни усвоения этих знаний определяются нормативными требованиями к подготовке выпускников.
В нормативных документах отмечено, что по итогам обучения химии участники ЕГЭ по химии должны уметь:
− характеризовать общие свойства химических элементов и их соединений на основе положения в периодической системе ; состав, свойства и применение веществ; факторы, влияющие на изменение скорости химической реакции и состояние химического равновесия;
− объяснять закономерности в изменении свойств веществ, сущность химических реакций;
− составлять формулы веществ, схемы строения атомов, уравнения химических реакций различных типов;
− называть и определять вещества, их свойства, признаки классификации веществ, типы реакций и др.;
− проводить вычисления по химическим формулам и уравнениям;
− использовать приобретенные знания для объяснения химических явлений, происходящих в природе, быту и на производстве; для распознавания важнейших веществ, безопасной работы с веществами и т. д.
Представление о содержательной основе экзаменационной работы ЕГЭ дает Кодификатор элементов содержания по учебному предмету для составления контрольных измерительных материалов ЕГЭ, который включает максимально возможное число проверяемых элементов учебного материала (элементов содержания) – 56.
За все годы эксперимента, предшествовавшего введению единого государственного экзамена в штатный режим (2002 – 2008 г. г.), проводилась целенаправленная работа по корректировке кодификатора как одного из важнейших составляющих системы КИМ. Так, в кодификаторе были:
детализированы позиции, проверяющие усвоение таких важнейших разделов, как свойства основных классов неорганических и органических соединений;
введены позиции, проверяющие усвоение существа генетической взаимосвязи между классами неорганических веществ, знание качественных реакций на ионы и функциональные группы;
укрупнены излишне детализированные элементы содержания.
С учетом Федерального компонента государственного стандарта общего образования по химии, отдельные содержательные блоки кодификатора были дополнены новыми элементами содержания:
так раздел I - «Химический элемент» дополнен позицией «Основное и возбужденное состояние атомов»;
в раздел II «Вещество» внесены позиции - «Характеристики ковалентной связи», «Гомологический ряд углеводородов, структурная и пространственная изомерия», «Мыла», «Моносахариды, дисахариды и полисахариды»;
в разделе IV уточнена позиция «Познание и применение веществ и химических реакций», которая в новой редакции звучит следующим образом: «Правила работы в лаборатории. Лабораторная посуда и оборудование. Правила безопасности при работе с едкими, горючими и токсичными веществами, средствами бытовой химии».
Тем самым была обеспечена возможность дальнейшего приближения контрольных измерительных материалов к тому содержанию, которое является основным объектом изучения на уроках химии, а также обеспечена возможность классификации самих проверочных заданий по ведущим разделам и темам курса, по проверяемым элементам содержания; уровням сложности (базовый, повышенный, высокий); видам учебной деятельности.
Контрольные измерительные материалы призваны обеспечить дифференциацию выпускников по уровню их общеобразовательной подготовки по химии. Этим целям служит экзаменационная работа комплексного характера в разумных пределах сочетающая в себе элементы теста и традиционной письменной экзаменационной работы.
Структура экзаменационной работы ЕГЭ была определена в самом начале эксперимента и оставалась неизменной. В ней присутствуют три части, по которым распределяются задания: часть 1 – задания с выбором ответа (базового уровня сложности); часть 2 – задания с кратким ответом (повышенного уровня сложности); часть 3 – здания с развернутым ответом (высокого уровня сложности).
Общее число заданий в работах разных лет составило:
в 2002 году – 60 заданий (45 – базового, 10 – повышенного и 5 – высокого уровней сложности);
в 2003 – 2005 годах – 50 заданий (35 – базового, 10 – повышенного и 5 – высокого уровней сложности);
в 2006 – 2008 годах – 45 заданий (30 – базового, 10 – повышенного и 5 – высокого уровней сложности).
Как видно, уменьшение общего числа заданий с 60 до 45 в экзаменационных работах разных лет осуществлено за счет заданий базового уровня сложности. Преимущественно это задания репродуктивного характера с большой нагрузкой на память. В практике проведения ЕГЭ данная структура работы признана целесообразной, поскольку она дает экономию во времени. Тем самым экзаменуемые могут уделить больше внимания заданиям повышенного и высокого уровней сложности.
Другие изменения, которые произошли в экзаменационной работе ЕГЭ, коснулись содержательной основы и системы оценивания отдельных заданий.
Так, в части 1 работы наряду с традиционными заданиями базового уровня получила распространение новая форма заданий – «на два суждения». Их выполнение предполагает иную последовательность действий по выбору правильного ответа, чем в случае традиционных заданий: на первом этапе следует оценить правильность каждого из суждений и затем с учетом этого выбрать ответ. Использование таких заданий обеспечило большую вариативность выбора элементов содержания, усвоение которых должно проверяться на базовом уровне.
Определенные изменения претерпели также задания частей 2 и 3 работы. Прежде всего это задания С2, согласно условию которых требовалось написать уравнения реакций, соответствующих заданной последовательности превращения веществ – так называемой «цепочке превращений». Начиная с 2006 года в КИМ на этой позиции стали использоваться задания, при выполнении которых требуется написать уравнения четырёх возможных реакций между предложенными веществами. Это означает, что в условии таких заданий отсутствует жестко заданная схема действий, поэтому выпускники могут творчески подойти к выполнению задания и тем самым проявить более высокий уровень познания свойств веществ различных классов. Кроме того, важно отметить, что подобные задания являясь своеобразным «мысленным экспериментом», существенно усиливают практикоориентированную направленность КИМ по химии.
В 2007 году заметную корректировку претерпели задания части 2 – «на установление соответствия», ориентированные на проверку усвоения элемента содержания «электролиз расплавов и растворов солей». В предыдущие годы при выполнении таких заданий требовалось установить соответствие между формулой вещества и продуктами электролиза его водного раствора на инертных электродах. Результаты экзамена показали, что эти задания вызвали большие затруднения у экзаменуемых, поскольку по уровню своей сложности они больше напоминали задания части 3. В работе 2007 года усвоение данного элемента содержания проверялось заданиями уже в значительной степени облегченными: требовалось установить соответствие между формулой вещества и продуктом, который образуется в результате электролиза его водного раствора только на одном электроде (аноде или катоде). Таким образом, уровень сложности этих заданий был приведен в соответствие с требованиями стандарта к усвоению сложного по сути своей элемента содержания. Эта тенденция была в последующем сохранена.
Описанные и подобные им изменения содержательной основы заданий обусловили изменение системы их оценивания. В 2006 году была введена новая шкала оценивания большинства заданий (8 из 10) части 2. Это задания В1 – В5 – «на установление соответствия позиций, представленных в двух перечнях», и задания В6 – В8 «на выбор нескольких правильных ответов из предложенного списка (множественный выбор)».
По прежней шкале выполнение этих заданий оценивалось 1 баллом. Согласно новой шкале за полный правильный ответ экзаменуемый получает 2 балла, за неполный правильный ответ – 1 балл, за неверный – 0 баллов. Такое изменение системы оценивания заданий В1 – В8 повысило их вклад в общую оценку экзаменационной работы и дало определенные преимущества более подготовленным выпускникам.
Изменилась также система оценивания заданий части 3: С1 (с 5 до 3 баллов); С2 (с 5 до 4 баллов); С4 (с 5 до 4 баллов); С5 (с 5 до 3 баллов). Этим было обеспечено соответствие разработанных критериев оценки ответов экзаменуемых уровню требований к усвоению соответствующего понятия, а также тем действиям, которые необходимо осуществить при выполнении задания.
Все изменения в экзаменационных работах г. г., явились следствием совершенствования КИМ в свете требований государственного стандарта общего образования по химии и на основе результатов ЕГЭ.
В 2008 г. была проведена корректировка содержательной основы ряда заданий, в первую очередь тех, которые в работах предыдущих лет отличались определенной новизной. Так, например, была пересмотрена содержательная основа заданий «на два суждения». В 2008 году они впервые были использованы для проверки усвоения таких элементов содержания, как «Общие способы получения металлов. Общие научные принципы химического производства. Природные источники углеводородов, их переработка.». Общее число таких заданий в КИМ 2008 года было увеличено. Оно составило от 3 до 4 заданий на вариант.
Структура и содержание экзаменационной работы 2009 года не изменились. Ориентация содержания КИМ на Федеральный компонент государственного стандарта общего образования 2004 года была усилена. Так, в кодификаторе элементов содержания для составления КИМ ЕГЭ 2009 года проведены отдельные структурные и содержательные преобразования с целью достижения более полного соответствия содержания КИМ требованиям стандарта (базового и профильного уровней) к общеобразовательной подготовке выпускников средней школы по химии. В основном это касается элементов содержания блока «Вещество» (элементы органической химии) и блока «Познание и применение веществ и химических реакций» (расчетные задачи).
В спецификации экзаменационной работы 2009 года отмечено следующее:
· В части 1 использованы три разновидности заданий базового уровня сложности, предусматривающие различную последовательность действий по выбору правильного ответа. В результате экзаменуемые смогут продемонстрировать более широкий круг умений по применению знаний уже на базовом уровне.
· Продолжена работа по уточнению системы оценивания заданий части 3. в частности, шкала оценивания задания С5 изменена с 3 до 2 баллов. Это уточнение в оценивании является следствием анализа результатов ЕГЭ. Таким образом, максимальный балл за выполнение каждого из заданий части 3 составит соответственно: С1 – 3 балла, С2 – 4 балла, С3 – 5 баллов, С4 – 4 балла, С5 – 2 балла;
· Максимальный первичный балл за выполнение работы в целом составляет 66 баллов.
Результаты ЕГЭ по химии в 2009 году
В 2009 году ЕГЭ по химии сдавали 395 учащихся. В 2009 году была отменена система перевода баллов в школьную систему оценок, поэтому целесообразно проводить сравнительный анализ полученных результатов в баллах.
Из 395 учащихся, сдававших ЕГЭ по химии, два человека набрали максимальное количество баллов – 97, трое получили минимальное количество баллов – 27. В итоге средний тестовый балл по Томской области составил 55,2, в то время как по России эта показатель равен 54,7. 2009 год не оказался исключением, как и ранее, средний тестовый балл по ЕГЭ в Томской области выше Российского примерно на 1-3 %, что свидетельствует о стабильной и качественной подготовке учащихся к экзамену по данному предмету. Минимальное количество баллов, подтверждающее освоение выпускниками основных общеобразовательных программ среднего (полного) общего образования по химии, составило 33 балла (для сравнения: максимум 39 баллов – обществознание, минимум 20 баллов – иностранные языки). 33 человека в Томской области не подтвердили освоение программы средней школы.
Сравнение результатов сдачи ЕГЭ выпускниками школ Томской области с российскими показывает, что Томские школьники получили в 1,5 раза меньше низких баллов (меньше 32), более 20% учеников, то есть каждый пятый, набрали баллы выше 70. Таким образом, учащиеся г. Томска и области продемонстрировали стабильность знаний по химии.
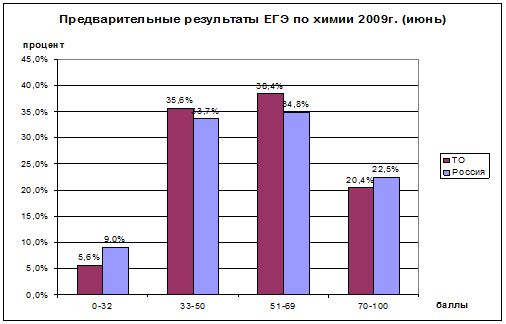
Рис. 2. Результаты ЕГЭ по химии в Томской области и России в 2009 г.
Анализ решаемости заданий ЕГЭ по химии
Экзаменационная работа ЕГЭ отвечает следующим исходным положениям:
· Содержание работы в целом соответствует требованиям к общеобразовательной подготовке по химии. В нее включаются для проверки только те элементы знаний, которые присутствуют в содержательных блоках «Обязательного минимума содержания среднего (полного) общего образования по химии».
· В работу включаются задания, проверяющие усвоение содержания всех ведущих разделов школьного курса химии, составляющих инвариантное ядро различных программ по химии для средней школы. Задания проверяют совокупность знаний о химическом элементе, веществе, химической реакции, методах познания и применения веществ и реакций. Таким образом, можно отметить, что по полноте охвата курса химии содержание работы полностью соотносится с целями обучения химии в средней школе.
· В работу включаются задания разного уровня сложности – базового, повышенного, высокого. Благодаря этому обеспечивается возможность дифференцированного оценивания достижений каждого выпускника, выполняющего работу.
· Условия заданий формулируются таким образом, чтобы задание предусматривало выполнение выпускником определенных действий: выявить классификационные признаки веществ и реакций, определить степень окисления химических элементов по формулам их соединений, объяснить сущность того или иного процесса, взаимосвязи состава, строения и свойств веществ и т. п.
· Равноценность всех вариантов экзаменационной работы обеспечивается строгим соблюдением одинакового соотношения числа заданий, проверяющих усвоение основных элементов содержания различных разделов курса: общей, неорганической и органической химии.
Такой подход к составлению экзаменационной работы обеспечивает инвариантность ее содержания в условиях вариативности преподавания химии на старшей ступени школы по различным программам и учебникам. Это означает, что каждый выпускник, независимо от того, по какому учебнику он изучал химию, имеет равные возможности для успешного выполнения заданий экзаменационной работы ЕГЭ.
Сравнение решаемости заданий базовой, повышенной и высокой уровней сложности показало, что средняя решаемость заданий базового уровня сложности (части А) составила 63,24 %, повышенной сложности (части В) - 44,3 % и 32,9 % - средняя решаемость заданий части С. Нужно отметить, что учащиеся Томской области, сдававшие экзамен по химии, показали неплохие результаты 95,4% учеников приступили к решению заданий высокой степени сложности, причем, во многих работах решены полностью, либо частично задачи С4, что свидетельствует о постепенном приобретении учащимися навыков решения расчетных многоходовых задач и умении логически мыслить.
Решаемость заданий базового уровня сложности
Каждый из вариантов билета ЕГЭ включал в себя 30 заданий базового уровня сложности.
Таблица 1.
Данные по решаемости заданий части А
№ | Проверяемые элементы содержания | Решаемость, % |
А1 | Современные представления о строении атомов; строение электронных оболочек атомов элементов первых четырех периодов (понятие об электронном облаке, s - и р - электронах; радиусы атомов, их периодические изменения в системе химических элементов). | 64,2 |
А2 | Периодический закон и периодическая система химических элементов . (Закономерности изменения химических свойств элементов и их соединений по периодам и группам.) | 78,1 |
А3 | Химическая связь: ковалентная (полярная и неполярная), ионная, металлическая, водородная. Способы образования ионной и ковалентной связи. Длина и энергия связи. | 70,8 |
А4 | Понятие об электроотрицательности химических элементов. Заряды ионов. Степень окисления. | 68,9 |
А5 | Вещества молекулярного и немолекулярного строения. Зависимость свойств веществ от особенностей их кристаллической решетки. | 62,8 |
А6 | Классификация неорганических веществ. | 65,2 |
А7 | Общая характеристика металлов главных подгрупп I—III групп, металлов – меди, хрома, железа в связи с их положением в периодической системе химических элементов и особенностями строения их атомов. | 62,0 |
А8 | Общая характеристика неметаллов главных подгрупп IV-VII групп в связи с их положением в периодической системе химических элементов и особенностями строения их атомов. | 59,9 |
А9 | Характерные химические свойства неорганических веществ различных классов: простых веществ-металлов, простых веществ-неметаллов | 63,8 |
А10 | Характерные химические свойства неорганических веществ различных классов: оксидов (основных, амфотерных, кислотных) | 62,5 |
А11 | Характерные химические свойства неорганических веществ различных классов: кислот, , оснований, амфотерных гидроксидов | 61,6 |
А12 | Характерные химические свойства неорганических веществ различных классов: солей (средних). | 35,2 |
А13 | Взаимосвязь неорганических веществ. | 70,1 |
А14 | Основные положения теории химического строения органических веществ А. М Бутлерова. Изомерия и гомология органических веществ. | 67,4 |
А15 | Классификация органических веществ. Систематическая номенклатура. | 67,8 |
А16 | Особенности химического и электронного строения алканов, алкенов, алкинов, их свойства. Бензол – ароматический углеводород (электронное строение и свойства). Толуол – гомолог бензола. | 58,6 |
А17 | Характерные химические свойства кислородсодержащих органических соединений: предельных одноатомных и многоатомных спиртов, фенола, альдегидов, предельных карбоновых кислот. | 65,2 |
А18 | Взаимосвязь органических веществ | 59,6 |
А19 | Классификация химических реакций. | 49,4 |
А20 | Понятие о скорости химической реакции. Факторы, влияющие на изменение скорости химической реакции. | 65,6 |
А21 | Обратимые и необратимые химические реакции. Химическое равновесие и условие его смещения. | 67,5 |
А22 | Электролитическая диссоциация неорганических и органических кислот, щелочей, солей. Степень диссоциации. | 64,6 |
А23 | Реакции ионного обмена. | 83,8 |
А24 | Реакции окислительно-восстановительные. | 59,9 |
А25 | Гидролиз солей (реакция среды раствора). | 76,8 |
А26 | Реакции, характеризующие основные свойства и способы получения углеводородов. | 61,8 |
А27 | Реакции, характеризующие основные свойства и способы получения кислородосодержащих и азотсодержащих соединений. | 47,2 |
А28 | Сведения о токсичности и пожарной опасности изучаемых веществ. Правила обращения с веществами и оборудованием. Методы исследования объектов, изучаемых в химии. (Качественные реакции неорганических и органических веществ.) | 59,4 |
А29 | Общие научные принципы химического производства (на примере промышленного получения аммиака, серной кислоты, метанола). Природные источники углеводородов, их переработка. Основные методы синтеза высокомолекулярных соединений (пластмасс, синтетических каучуков). | 53,1 |
А30 | Тепловой эффект химической реакции. Расчеты теплового эффекта реакции. | 64,7 |
Задания А1. Средняя решаемость заданий А1 составила 64,2 %, при этом наибольшую сложность составили вопросы:

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 |



