![]() . (2.51)
. (2.51)
Функция
![]() (2.52)
(2.52)
или
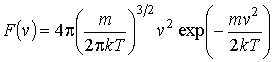 (2.53)
(2.53)
называется функцией распределения Максвелла по абсолютным значениям скоростей, и она показывает вероятность того, что величина скорости имеет значения от v до (v+dv).
На рис. 2.4 изображен график функции распределения F(v). Максимум этой функции соответствует наиболее вероятному значению скорости молекул газа vm, которую можно определить, приравняв к нулю производную от функции F(v):
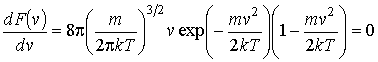 . (2.54)
. (2.54)
Отсюда следует, что кроме случаев когда v=0 и v=![]()
![]() , соответствующих минимуму функции F(v), имеется решение:
, соответствующих минимуму функции F(v), имеется решение:
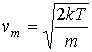 , (2.55)
, (2.55)
дающее выражение для наиболее вероятной скорости молекул газа.
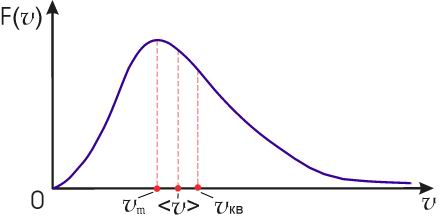
Рис.2.4
Кроме наиболее вероятной скорости, функция F(v) позволяет найти среднюю скорость:
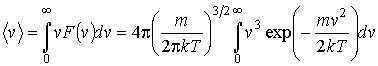 (2.56)
(2.56)
и среднее значение квадрата скорости
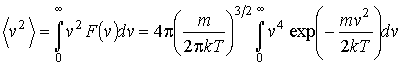 . (2.57)
. (2.57)
Вычисление интегралов окончательно дает выражения для средней скорости:
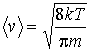 (2.58)
(2.58)
и для средней квадратичной скорости молекул:
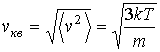 . (2.59)
. (2.59)
Формула (2.59) для средней квадратичной скорости может быть также получена на основании формулы, описывающей среднюю кинетическую энергию поступательного движения молекул газа.
Полученные значения скоростей численно отличаются друг от друга на величину, меньшую, чем их значения, причем ![]()
![]() , что проиллюстрировано на рис. 2.4.
, что проиллюстрировано на рис. 2.4.
Кроме функции распределения по абсолютным значениям скорости F(v)применяется функция распределения по значениям кинетической энергии
поступательного движения молекул FE(EK), характеризующая вероятность попадания значений кинетической энергии EK в интервал dEK:
![]() . (2.60)
. (2.60)
Приравняв вероятности ![]()
![]() или
или ![]()
![]() , и используя подстановку:
, и используя подстановку: ![]()
![]() и
и ![]()
![]() , имеем:
, имеем:
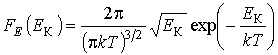 . (2.61)
. (2.61)
Необходимо отметить, что все полученные распределения справедливы только для равновесного состояния термодинамической системы. Вследствие достаточно общего метода их получения, они применимы не только для газов, но и для любых систем, движение микрочастиц которых описывается уравнениями классической механики.
Экспериментальная проверка распределения Максвелла
Одними из самых известных опытов с молекулярными пучками были эксперименты Штерна, в которых впервые удалось осуществить прямые измерения молекулярных скоростей.
-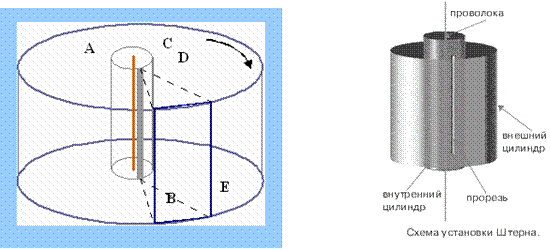
Рис. 2.5а Схема устройства прибора О. Штерна для измерения средней скорости движении молекул
Наиболее известная схема опыта (1920г.) Штерна показана на рис. 2.5б. Платиновая нить 1, на которую была нанесена капля серебра, находилась на оси двух коаксиальных цилиндров 2 и 3, причём в цилиндре 2 имелась щель, параллельная его оси. Цилиндры могли вращаться вокруг своей оси. В опытах Штерна угловая скорость их вращения составляла 2...3 тысячи оборотов в минуту.
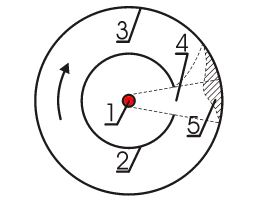
Рис. 2.5б
На рисунке обозначено: 1 - источник молекул, 2 и 3 - вращающиеся цилиндры,
4 - щель, ограничивающая молекулярный пучок, 5 - след молекулярного пучка
При пропускании через платиновую нить электрического тока она разогревалась до максимальной температуры порядка 1200 oС. В результате этого серебро начинало испаряться, его атомы пролетали через щель 4 цилиндра 2 и оседали на поверхности цилиндра 3, оставляя на нём след 5. Для не вращающихся цилиндров, атомы серебра, двигаясь прямолинейно, более-менее равномерно оседали на поверхности внешнего цилиндра, внутри сектора, соответствующего прямолинейному их распространению. Вращение цилиндров приводило к искривлению траектории молекул в системе отсчёта, связанной с цилиндрами и, как следствие, к изменению положения атомов серебра, осевших на внешний цилиндр.
Анализируя плотность осевших молекул, можно было оценить характеристики распределения молекул по скоростям, в частности, максимальную и минимальную скорости, соответствующие краям следа, а также найти наиболее вероятную скорость, соответствующую максимуму плотности осевших молекул.
При температуре нити 1200 oС среднее значение скорости атомов серебра, полученное после обработки результатов опытов Штерна, оказалось близким к 600 м/с, что вполне соответствует значению средней квадратичной скорости, вычисленному по формуле.
Прямые измерения скорости атомов ртути в пучке были выполнены в 1929 году Ламмертом. Упрощенная схема этого эксперимента показана на рис.2.6.
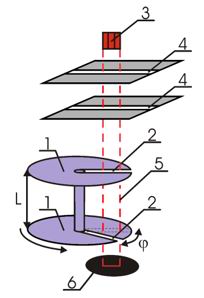 Рис. 2.6
Рис. 2.6
На рисунке 2.6 обозначено: 1 - быстро вращающиеся диски, 2 - узкие щели, 3 - печь, 4 - коллиматор, 5 - траектория молекул, 6 - детектор
Два диска 1, насаженные на общую ось, имели радиальные прорези 2, сдвинутые друг относительно друга на угол ![]() . Напротив щелей находилась печь 3, в которой нагревался до высокой температуры легкоплавкий металл. Разогретые атомы металла, в данном случае ртути, вылетали из печи и с помощью коллиматора 4 направлялись в необходимом направлении. Наличие двух щелей в коллиматоре обеспечивало движение частиц между дисками по прямолинейной траектории 5, параллельной их оси. В установке Ламмерта в дисках было сделано множество щелей (они на рисунке не изображены) с целью увеличения интенсивности прошедшего пучка. Далее атомы, прошедшие прорези в дисках, регистрировались с помощью детектора 6. Вся описанная установка помещалась в глубокий вакуум.
. Напротив щелей находилась печь 3, в которой нагревался до высокой температуры легкоплавкий металл. Разогретые атомы металла, в данном случае ртути, вылетали из печи и с помощью коллиматора 4 направлялись в необходимом направлении. Наличие двух щелей в коллиматоре обеспечивало движение частиц между дисками по прямолинейной траектории 5, параллельной их оси. В установке Ламмерта в дисках было сделано множество щелей (они на рисунке не изображены) с целью увеличения интенсивности прошедшего пучка. Далее атомы, прошедшие прорези в дисках, регистрировались с помощью детектора 6. Вся описанная установка помещалась в глубокий вакуум.
При вращении дисков с постоянной угловой скоростью ![]() , через их прорези беспрепятственно проходили только атомы, имевшие скорость
, через их прорези беспрепятственно проходили только атомы, имевшие скорость ![]() :
:
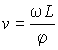 , (2.62)
, (2.62)
где ![]() - расстояние между вращающимися дисками.
- расстояние между вращающимися дисками.
Изменяя угловую скорость вращения дисков можно было отбирать из пучка молекулы, имеющие определенную скорость ![]() , и по регистрируемой детектором интенсивности судить об относительном содержании их в пучке.
, и по регистрируемой детектором интенсивности судить об относительном содержании их в пучке.
Таким способом удалось экспериментально проверить статистический закон распределения молекул по скоростям. Позже, когда при создании ядерного оружия возникла необходимость выделения нейтронов с определенной кинетической энергией, подобная схема была применена в устройстве, названным нейтронным монохроматором, позволяющим получать энергетические спектры нейтронов.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51 |




