![]() . (3.19)
. (3.19)
Анализ выражения (3.18) показывает, что теплоемкость при постоянном давлении больше теплоемкости при постоянном объеме. Это связано с тем, что при изобарическом процессе, в отличие от изохорического, совершается работа, на выполнение которой затрачивается часть подведенной теплоты.
Таким образом, молярная теплоёмкость идеального газа зависит от вида процесса, в котором он участвует, и от внешних условий, обеспечивающих протекание этого процесса. Например, в соответствии с определением теплоёмкости (3.3), для адиабатического процесса, когда теплообмен с окружающей средой отсутствует и ![]()
![]() , она равна нулю, а для изотермического при dT=0 - бесконечности.
, она равна нулю, а для изотермического при dT=0 - бесконечности.
Известный закон равнораспределения энергии по степеням свободы позволяет определять теплоемкость не только газов, но и твёрдых тел. В 1819 г. Пьер Луи Дюлонг (1785 - 1838) и Алексис Терез Пти (1791 - 1820) установили, что произведение удельной (на единицу массы вещества) теплоёмкости на атомную массу элемента, из которого состоит твёрдое тело, есть величина почти постоянная.
Закон Дюлонга и Пти был установлен ими эмпирически путём проведения большого количества опытов. В этих опытах измерялась скорость охлаждения различных веществ, находящихся при одинаковых внешних условиях, при которых передача теплоты определялась только разностью температуры вещества и окружающей среды. Если для различных веществ разности температур одинаковы, то отношение их теплоёмкостей будет равно обратному отношению скоростей изменения температуры.
В то время, когда Дюлонг и Пти проводили свои эксперименты, атомные массы многих элементов ещё не были установлены. Сейчас, с учетом того факта, что молярная масса пропорциональна атомной массе элемента, закон Дюлонга и Пти может быть сформулирован как закон постоянства молярной теплоёмкости
(при постоянном объёме) для большинства твёрдых тел, состоящих из простых соединений. Величина этой теплоемкости равна 24,9 Дж/моль*К.
Закон постоянства молярной теплоёмкости может быть объяснён равнораспределением энергии по степеням свободы. Считая твёрдое тело состоящим из атомов, каждый из которых представляет собой гармонический осциллятор с тремя степенями свободы, имеем на каждую степень свободы атома среднюю кинетическую энергию ![]()
![]() и такую же среднюю потенциальную энергию. Тогда внутренняя энергия одного моля вещества может быть определена с помощью формулы:
и такую же среднюю потенциальную энергию. Тогда внутренняя энергия одного моля вещества может быть определена с помощью формулы:
![]() , (3.20)
, (3.20)
а, соответственно, его молярная теплоемкость примет вид:
![]() , (3.21)
, (3.21)
что хорошо согласуется с указанным выше значением.
Закон Дюлонга и Пти удовлетворительно выполняется при комнатных и более высоких температурах. Однако, при низких температурах происходит "вымерзание" колебательных степеней свободы, и молярная теплоёмкость твердых тел уменьшается. Существуют вещества, например алмаз, бериллий, а также сложные кристаллические соединения, для которых закон Дюлонга и Пти не выполняется.
Опыт показал (см. приведенный ниже график), что в определенном интервале температур эта теплоемкость составляет всего (5/2)R, при очень низких температурах она уменьшалась до (3/2)R, а при высоких становится больше 3R. Это означает, что при низких температурах молекулы участвуют только в поступательном движении. По мере повышения Т молекулы начинают совершать и вращательные движения. И лишь при высоких температурах она совершает все три вида движения (добавляется колебательное).
Согласно приведенным формулам, теплоемкость идеального газа должна быть числом кратным R/2 и не зависеть от температуры. Однако эксперимент показывает, что достаточно хорошее совпадение экспериментальных данных с теоретическими выводами наблюдается лишь в случае одноатомных газов. Для многоатомных газов теплоемкость оказывается функцией температуры.
Из рисунка видно, что теплоемкость двухатомных молекул ступенчато растет с ростом температуры, как если бы степени свободы молекулы «включались» при разных температурах. В широком диапазоне температур (от нескольких кельвин
до тысяч кельвин) теплоемкость соответствует уравнению ![]() - молекула ведет себя, как молекула с жесткой связью. Значение теплоемкости
- молекула ведет себя, как молекула с жесткой связью. Значение теплоемкости ![]() для большинства газов нельзя достичь экспериментально, так как при столь высоких температурах происходит диссоциация молекул - молекулы распадаются на атомы.
для большинства газов нельзя достичь экспериментально, так как при столь высоких температурах происходит диссоциация молекул - молекулы распадаются на атомы.
Объяснить такую температурную зависимость теплоемкости газов можно лишь на основе квантовых представлений. В соответствии с этими представлениями, энергия вращательного ![]() и колебательного
и колебательного ![]() движений может принимать строго определенный, причем дискретный набор значений. Для того, чтобы молекула начала вращаться, или для того, чтобы возникли колебания ее атомов, молекуле необходимо сообщить энергию, превышающую, соответственно, значение
движений может принимать строго определенный, причем дискретный набор значений. Для того, чтобы молекула начала вращаться, или для того, чтобы возникли колебания ее атомов, молекуле необходимо сообщить энергию, превышающую, соответственно, значение ![]() или
или ![]() . Такая энергия может быть получена молекулой при столкновении с другой молекулой, если кинетическая энергия последней достаточно велика. Кинетическая энергия молекулы
. Такая энергия может быть получена молекулой при столкновении с другой молекулой, если кинетическая энергия последней достаточно велика. Кинетическая энергия молекулы![]() , следовательно, для возникновения вращения необходимо, чтобы
, следовательно, для возникновения вращения необходимо, чтобы ![]() , для возникновения колебаний -
, для возникновения колебаний - ![]() . Значения
. Значения ![]() и
и ![]() для различных газов приведены в таблице
для различных газов приведены в таблице
газ |
|
|
О2 | 2300 | 2,1 |
СО | 3050 | 2,8 |
N2 | 3400 | 2,9 |
Конечно, при любой температуре газа в нем есть молекулы с достаточно высокими энергиями. Но для того, чтобы теплоемкость приняла значение ![]() или
или ![]() , во вращательном и колебательном движениях должны участвовать большинство молекул. Поэтому реальные значения температур, при которых теплоемкость достигает соответствующих значений, превышают те, что приведены в таблице.
, во вращательном и колебательном движениях должны участвовать большинство молекул. Поэтому реальные значения температур, при которых теплоемкость достигает соответствующих значений, превышают те, что приведены в таблице.
Таким образом, температурная зависимость теплоемкости газов – это проявление квантовых законов движения и взаимодействия молекул.
3.3 Адиабатический процесс. Политропный процесс. Применение первого начала термодинамики к изопроцессам
В сороковых годах ХIХ столетия английский физик Джеймс Прескотт Джоуль (1818 - 1889) провёл серию экспериментальных исследований с целью выяснить, существует ли точное количественное соотношение между теплотой и механической энергией. В 1843г. Джоуль опубликовал результаты своей работы по установлению механического эквивалента теплоты. В его опытах было экспериментально показано, что внутренняя энергия является функций
состояния, зависящей только от того, в каком состоянии находится термодинамическая система. В дальнейшем термином состояние будем обозначать равновесное (или, точнее, квазиравновесное) состояние. Изменение функции состояния не зависит от того, каким образом термодинамическая система перешла из одного состояния в другое, а определяется только конечным и начальным состояниями системы.
Схема опыта Джоуля изображена на рис. 3.4. Воду, находящуюся в калориметре - сосуде с теплоизолированными стенками, перемешивали лопатками, насаженными на деревянный, не проводящий теплоту стержень. В сосуде были установлены перегородки с прорезями, не позволявшими воде приобретать большую скорость вращения. Благодаря этому, вследствие сил внутреннего трения по окончании вращения лопаток потоки в воде быстро затухали, и она приходила в состояние термодинамического равновесия.
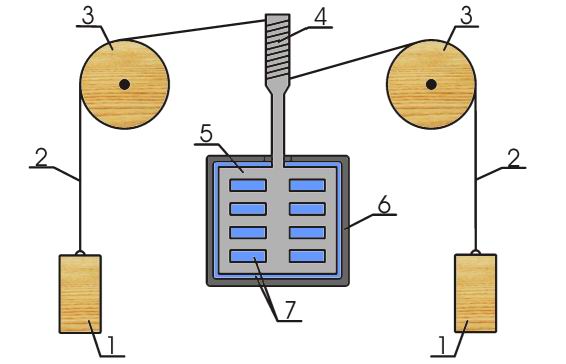
Рис.3.4
На рисунке 3.4: 1 - грузы, 2 - тросы, 3 - подвижные блоки, 4 - шкив, 5 - лопатка,
6 - теплоизолирующий сосуд, 7 - вода
При выполнении опытов предполагалось, что вода в сосуде является адиабатически изолированной термодинамической системой. Такой системой называется система, в которой изменения её состояния могут происходить только благодаря механическим перемещениям частей системы и её оболочки (окружающих тел) и не могут происходить путём теплообмена с окружающими телами. Любое изменение состояния адиабатически изолированной системы называют адиабатическим процессом, а оболочку, окружающую такую систему - адиабатической оболочкой.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51 |




