Примером адиабатической оболочки является сосуд Дьюара, названный по имени Джеймса Дьюара (1842 - 1923), который в 1892 году изобрёл его для сохранения сжиженных газов. Он представляет собой сосуд с двойными стенками (рис.3.5), пространство между которыми откачано до высокого вакуума, благодаря чему резко уменьшается теплообмен вещества в сосуде с окружающей
средой. Однако, идеальной адиабатической оболочки в природе не существует. Например, в сосудах Дьюара, даже при отсутствии теплообмена посредством конвекции, остаётся теплообмен посредством излучения и теплопроводности. Для уменьшения потока энергии за счет излучения стенки сосуда металлизируют, то есть покрывают тонким слоем металла, что повышает коэффициент зеркального отражения излучения. Вследствие невозможности реально изготовить идеальную адиабатическую оболочку, Джоуль при проведении своих экспериментов вводил поправку на охлаждение воды в течение опыта.
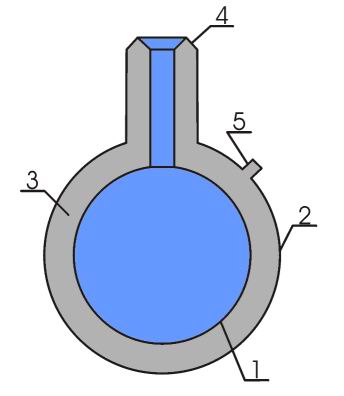
Рис.3.5
На рисунке 3.5 обозначено:1 - внутренняя оболочка, 2 - внешняя оболочка, 3 - вакуумная изоляция, 4 - горловина с низкой теплопроводностью, 5 - отросток для откачки.
Механическая работа, затрачиваемая на перемешивание воды в калориметре, определялась по изменению механической энергии двух гирь, опускавшихся под действием своего веса и посредством шкива создававших вращение стержня с лопатками. Зная высоту, на которую опустились гири и их скорости в нижней точке, можно определить изменение механической энергии системы.
Переход воды из одного состояния в другое регистрировался посредством измерений температуры воды в начальном и конечном состояниях. При заданных параметрах (в данном случае давлении и объёме воды), температура определяет состояние термодинамического равновесия системы. В описываемом эксперименте внешнее давление и объём воды можно считать неизменными. На самом деле начальное и конечное состояния воды характеризуются различными объёмами, однако, тепловое расширение воды настолько мало, что можно пренебречь изменением объёма и совершаемой при этом работой.
Джоуль обнаружил, что при различных моментах сил, скоростях движения лопаток, массах гирь и т. д., механическая работа, произведённая над водой при переходе из одного её состояния в другое фиксированное состояние, остаётся неизменной величиной при одинаковом количестве воды. Таким образом, удалось экспериментально подтвердить, что для адиабатического перехода системы из определённого начального состояния в определённое конечное состояние всегда требуется одинаковая работа, независимо от того, как осуществляется адиабатический переход.
Следовательно, механическая работа, совершённая над термодинамической системой при адиабатическом переходе из первого равновесного состояния во второе, является величиной, равной изменению некой функции состояния системы, значение которой с точностью до произвольной постоянной определяется равновесным состоянием термодинамической системы и не зависит от того, каким образом система пришла в это состояние. Этой функцией состояния является внутренняя энергия системы. Отметим, что температура, давление и объем также являются функциями состояния термодинамической системы.
Таким образом, работа А12, совершённая адиабатически изолированной термодинамической системой при переходе из первого состояния с внутренней энергией U1 во второе состояние с внутренней энергией U2, равна разности внутренних энергий в указанных состояниях:
![]() (3.22)
(3.22)
Соотношение (3.22) выражает первое начало термодинамики для адиабатически изолированных систем.
В опыте Джоуля силы трения совершали положительную работу, поэтому внутренняя энергия воды возрастала, а механическая энергия грузов уменьшилась. Так как в соответствии с определением внутренней энергии она представляет собой сумму кинетической и потенциальной энергий всех частиц, входящих в систему, то включение грузов в полную систему приводит соотношение (3.22) к выражению, описывающему закон сохранения энергии.
Таким образом, выражение (3.22) представляет собой запись закона сохранения энергии. При всяких изменениях состояния адиабатически изолированной системы, приращение энергии (внутренней и механической) одних тел обязательно равно убыли энергии (внутренней и механической) других тел.
Если в каком-либо состоянии величина внутренней энергии системы равна U1 (она определяется с точностью до константы), то в любом другом состоянии внутренняя энергия U2 может быть определена из соотношения:
![]() , (3.23)
, (3.23)
где ![]()
![]() - работа, совершённая над системой при адиабатическом переходе из первого состояния во второе состояние. Работа
- работа, совершённая над системой при адиабатическом переходе из первого состояния во второе состояние. Работа ![]()
![]() , совершенная над системой, равна взятой с отрицательным знаком работе A12, совершенной самой системой над внешними телами:
, совершенная над системой, равна взятой с отрицательным знаком работе A12, совершенной самой системой над внешними телами: ![]()
![]() =- A12
=- A12
Нахождение внутренней энергии с помощью выражения (3.23) возможно, если существует адиабатический переход из одного термодинамического состояния в другое.
Итак, адиабатически изолированная система, то есть система, которая не обменивается теплотой с окружающими телами. Процессы, происходящие в такой системе, называются адиабатическими. Так как при адиабатических процессах ![]()
![]() , то первое начало термодинамики для них можно записать в форме:
, то первое начало термодинамики для них можно записать в форме:
![]() . (3.24)
. (3.24)
Совместное применение этого выражения и уравнения Клапейрона-Менделеева позволяет получить уравнение, описывающее адиабатический процесс в идеальном газе. Для этого представим выражение (3.26) в виде:
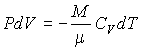 . (3.25)
. (3.25)
Нахождение полных дифференциалов от правой и левой частей уравнения Клапейрона-Менделеева дает:
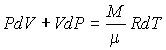 . (3.26)
. (3.26)
Вычитание из этой формулы выражения (3.27) приводит его к виду:
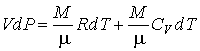 . (3.27)
. (3.27)
С учетом соотношения Майера имеем:
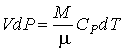 . (3.28)
. (3.28)
Умножим выражение (3.25) на отношение теплоемкостей ![]() и сложим его с формулой (3.28). Тогда получим:
и сложим его с формулой (3.28). Тогда получим:
![]() , (3.29)
, (3.29)
где введено обозначение:
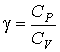 . (3.30)
. (3.30)
Величина ![]() называется показателем адиабаты. Используя ранее записанные формулы, можно определить показатель адиабаты через количество степеней свободы i:
называется показателем адиабаты. Используя ранее записанные формулы, можно определить показатель адиабаты через количество степеней свободы i:
![]() (3.31)
(3.31)
Из этого выражения следует, что показатель адиабаты для идеального газа всегда больше единицы. Для одноатомных газов этот показатель равен 1,67, а для двухатомных и многоатомных соответственно 1,4 и 1,33.
Поделив уравнение (3.29) на произведение PV, преобразуем его к виду:
![]() (3.32)
(3.32)

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51 |




