Процесс охлаждения газа может быть реализован так же с помощью обратимого адиабатического расширения. Тогда для обратимого адиабатического расширения газа можно записать:
![]() . (6.21)
. (6.21)
С учетом формулы (6.6) имеем:
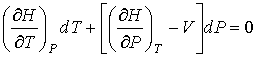 . (6.22)
. (6.22)
Отсюда следует, что при описании обратимого адиабатического процесса вместо формулы (6.7) необходимо использовать выражение:
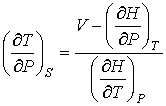 . (6.23)
. (6.23)
С учетом полученных выше выражений вместо формулы (6.13) можно записать:
УМКД 042-18-38.1.11/01-2013 | Редакция № 1 от «11сентября»2013 г. | Страница 13 из 1 |
УМКД 042-18-38.1.11/01-2013 | Редакция № 1 от «11сентября»2013 г. | Страница 110 из 155 |
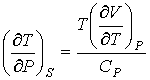 . (6.24)
. (6.24)
Для газов характерно изобарическое расширение при их нагревании. Поэтому из условия
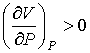 , (6.25)
, (6.25)
справедливого для всех газов, следует, что:
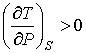 . (6.26)
. (6.26)
Поэтому при обратимом адиабатическом расширении газ охлаждается (![]() ), так как при этом его давление уменьшается (
), так как при этом его давление уменьшается (![]() ). В частности, при расширении идеального газа, из формул (6.14) и (6.24) имеем:
). В частности, при расширении идеального газа, из формул (6.14) и (6.24) имеем:
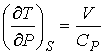 . (6.27)
. (6.27)
Для газа Ван-дер-Ваальса при обратимом адиабатическом расширении с учетом формулы (6.19) при условии ![]() получим следующее выражение для определения изменения его температуры:
получим следующее выражение для определения изменения его температуры:
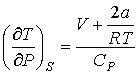 . (6.28)
. (6.28)
Из выражений (6.27) и (6.28) следует, что как идеальный газ, так и газ Ван-дер-Ваальса охлаждается при обратимом адиабатическом расширении.
Таким образом, применение для охлаждения газа обратимого адиабатического процесса имеет принципиальное преимущество по сравнению с применением эффекта Джоуля-Томсона, связанное с отсутствием явления инверсии. Однако для реализации этого преимущества возникает необходимость создания технических устройств, в которых газ должен совершать механическую работу над внешними телами, например, над поршнем или турбиной. Только в этом случае расширение газа может быть обратимым. Машины, служащие для получения низких температур за счет расширения газа с совершением им механической работы, получили названия детандеров. Для охлаждения больших количеств газа наибольшее распространение получили турбодетандеры, в которых вместо поршня используется турбина. Обеспечение работоспособности детандеров и турбодетандеров в условиях низких температур является достаточно сложной технической задачей.
Особенности жидкого состояния. Поверхностное натяжение. Формула Лапласа. Капиллярные явления.
УМКД 042-18-38.1.11/01-2013 | Редакция № 1 от «11сентября»2013 г. | Страница 111 из 155 |
Жидкость занимает по свойствам и строению промежуточное положение между газами и твердыми кристаллическими веществами. Поэтому обладает свойствами как газообразных, так и твердых веществ.
В молекулярно-кинетической теории различные агрегатные состояния вещества связывают с различной степенью упорядоченности молекул. Для твердых тел наблюдается так называемый дальний порядок в расположении частиц, т. е. их упорядоченное расположение, повторяющееся на больших расстояниях. В жидкостях имеет место так называемый ближний порядок в расположении частиц, т. е. их упорядоченное расположение, повторяющееся на расстояниях, сравнимы с межатомными. При температурах, близких к температуре кристаллизации, структура жидкости близка к твердому телу. При высоких температурах, близких к температуре кипения, структура жидкости соответствует газообразному состоянию – практически все молекулы участвуют в хаотическом тепловом движении.
Жидкости, подобно твердым телам, обладают определенным объемом, подобно газам, принимают форму сосуда, в котором они находятся. Молекулы газа практически не связаны между собой силами межмолекулярного взаимодействия, и в данном случае средняя энергия теплового движения молекул газа гораздо больше средней потенциальной энергии, обусловленной силами притяжения между ними, поэтому молекулы газа разлетаются в разные стороны и газ занимает предоставленный ему объем. В твердых и жидких телах силы притяжения между молекулами уже существенны и удерживают молекулы на определенном расстоянии друг от друга. Средней энергии теплового движения молекул недостаточно для преодоления сил притяжения между молекулами, поэтому твердые тела и жидкости имеют определенный объем. Давление в жидкостях с увеличением температуры и уменьшением объема возрастает весьма резко. Объемное расширение жидкостей гораздо меньше, чем паров и газов, так как более значительны силы, связывающие молекулы в жидкости; то же замечание касается теплового расширения.
Теория жидкости до настоящего времени полностью не развита. Разработка ряда проблем в исследовании сложных свойств жидкости принадлежит (1894 – 1952). Тепловое движение в жидкости он объяснял тем, что каждая молекула в течение некоторого времени колеблется около определенного положения равновесия, после чего скачком переходит в новое положение, отстоящее от исходного на расстоянии порядка межатомного. Таким образом, молекулы жидкости довольно медленно перемещаются по всей массе жидкости. С повышением температуры жидкости частота колебательного движения резко увеличивается, возрастает подвижность молекул.
Характерной особенностью жидкости является ее способность иметь свободную поверхность (не ограниченную твердыми стенками).
Поверхность жидкости, соприкасающейся с другой средой, например, с ее собственным паром, с какой-либо другой жидкостью или с твердым телом (в частности, со стенками сосуда, в котором она содержится), находится в особых условиях по сравнению с остальной массой жидкости. Возникают эти особые условия потому, что молекулы пограничного слоя жидкости окружены молекулами той же жидкости не со всех сторон.
УМКД 042-18-38.1.11/01-2013 | Редакция № 1 от «11сентября»2013 г. | Страница 112 из 155 |
Рассмотрим две молекулы внутри жидкости (рис.7.1). Пусть r – расстояние, при котором рассматриваемая молекула взаимодействует с соседней молекулой. Если молекула находится на расстоянии, большем чем r, то взаимодействия нет. Такой
радиус называют радиусом молекулярного взаимодействия, а сфера этого радиуса – сферой молекулярного действия. Величина r имеет порядок нескольких молекулярных диаметров (~10-9м). В сфере
молекулярного действия молекулы в глубине заполнены равномерно. Для второй, поверхностной, молекулы часть соседей – это частицы второй среды. В случае, если жидкость граничит со своим собственным паром (насыщенным), то есть в случае, когда мы имеем дело с одним веществом, сила, испытываемая молекулами поверхностного слоя, направлена внутрь жидкости. Это объясняется тем, что
Рис.7.1 плотность молекул в жидкости много больше, чем в насыщенном паре над жидкостью. Поэтому сила притяжения, испытываемая молекулой поверхностного слоя со стороны жидкости больше, чем со стороны молекул пара. Действием молекул в выступающей части сферы молекулярного действия (в поверхностном слое) можно пренебречь. Но тогда будет действовать некоторая равнодействующая, направленная вглубь жидкости. Таким образом, результирующие силы всех молекул поверхностного слоя оказывают на жидкость давление, называемое молекулярным (или внутренним).
Под действием силы, стремящейся втянуть молекулу внутрь жидкости, происходит непрерывное перемещение одних молекул внутрь и выход других, более энергичных молекул наружу. Если молекула движется из глубины в поверхностный слой, то должна совершаться работа (за счет убыли энергии теплового движения молекул).

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51 |




