- при каком условии происходят явления переноса? как записывается в общем виде уравнение переноса?
УМКД 042-18-38.1.11/01-2013 | Редакция № 1 от «11сентября»2013 г. | Страница 136 из 155 |
- чем объяснить то, что все явления переноса протекают медленно, хотя все они происходят благодаря быстрым движениям молекул?
- что называют градиентом некоторой физической величины?
- как можно рассчитать коэффициенты переноса?
- что такое технический вакуум?
- почему коэффициент теплопроводности не зависит от давления в случае, когда средняя длина свободного пробега значительно меньше линейных размеров сосуда?
- какая связь существует между коэффициентами теплопроводности и внутреннего трения?
- при каком разрежении газа коэффициент внутреннего трения убывает обратно пропорционально концентрации молекул газа?
- получите выражение для коэффициента диффузии и найдите его связь с другими коэффициентами переноса для нейтрального газа.
- как меняются коэффициенты переноса при изменении давления, если газ находится: а) в состоянии, далеком от технического вакуума; б) в состоянии технического вакуума?
- как изменяются коэффициенты переноса при изменении температуры, если газ находится: а) в состоянии, далеком от технического вакуума; б) в состоянии технического вакуума?
- как может быть рассчитана внутренняя энергия реального газа?
- чем определяется внутренняя энергия молекул реального газа?
Чем объясняется то, что в процессе дросселирования при комнатной температуре водород нагревается, а кислород охлаждается?
- каков в опыте Джоуля-Томсона знак приращения внутренней энергии газа? энтропии? энтальпии (тепловой функции)?
- расширение 1 моль газа в опыте производится от начального состояния, характеризуемого параметрами T0, V0, до сильно разреженного состояния, в котором газ можно считать идеальным. График изменения состояния газа изображается в плоскости (T, V) кривой, которая делит эту плоскость на две области: в одной области ?Т<0 (газ охлаждается), в другой – ?Т> 0 (газ нагревается). Каков физический смысл отмеченных на рисунке температуры Т1, объема V1? Как меняется температура газа при дросселировании, если в начальном состоянии газ имеет: а)параметры точки 1; б)параметры точки 2?
Т
Т1
0 V1 V
Рассмотрите примеры решения задач:
Задача 1.. В сосуде объемом 200 л находится 300 моль водорода при нормальном давлении. Во сколько раз надо увеличить температуру, чтобы давление увеличилось в 3 раза? Сравнить с результатами для идеального газа.
УМКД 042-18-38.1.11/01-2013 | Редакция № 1 от «11сентября»2013 г. | Страница 137 из 155 |
Дано: V=0,2 м3, ?=300 моль, ?=2.10-3кг/моль, р1?105Па, р2=3р1
Найти: Т2/Т1 - ?
Решение. Учитывая, что объем сосуда не изменяется при повышении температуры, запишем уравнения Ван-дер-Ваальса для первого и второго состояний реального газа:
![]() ;
; ![]() .
.
Разделив второе уравнение на первое, получим:
![]() .
.
После вычислений получим Т2/Т1?2,3.
Если считать газ идеальным, то уравнения состояний можно записать так:
р1V=?RT1; р2V=?RT2 .
Разделив эти равенства почленно, получим Т2/Т1=р2/р1=3.
Сравнивая полученные числовые результаты, замечаем, что идеальный газ нагревается в этих условиях до более высокой температуры, чем реальный.
Задача 2. В баллоне емкостью 8 л находится 300 г кислорода при температуре 27оС. Найти, какую часть объема составляет собственный объем молекул. Определить отношение внутреннего давления р’ к давлению газа р на стенки сосуда.
Дано: V=8.10-3м3, m=0,3 кг, ?=32.10-3кг/моль, Т=300К, а=0,137Дж. м3/моль2, b=3.10-5 м3/моль.
Найти: х1=V’/V - ? x2=p’/p - ?
Решение.
Поправка b в уравнении Ван-дер-Ваальса равна учетверенному собственному объему молекул одного моля газа: (m/?)b=4V’; V’=bm/(4?).
Этот объем занимает долю объема газа:
х1= bm/(4?V). x1=3.10-5.0,03/(4.32.10-3. 8.10-3) ?9.10-3=0,8%
Для ответа на второй вопрос задачи надо найти отношение
x2=p’/p, где p’- внутреннее, а p - внешнее давления:
p’=(m/?)2a/V2 ; p’?1,86.105 Па.
Давление р, производимое газом на стенки сосуда, найдем из уравнения Ван-дер-Ваальса: 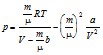 ?2,79.106(Па).
?2,79.106(Па).
Отсюда x2=p’/p=1,86.105/2,79.106=0,066=6,6%.
Задача 3. В цилиндре под поршнем находится один моль азота при нормальных условиях. Какую часть объема сосуда занимают при этом молекулы азота? Газ расширяется до объема, вдвое большего первоначального, при постоянной температуре. Найти изменение внутренней энергии газа и совершенную работу. Каково было бы значение этих величин, если бы газ был идеальным?
Дано: ?=1 моль, ?=28.10-3кг/моль, Т=273К, р=105 Па, V2=2V1, а=0,136Дж. м3/моль2, b=4.10-5 м3/моль.
Найти: ?U - ? A -? x - ?
УМКД 042-18-38.1.11/01-2013 | Редакция № 1 от «11сентября»2013 г. | Страница 138 из 155 |
Решение. Поправка Ван-дер-Ваальса b равна учетверенному собственному объему молекул: b= 4 V, откуда V= b/4= 10-5 м3/моль, что составляет х= b/4Vм=10-5/22,4.10-3=4,4.10-4 часть объема, занимаемого при нормальных условиях.
?U=![]() 0,136 /2.22,4.10-3?3 (Дж/моль)
0,136 /2.22,4.10-3?3 (Дж/моль)
![]()
A?8,314.273.2,3.ln2-0,136 /2.22,4.10-3?1,56.103-3?1,56.103 (Дж)
При идеальном процессе изменение внутренней энергии ?U=0, а работа А=1,56.103Дж/моль.
Рассмотреть примеры решения задач (Сборник задач по курсу общей физики под ред. вып.1989г.) № 15-5,7,10,13,19
Тема: Жидкости. Поверхностное натяжение. Капиллярные явления
Цель занятия: Дать анализ особенностей жидкого состояния, достичь понимания явлений в поверхностном слое жидкости; капиллярных явлений и его следствий.
Закрепление основных понятий.
Повторить теоретический материал по теме занятия и ответьте на следующие вопросы:
- молекулы жидкости, подобно частицам твердого тела, совершают колебания около некоторых положений равновесия. в чем отличие в поведении молекул жидких тел от поведения молекул газа, твердых тел?
- в чем причина малой сжимаемости жидкостей и особых свойств поверхностного слоя?
- если концы s-образной картонной пластинки потереть мылом и положить на поверхность воды, то пластинка начинает вращаться. почему? проверьте результат на опыте.
- почему струйка воды, вытекающая из водопроводного крана, постепенно делается тоньше и наконец распадается на отдельные капли?
- вертикальная капиллярная стеклянная трубка подвешена к коромыслу весов и уравновешена гирьками. что произойдет с весами, если под капиллярную трубку осторожно поднести сосуд с водой так, чтобы кончик капилляра коснулся ее поверхности?
- воду, находившуюся в стакане, вылили на пол. как при этом изменилась энтропия воды?
- мыльную пленку адиабатически растягивают (увеличивают ее поверхность). как при этом меняется ее температура?
Рассмотрите примеры решения задач:
Задача 1. Из конца стеклянной капиллярной трубки, опущенной в воду, выдули пузырек воздуха радиусом 0,02 см. При этом давление воздуха в пузырьке превышало атмосферное на 984 Па. На какую глубину опущена трубка.
Дано: r=2.10-4м, р-ро=984 Па, ?=103кг/м3, ?=0,07 Н/м.
Найти: h-?
Решение.
УМКД 042-18-38.1.11/01-2013 | Редакция № 1 от «11сентября»2013 г. | Страница 139 из 155 |
На глубине давление внутри пузырька складывается из атмосферного (над водой), гидростатического (слоя воды над пузырьком) и лапласовского:
р=ро+?gh+2?/r,
или р - ро=?gh+2?/r,
откуда
h=(р– рo–2?/r)/(?g) = 0,028 м.
Задача 2. Определить изменение свободной энергии поверхности мыльного пузыря при изотермическом увеличении его объема от 10 см3 до 20 см3. Считать для мыльного раствора ?=0,04 Н/м.
Дано: V1 =10-5м3, V2=2. 10-5м3, ?=0,04 Н/м.
Найти: ?Е - ?
Решение.
Свободная энергия поверхности жидкости пропорциональна площади этой поверхности: Е=?S. У мыльного пузыря имеются две поверхности - внешняя и внутренняя, площади которых практически равны из-за малой толщины мыльной пленки. Поэтому свободная энергия поверхности (внешней и внутренней вместе) мыльного пузыря Е=2?S.
Так как, по условию задачи, процесс изотермический, то поверхностное натяжение, являющееся для данной жидкости функцией только температуры, остается постоянным. Следовательно, изменение свободной энергии: ?Е=2??S, где ?S - изменение поверхности пузыря (одной - внутренней или внешней). Считая, что мыльный пузырь имеет форму сферы, найдем ?S:
?S=4?r22 - 4?r12, где r1 и r2 - радиусы сфер, соответствующие V1 и V2: r1=(3V1/4?)1/3, r1=(3V1/4?)1/3.
Тогда ?S=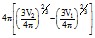 .
.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51 |




