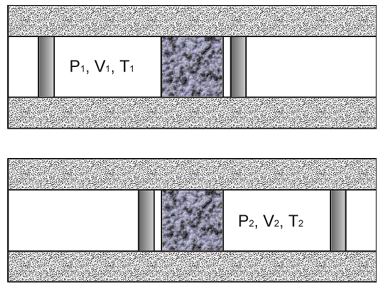
Рис.6.4
Проведем описание процесса протекания газа через пористую перегородку. Считая этот процесс достаточно медленным и адиабатическим, а также, учитывая постоянство давлений P1 и P2, применим первое начало термодинамики:
![]() (6.3)
(6.3)
Удобно для рассмотрения ввести функцию состояния:
![]() (6.4)
(6.4)
Функция H(P, S) является термодинамическим потенциалом при независимых параметрах P и S, и называется энтальпией. Учитывая определение энтальпии (6.4 =4.28):
УМКД 042-18-38.1.11/01-2013 | Редакция № 1 от «11сентября»2013 г. | Страница 107 из 155 |
![]() . (6.5)
. (6.5)
Следовательно, рассматриваемый процесс является не только адиабатическим, но и изоэнтальпийным.
Далее будем считать, что изменения давления ![]()
![]() и температуры
и температуры ![]() газа в рассматриваемом процессе малы. Тогда с точностью до величин второго порядка малости можно записать:
газа в рассматриваемом процессе малы. Тогда с точностью до величин второго порядка малости можно записать:
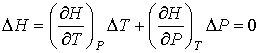 . (6.6)
. (6.6)
Следовательно:
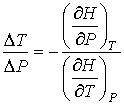 . (6.7)
. (6.7)
Для определения частных производных энтальпии ![]() найдем полный дифференциал от выражения (6.4)
найдем полный дифференциал от выражения (6.4)
![]() . (6.8)
. (6.8)
Тогда с учетом формулы (6.6) имеем:
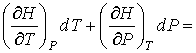
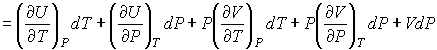 (6.9)
(6.9)
Из формулы (6.9) следует:
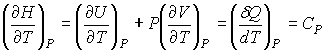 , (6.10)
, (6.10)
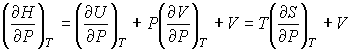 . (6.11)
. (6.11)
где ![]() - теплоемкость газа при постоянном давлении.
- теплоемкость газа при постоянном давлении.
Произведя ряд преобразований, можно получить следующее соотношение:
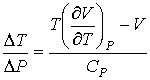 (6.12)
(6.12)
или для бесконечно малого изменения давления
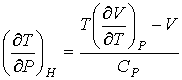 , (6.13)
, (6.13)
УМКД 042-18-38.1.11/01-2013 | Редакция № 1 от «11сентября»2013 г. | Страница 108 из 155 |
где производная 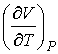 определяется уравнением состояния газа. Формула (6.12) позволяет рассчитать изменение температуры газа при просачивании его через пористую перегородку.
определяется уравнением состояния газа. Формула (6.12) позволяет рассчитать изменение температуры газа при просачивании его через пористую перегородку.
Если при проведении опыта использовать идеальный газ, описываемый уравнением Клапейрона-Менделеева, то имеем:
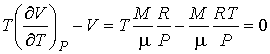 . (6.14)
. (6.14)
Следовательно, для идеального газа ![]() и изменения его температуры при прохождении через пористую перегородку не происходит.
и изменения его температуры при прохождении через пористую перегородку не происходит.
Таким образом, при необратимом адиабатическом расширении идеального газа через пористую перегородку его температура не изменяется, в отличие от обратимого адиабатического расширения, приводящего в соответствии с формулой (6.2) к охлаждению идеального газа.
Данный результат связан с тем, что при адиабатическом расширении идеального газа в опыте Джоуля-Томсона механическая работа не совершается, в отличие от обратимого адиабатического расширения. При применении в этом опыте реального газа совершаемая им механическая работа определяется силами межмолекулярного взаимодействия, и её знак зависит от этих сил.
Рассмотрим применение в опыте Джоуля-Томсона газа Ван-дер-Ваальса, уравнение для одного моля которого имеет вид:
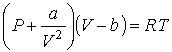 . (6.15)
. (6.15)
Раскроем скобки в этом уравнении
![]() (6.16)
(6.16)
и пренебрегая третьим и четвертым слагаемыми в левой части получившегося выражения в связи с их малостью (считая ![]() ), продифференцируем его по температуре
), продифференцируем его по температуре ![]() при постоянном давлении
при постоянном давлении ![]() :
:
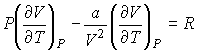 (6.17)
(6.17)
или
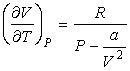 . (6.18)
. (6.18)
Выражая ![]() из формулы (6.15) и подставляя в (6.18) с последующим пренебрежением малыми слагаемыми имеем:
из формулы (6.15) и подставляя в (6.18) с последующим пренебрежением малыми слагаемыми имеем:
УМКД 042-18-38.1.11/01-2013 | Редакция № 1 от «11сентября»2013 г. | Страница 109 из 155 |
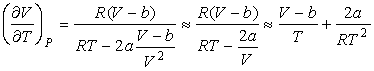 . (6.19)
. (6.19)
Тогда формула (6.12) для отношения ![]() принимает вид:
принимает вид:
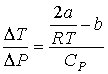 . (6.20)
. (6.20)
Из этой формулы следует, что существует температура:
![]() ,
,
при которой газ Ван-дер-Ваальса, проходя через пористую перегородку, не изменяет свою температуру. Эта температура ![]() называется температурой инверсии, так как при
называется температурой инверсии, так как при ![]() отношение
отношение ![]() и наблюдается охлаждение газа (так как
и наблюдается охлаждение газа (так как ![]() и, следовательно
и, следовательно ![]() ), а при
), а при ![]() отношение
отношение ![]() и газ нагревается. В первом случае эффект Джоуля-Томсона считается положительным, а во втором - соответственно отрицательным.
и газ нагревается. В первом случае эффект Джоуля-Томсона считается положительным, а во втором - соответственно отрицательным.
Как следует из проведенного анализа, при выполнении условия ![]() наблюдается охлаждение газа при необратимом адиабатическом расширении. По этой причине эффект Джоуля-Томсона применяется для охлаждения и ожижения газов, таких, например, как водород и гелий.
наблюдается охлаждение газа при необратимом адиабатическом расширении. По этой причине эффект Джоуля-Томсона применяется для охлаждения и ожижения газов, таких, например, как водород и гелий.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51 |




