Примеры уравнений состояния реального газа:
Уравнение Ван-дер-Ваальса (1873г.): 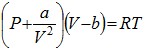
Уравнение Клаузиуса (1880г.): 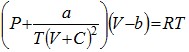
Уравнение Бертелло (1900г.): 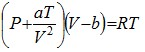
Уравнения Дитеричи: I.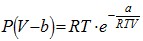 ,
,
уравнение записано в предположении, что распределение молекул описывается законом распределения Больцмана: ![]()
II.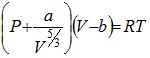 ,
,
при записи уравнения учитывалась поверхностная плотность молекул в пристенном слое.
Уравнение Валя (1914г.): 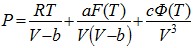 ,
,
здесь первое слагаемое определяет термическое давление;
второе – определяется силами притяжения;
третье - определяется силами отталкивания.
6.2 Внутренняя энергия реального газа. Эффект Джоуля-Томсона, его физическая сущность. Сжижение газов
В идеальном газе отсутствуют молекулярные взаимодействия, поэтому его внутренняя энергия, поскольку в нем представляет собой кинетическую энергию теплового движения молекул, которая зависит от температуры газа, но не зависит от занимаемого газом объема. В реальных газах нельзя пренебрегать
УМКД 042-18-38.1.11/01-2013 | Редакция № 1 от «11сентября»2013 г. | Страница 104 из 155 |
взаимодействием молекул, и потому внутренняя энергия реального газа находится суммированием кинетической энергии движения молекул Ек и потенциальной энергии их взаимодействия Ер:
![]()
Выразим Ек и Ер через макроскопические характеристики системы. Как и для идеального газа, кинетическая энергия молекул реального газа по определению пропорциональна его температуре, и для 1 моль
![]()
Потенциальная энергия молекулярного взаимодействия зависит от взаимного расположения молекул и потому должна изменяться при изменении объема газа. Потенциальную энергию взаимодействия можно определить, если учесть, что элементарная работа сил взаимодействия при Т=соnst равна: ![]() .
.
Эта работа связана с изменением потенциальной энергии взаимодействия молекул: ![]() , то есть
, то есть ![]() .
.
Поэтому ![]() . Приняв потенциальную энергию при V >® ?Ґ равной нулю, получим для внутренней энергии реального газа следующее выражение:
. Приняв потенциальную энергию при V >® ?Ґ равной нулю, получим для внутренней энергии реального газа следующее выражение:
![]()
![]() .
.
В отличие от идеального газа температура реального газа может изменяться даже в том случае, если его внутренняя энергия остается постоянной, так как она зависит не только от температуры, но и от объема.
Если исключить обмен энергией между газом и внешней средой, то сумма присущей молекулам газа кинетической и потенциальной энергией должна оставаться постоянной. Следовательно, изменение одного из видов энергии должно компенсироваться противоположным изменением второго вида энергии:
![]() .
.
Рассмотрим явление адиабатического расширения газа в вакуум. Представим себе сосуд, разделенный на две части перегородкой. В одной части находится газ, в другой - вакуум. Если убрать перегородку, то газ устремится в пустую часть сосуда. Так как работа против внешних сил в рассматриваемом случае отсутствует и, по условию, теплообмена нет, то внутренняя энергия газа до и после расширения газа должна быть одинаковой:
![]() .
.
Изменение температуры: ![]()
Так как V2>V1, то Т2<T1 (при расширении в пустоту газ Ван-дер-Ваальса охлаждается).
Эффекта Джоуля-Томсона.
В экспериментах, проведенных Джоулем и Томсоном на реальных газах, было установлено, что при адиабатическом расширении их температура изменяется, причем может, как повышаться, так и понижаться. Это явление получило название эффекта Джоуля-Томсона. Объясняется этот эффект тем, что
УМКД 042-18-38.1.11/01-2013 | Редакция № 1 от «11сентября»2013 г. | Страница 105 из 155 |
в силу закона сохранения энергии, уменьшение кинетической энергии реального газа равно приращению его потенциальной энергии. Если потенциальная энергия взаимодействия молекул реального газа при расширении возрастает, то его температура при этом падает. Если потенциальная энергия уменьшается, то его температура растет. В частности, для газа Ван-дер-Ваальса, если силы притяжения играют более существенную роль, чем силы отталкивания, то газ при расширении охлаждается, а если силы отталкивания превосходят силы притяжения, то его температура увеличивается. Практическое применение эффекта Джоуля-Томсона связано в первую очередь с охлаждением газов и ожижением их. В конце XIX века Карлом Линде (1842 - 1934) была разработана машина для ожижения воздуха, в которой охлажденный вследствие эффекта Джоуля-Томсона воздух осуществляет предварительное охлаждение следующей порции воздуха, которая затем в свою очередь расширяется с уменьшением температуры. Повторяя процесс многократно, можно получить температуру воздуха ниже критической, и ожижить его. Используя эту схему, нидерландский физик Гейке Камерлинг-Оннес (1853 - 1926) в 1908 году получил жидкий гелий, что стало началом новой области физики - физики низких температур.
Для получения жидкого гелия потребовалось предварительно охладить его жидким водородом. Для получения жидкого водорода также потребовалось его предварительное охлаждение жидким воздухом. Это объясняется тем, что расширение сжатых (как правило, до нескольких десятков атмосфер) гелия и водорода при комнатной температуре сопровождается увеличением их температуры. Предварительное охлаждение позволяет перевести их в состояние, при котором адиабатическое расширение приводит к их охлаждению.
В 30-е годы XX столетия советским физиком (1894 - 1984) был разработан более эффективный способ получения сжиженных газов, основанный на том, что газ при адиабатическом расширении совершает положительную работу, то есть его внутренняя энергия уменьшается. Созданное Капицей устройство называется турбодетандером. В нем газ совершает работу при вращении теплоизолированной турбины.
Адиабатическое расширение газа обычно приводит к изменению его температуры. Если при адиабатическом расширении уменьшение внутренней энергии газа равно совершенной им механической работе над внешними телами, то такой процесс будет обратимым. При обратимом адиабатическом расширении температура газа изменяется в соответствии с уравнением адиабаты. Для идеального газа эта зависимость имеет вид:
![]() , (6.2)
, (6.2)
где: V1 и T1 - объем и температура газа в начале процесса, V2 и T2 - объем и температура газа после расширения. Так как V2 > V1 , то из формулы (6.2) следует, что при обратимом адиабатическом расширении идеального газа происходит уменьшение его температуры: T2< T1.
Указанное уменьшение температуры идеального газа при его адиабатическом расширении происходит только в том случае, если этот процесс является обратимым. Опыт Гей-Люссака показал, что при необратимом адиабатическом расширении идеального газа без совершения им работы над
УМКД 042-18-38.1.11/01-2013 | Редакция № 1 от «11сентября»2013 г. | Страница 106 из 155 |
внешними телами его внутренняя энергия и температура остаются неизменными. Поэтому при таком расширении использование выражения (6.2) для определения температуры идеального газа становится невозможным.
При необратимом адиабатическом расширении величина и знак изменения температуры зависят от свойств использующегося в процессе газа. Необратимое адиабатическое расширение газа может быть осуществлено путем его пропускания через пористую перегородку, которая обеспечивает медленное течение газа без возникновения в нем турбулентных потоков, что позволяет считать кинетическую энергию газа малой величиной. Наблюдаемый при этом эффект, заключающийся в изменении температуры газа, называется эффектом Джоуля-Томсона. На примере описания этого эффекта рассмотрим применение метода термодинамических потенциалов.
На рис.6.4 схематически изображен опыт Джоуля-Томсона. Внутри теплоизолированной трубки помешалась пористая перегородка, через которую осуществлялось медленное стационарное течение газа. Газ внутри пористой перегородки находится в неравновесном состоянии, а процесс его протекания - является необратимым. Но вследствие медленности течения, газ по обе стороны от перегородки можно считать находящимся в равновесии. Давления P1 и P2 в обеих частях цилиндрической трубки поддерживались постоянными. Пусть при протекании через пористую перегородку некоторой порции газа, имевшей объем V1 и температуру T1, она приобрела объем V2 и температуру T2.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51 |




