Другая ситуация имеет место в случае, если учитывать изменение объёма тела, но пренебрегать внутренними силами трения в нём. Тогда механическая работа, совершаемая телом, будет определяться механическим движением границы тела (все внутренние движения из-за отсутствия трения не приведут к совершению работы). В этом случае, без учета изменения потенциальной энергии тела при наличии, например, гравитационных или электромагнитных полей, работа, совершенная телом, определяется двумя параметрами - давлением и объёмом.
В случае, если термодинамические процессы в системе квазиравновесные, и потоки энергии, вещества и т. д. в ней отсутствуют, то можно пренебречь внутренним трением, считая, что изменения объёма и давления определяют изменение состояния системы.
Работа ![]() , совершаемая телом (например, газом) над внешними телами при перемещении элемента поверхности этого тела (оболочки газа), площадью
, совершаемая телом (например, газом) над внешними телами при перемещении элемента поверхности этого тела (оболочки газа), площадью ![]() , на расстояние
, на расстояние ![]() вдоль нормали к поверхности равна:
вдоль нормали к поверхности равна:
![]() , (3.8)
, (3.8)
где ![]() - сила, действующая по нормали к поверхности
- сила, действующая по нормали к поверхности ![]() ,
, ![]() - внешнее давление, которое считается неизменным при перемещении элемента
- внешнее давление, которое считается неизменным при перемещении элемента ![]() на расстояние
на расстояние ![]() . Если давление
. Если давление ![]() одно и то же во всех точках поверхности тела, то, просуммировав по всей поверхности, получим:
одно и то же во всех точках поверхности тела, то, просуммировав по всей поверхности, получим:
![]() , (3.9)
, (3.9)
где ![]() - работа, совершённая телом при приращении его объёма на малую величину
- работа, совершённая телом при приращении его объёма на малую величину ![]() (см. рис.3.1).
(см. рис.3.1).
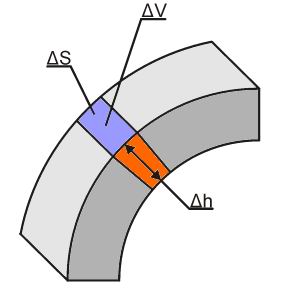
Рис. 3.1
Для элементарной работы ![]() выражение (1.11) принимает вид:
выражение (1.11) принимает вид:
![]() (3.10)
(3.10)
Работа при конечных изменениях объёма тела может быть определена путем интегрирования выражения (3.10):
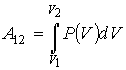 (3.11)
(3.11)
Этот интеграл зависит от пути перехода из состояния с объемом V1 в состояние с объемом V2 , так как функция P(V) может иметь различный вид.
Рисунок 3.2 иллюстрирует зависимость величины интеграла (3.11), численно равного площади под кривой P(V), от вида функции P(V).
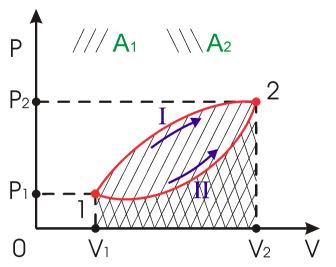
Рис.3.2
В зависимости от траектории I или II перехода из первого состояния во второе, площадь под кривой P(V) будет различна, а, следовательно, будет различна механическая работа, совершаемая системой в этих термодинамических
процессах. Количество теплоты Q12, необходимое для перехода из первого состояния во второе, также будет зависеть от вида кривой P(V) (формы траектории). В этом можно убедиться, если учесть тот факт, что внутренняя энергия является функцией состояния термодинамической системы, и ее изменение при переходе из первого состояния во второе не зависит от пути этого перехода. А, следовательно, в соответствии с первым началом термодинамики (3.2) теплота, так же как и работа, должна зависеть от термодинамического процесса, с помощью которого производился переход термодинамической системы.
Первое начало термодинамики запрещает создание вечных двигателей первого рода, принцип действия которых основан на получения полезной работы без подвода внешней энергии к системе. Действительно, если к системе не подводится теплота Q, то в соответствии с формулой (3.2) полезная работа A может быть совершена только за счет убыли внутренней энергии системы на величину ![]()
![]() . А так как внутренняя энергия любой системы ограничена, то и совершаемая таким образом полезная работа так же будет некоторой ограниченной величиной. После исчерпания внутренней энергии совершение системой полезной работы прекратится, и двигатель остановится.
. А так как внутренняя энергия любой системы ограничена, то и совершаемая таким образом полезная работа так же будет некоторой ограниченной величиной. После исчерпания внутренней энергии совершение системой полезной работы прекратится, и двигатель остановится.
3.2 Молярные и удельные величины. Теплоемкость газа. Понятие о квантовой теории теплоемкости
Теплоёмкость идеального газа
Как показывают результаты экспериментов, во многих случаях приращение температуры тела прямо пропорционально количеству теплоты, сообщенного ему. Для количественного описания этого соотношения вводится коэффициент пропорциональности Стела между количеством теплоты, сообщаемого телу, и изменением его температуры, называемым теплоёмкостью:
![]() (3.3)
(3.3)
Этот коэффициент позволяет определить количество теплоты ![]()
![]() , которое необходимо сообщить телу для повышения его температуры на величину dT.
, которое необходимо сообщить телу для повышения его температуры на величину dT.
В самом общем случае для произвольного тела его теплоемкость может зависеть от параметров состояния этого тела, например, от его температуры или объема. Очевидно, что теплоемкость термодинамической системы изменяется при изменении количества вещества в ней. Для систем, находящихся в состоянии термодинамического равновесия, их теплоемкость пропорциональна количеству вещества. Это позволяет ввести для описания свойств тела удельную теплоемкость:
![]() (3.4)
(3.4)
и, соответственно, молярную теплоемкость:
![]() , (3.5)
, (3.5)
где: ![]() - масса тела,
- масса тела, ![]()
![]() - количество вещества в нем. Эти теплоемкости связаны между собой через молярную массу
- количество вещества в нем. Эти теплоемкости связаны между собой через молярную массу ![]()
![]() следующим соотношением:
следующим соотношением:
![]() (3.6)
(3.6)
Теплоемкость, так же как и количество переданной телу теплоты, зависит от того, каким образом, а точнее при осуществлении какого процесса, теплота передавалась этому телу.
Если в процессе изменения состояния идеального газа теплоёмкость его не изменяется, то такой процесс называется политропическим. Частными случаями политропического процесса являются рассмотренные ранее изопроцессы, протекающие при постоянных значениях температуры, давления или объема.
Проведем определение теплоёмкости идеального газа в процессе, при котором его объём остаётся неизменным. При таком процессе работа не совершается: ![]()
![]() , так как нет изменения объема газа. Поэтому, в соответствии с первым началом термодинамики, имеем равенство подведенной к телу теплоты
, так как нет изменения объема газа. Поэтому, в соответствии с первым началом термодинамики, имеем равенство подведенной к телу теплоты ![]()
![]() и изменения его внутренней энергии dU:
и изменения его внутренней энергии dU:

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51 |




