6. Реальные газы
6.1 Уравнение, изотермы Ван дер Ваальса, их анализ. Критическое состояние. Область двухфазных состояний
Известно, что при изучении тех или иных явлений природы физики на основе данных опыта и измерений устанавливают количественные соотношения между величинами, характеризующими изучаемое явление. Такие соотношения часто имеют приближенный характер и справедливы в определенных пределах переменных величин. В этом смысле универсальными являются законы сохранения энергии и импульса (для замкнутых систем).
Изученное ранее уравнение Клапейрона-Менделеева также является приближенным, и справедливо только при достаточно малых давлениях, когда газ мы считаем идеальным. При повышении давления наблюдаются отклонения от записанных ранее газовых законов. Приведенные в таблице данные (для азота) демонстрируют отклонение поведения реального газа от законов, записанных для идеального газа.
Р, атм |
|
| Р, атм |
|
|
1 100 300 500 | 224 2,4 0,85 0,625 | 224 240 255 322 | 700 900 1000 | 0,532 0,483 0,460 | 372 437 461 |
УМКД 042-18-38.1.11/01-2013 | Редакция № 1 от «11сентября»2013 г. | Страница 99 из 155 |
В таблице приведены полученные на опыте значения объема V одного моля азота N2 при различных давлениях p и температуре 273 К (00С), а также значения произведения pV.
Видно, что с увеличением р значения V все больше отличаются от теоретически вычисленных по уравнению Клапейрона, аналогичное можно сказать о произведении pV. Произведение pV непрерывно растет с увеличением р, все более отклоняясь от значения, требуемого уравнением Клапейрона. Указанное несоответствие данных опыта уравнению состояния идеального газа носит не только количественный характер, но связан и с важными качественными
изменениями при достаточно высоких давлениях и соответствующих температурах. Известно, что при определенных значениях давления и температуры газ конденсируется, т. е. переходит в жидкое состояние. Этот процесс можно исследовать экспериментально в установке, схематически представленной на рис.6.1. Пусть исследуемый газ помещен в сосуд, закрытый подвижным поршнем. Будем поддерживать температуру постоянной, но ниже характерного для
каждого газа значения. Перемещая поршень М вверх, уменьшают
рис.6.1 объем и увеличивают тем самым давление газа, которое измеряется
манометром М. При этом давление растет непрерывно, причем сначала обратно пропорционально V, а потом все медленнее. Затем достигает некоторой предельной величины и дальше не изменяется, хотя поршень продолжает подниматься. В это время на стенках сосуда и поверхности поршня появляются капельки жидкости. Дальнейшее продвижение поршня вверх сопровождается увеличением количества жидкости под поршнем и, соответственно, уменьшением количества газа (пара) над жидкостью, при этом манометр показывает неизменное давление, которое остается постоянным до тех пор, пока весь объем между поршнем и стенками сосуда не окажется заполненным жидкостью. Если продолжить подъем поршня, т. е. сжимать жидкость, то даже самое незначительное уменьшение объема вещества приводит к значительным (очень большим) увеличениям давления, т. е. сжимаемость жидкости очень мала. Вместо поршня часто применяется жидкостный «поршень» - пресс Кальете. В этом случае под действием внешнего давления перемещается столбик ртути, над которым находится исследуемый газ. Ниже представлена схема описываемого пресса, (Далее включается демонстрационная компьютерная модель установки).
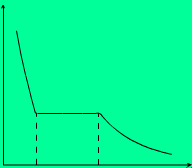
Графически описанный процесс изображается изотермой (рис. 6.2)
УМКД 042-18-38.1.11/01-2013 | Редакция № 1 от «11сентября»2013 г. | Страница 100 из 155 |
p
 V
V
0 V2 V1
рис.6.2
Начало процесса конденсации происходит при значении объема V1 и продолжается до значения объема V2, когда газ полностью переходит в жидкое состояние. После чего происходит уже сжатие жидкости. На участке между V1 и V2 часть сосуда занята жидкостью, часть – газом, который в этом случае называется насыщенным паром. Давление насыщенного пара (упругость насыщенного пара) не зависит от объема V, зависит лишь от температуры Т.
Примечание: чтобы представить порядок величин, характеризующих конденсацию, можно привести численные данные, относящиеся к воде (водяному пару). Так, при 200 С рнас= 17,5 мм. рт. ст. Молярный объем водяного пара, вычисленный из уравнения состояния идеального газа, Vм= 1,04 м3/моль.
Молярный объем жидкости (воды) равен приблизительно 1,8?10-5м3.
Т. е. соотношение ![]() . Даже при 1000С
. Даже при 1000С ![]()
Поэтому представить эту изотерму для воды в реальном масштабе (удобном!) невозможно. Можно эти результаты сравнивать, используя понятие «плотность», т. е. 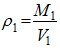 - для пара;
- для пара; 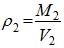 - для воды
- для воды
Нагляднее картина изменения названных величин представлена в таблице «Плотность воды и ее насыщенного пара при различных Т и р»:
Т, К | р, 105 Па |
|
|
273,15 323,15 373,15 423,15 473,15 523,15 573,15 623,15 647,25 | 0,006 0,122 1,013 4,750 15,54 39,76 85,88 165,34 217,72 | 0,004 0,083 0,6 2,5 8,0 19,9 46,2 113,6 329,0 | 999,9 988,0 958,0 917,0 863,0 799,0 712,0 575,0 329,0 |
УМКД 042-18-38.1.11/01-2013 | Редакция № 1 от «11сентября»2013 г. | Страница 101 из 155 |
Из таблицы видно, что при Т=647,3К ![]() (плотность воды и насыщенного пара равны). Т. е. при этой температуре Т стирается граница между жидкостью и ее насыщенным паром.
(плотность воды и насыщенного пара равны). Т. е. при этой температуре Т стирается граница между жидкостью и ее насыщенным паром.
При Т> 647,3К вода ведет себя как обычные газ, т. е. при повышении р ее объем V уменьшается. Вместо двух агрегатных состояний (жидкого и газообразного), существующих одновременно, остается только одно – газообразное, хотя при достаточно высоком давлении плотность такого газа может стать равной плотности жидкости и превысить ее.
Все изложенное относится не только к воде, но и к любому веществу.
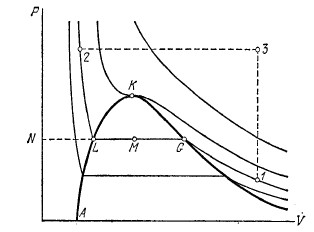
Для каждого вещества существует некоторая температура, при которой исчезает различие между паром и жидкостью, и выше которой вещество может быть только однородным при любом сжатии. Эту температуру называют критической температурой, для разных веществ она различна. Для углекислоты экспериментальное исследование уравнения состояния при высоких давлениях впервые провел Эндрьюс. Полученные изотермы приведены на рис.6.3. Изотермы
Рис.6.3 соответствуют разным Т. По мере увеличения Т горизонтальный участок становится все короче, т. к. удельный объем жидкости и пара сближаются. Наконец, при 31,40С горизонтальный участок исчезает, вырождаясь в точку перегиба К, - удельные объемы жидкости и пара становятся равными. Эту изотерму, соответствующую Тк, называют критической изотермой.
При Т < Тк образование жидкости ни при каких р невозможно. Увеличение р вызывает только увеличение плотности (уменьшение объема). При Т > Тк изотермы качественно выглядят так же, как изотермы идеального газа.
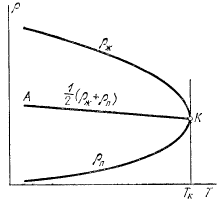
Ещё одной иллюстрацией описанного служит график, полученный по данным опыта изучения зависимости плотности жидкого азота и его насыщенного пара от температуры Т.
УМКД 042-18-38.1.11/01-2013 | Редакция № 1 от «11сентября»2013 г. | Страница 102 из 155 |
Здесь можно видеть, как плотность жидкого азота с повышением Т уменьшается, а плотность паров растет, пока при Тк=-147,10С обе плотности не достигнут одинакового значения. Соответствующие объем и давление называют критическими: ![]() , Тк, Vк – параметры критического состояния.
, Тк, Vк – параметры критического состояния.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51 |




