Таким образом, соединение всех этих методов исследования позволило продуктивно решать обильный круг проблем: строение вещества в различных агрегатных состояниях (твердом, жидком, газообразном), вопросы изменения структуры при переходах вещества из одной термодинамической фазы в другую, а также в результате изменения внешних физических факторов (давление, температура, электрическое и магнитное поле и т. д.). Соединение указанных методов позволило на количественном и качественном уровнях описать явления переноса (диффузия, теплопроводность, внутреннее трение). Кроме того, успешно описываются кристаллическое состояние вещества, образование полимеров,
явления, происходящие на границе раздела жидкостей, твердых тел и газов. Развитие молекулярной физики привело к выделению из нее самостоятельных разделов науки – таких, как физическая кинетика, физика твердого тела, физическая химия, молекулярная биология, физика металлов, физика полимеров, физика плазмы, кристаллофизика, физико-химия дисперсных частиц и поверхностных явлений, физико-химическая механика.
При всем различии объектов и методов исследования, применяемых в указанных разделах науки, имеет место главная идея: исследование микроскопических свойств молекулярных систем (физических тел) основывается на микроскопическом (то есть молекулярном) представлении о материи.
В молекулярной физике впервые ставится вопрос о строении материи, в частности, о строении вещества как формы существования материи. В последующих разделах физики (электродинамика, оптика, атомная физика, физика элементарных частиц) эта проблема получает дальнейшее развитие в рамках единой концепции “вещество-поле”.
Окружающие нас тела кажутся нам сплошными. Наши органы чувств способны воспринимать вещество, построенные из вещества тела – как непрерывно заполненные без промежутков объекты, но оказалось, что наши органы чувств вводят нас в заблуждение Развитие методов исследования, технических средств, физических технологий привело к выводу: все тела реального мира имеют дискретное (т. е. прерывное) строение: то есть они построены из мельчайших частиц, обладающих микроскопическими размерами и массой (микрочастиц), которые взаимодействуют друг с другом посредством различных физических полей (физические поля – это материальная субстанция, осуществляющая взаимодействие микрочастиц и макротел). Идея о прерывном строении вещества зародилась еще в V в. до н. э. (2,5 тысячи лет тому назад).
Впервые эта идея появилась в трудах древнегреческих античных философов Анаксагора, Демокрита и Эпикура: атом представлялся как мельчайшая частица вещества, наделенная свойством неделимости (atomos – неделимый, греч.). Представление об атомном строении вещества оставалось вплоть до XX века гениальнейшей догадкой выдающихся умов, которая была сформулирована интуитивно, но не имела экспериментального подтверждения.
Представление об атомах вещества преследовались церковными и светскими властями во всем мире, и поэтому успехи, которые могли быть достигнуты в области атомно-молекулярном строении, велись до 1626 г. Действовал, в частности, декрет, который запрещал любые обсуждения атомизма под страхом смертной казни. Возрождение атомизма следует относить к началу 17 века. Его связывают с именами Пьера Гассенди, Роберта Бойля, Даниила Бернулли. В 1738 г. Бернулли впервые дал не только качественное, но и количественное объяснение давления в газе; его представления практически полностью совпадают с современными. Бернулли объяснял, что давление, производимое газом на оболочку, есть результат множественных столкновений большого числа частиц газа с этой оболочкой.
В пределах XVII-XVIIIв. в. многие ученые не разделяли атомизма. В их числе были такие как Рене Декарт, . Наиболее прогрессивными и последовательными оказались взгляды . Он считал, что все тела
состоят из мельчайших частиц, которые он называл элементами. “Элемент есть частица тела, не состоящая из каких-либо других меньших или отличающихся от него тел.”
На современном языке термину “элемент” у Ломоносова сопоставляют термин “атом”. Далее, Ломоносов указывал, что наряду с элементами, существуют более сложные частицы – “корпускулы”. “Корпускулы есть собрание элементов, образующие одну малую массу. Корпускулы однородны, если состоят из одинакового количества одних и тех же элементов. Корпускулы разнородны, когда элементы их различны или соединены различными образами или в различном числе. От этого зависит бесконечное разнообразие тел”. (Ломоносов.) Термину “корпускула” в современном физическом языке соответствует термин “молекула”.
Современные представления об атомах и молекулах: атомы – частицы вещества микроскопических размеров и массы (микрочастица), которые представляют данный химический элемент и являются носителем его физико-химических свойств.
Молекулярно-кинетическая теория (МКТ) – это учение, которое объясняет тепловые явления в макроскопических телах и внутренние свойства этих тел движением и взаимодействием атомов, молекул и ионов, из которых состоят тела. В основе молекулярно-кинетической теории строения вещества лежат три основных положения:
- Вещество состоит из частиц – молекул, атомов и ионов. В состав этих частиц входят более мелкие элементарные частицы. Молекула – наименьшая устойчивая частица данного вещества. Молекула обладает основными химическими свойствами вещества. Молекула является пределом деления вещества, то есть самой маленькой частью вещества, которая способна сохранять свойства этого вещества. Атом – это наименьшая частица данного химического элемента.
- Частицы, из которых состоит вещество, находятся в непрерывном хаотическом (беспорядочном) движении.
- Частицы вещества взаимодействуют друг с другом - притягиваются и отталкиваются.
Эти основные положения подтверждаются экспериментально и теоретически.
Современные приборы позволяют наблюдать изображения отдельных атомов и молекул. С помощью электронного микроскопа или ионного проектора (микроскопа) можно получить изображения отдельных атомов и оценить их размеры. Диаметр любого атома имеет порядок d = 10-8 см (10-10 м). Размеры молекул больше размеров атомов. Поскольку молекулы состоят из нескольких атомов, то чем больше количество атомов в молекуле, тем больше её размер. Размеры молекул лежат в пределах от 10-8 см (10-10 м) до 10-5 см (10-7 м).
Непрерывное хаотическое движение частиц подтверждается броуновским движением и диффузией. Хаотичность движения означает, что у молекул не существует каких-либо предпочтительных путей и их движения имеют случайные направления. Это означает, что все направления равновероятны.
Диффузия (от латинского diffusion – растекание, распространение) – явление, когда в результате теплового движения вещества происходит самопроизвольное проникновение одного вещества в другое (если эти вещества соприкасаются). Взаимное перемешивание веществ происходит по причине непрерывного и беспорядочного движения атомов или молекул (или других частиц) вещества. С течением времени глубина проникновения молекул одного вещества в другое увеличивается. Глубина проникновения зависит от температуры: чем выше температура, тем больше скорость движения частиц вещества и тем быстрее протекает диффузия. Диффузия наблюдается во всех состояниях вещества – в газах, жидкостях и твёрдых телах. Примером диффузии в газах служит распространение запахов в воздухе при отсутствии прямого перемешивания. Диффузия в твёрдых телах обеспечивает соединение металлов при сварке, пайке, хромировании и т. п. В газах и жидкостях диффузия происходит намного быстрее, чем в твёрдых телах.
Существование устойчивых жидких и твёрдых тел объясняется наличием сил межмолекулярного взаимодействия (сил взаимного притяжения и отталкивания). Этими же причинами объясняется малая сжимаемость жидкостей и способность твёрдых тел сопротивляться деформациям сжатия и растяжения.
Силы межмолекулярного взаимодействия имеют электромагнитную природу – это силы электрического происхождения. Причиной этого является то, что молекулы и атомы состоят из заряженных частиц с противоположными знаками зарядов – электронов и положительно заряженных атомных ядер. В целом молекулы электрически нейтральны. По электрическим свойствам молекулу можно приближённо рассматривать как электрический диполь.
Силы притяжения принято считать отрицательными, а силы отталкивания – положительными, хотя это деления является условным.
Сила взаимодействия между молекулами имеет определённую зависимость от расстояния между молекулами. Эта зависимость изображена на рис. 1.1. Здесь показаны проекции сил взаимодействия на прямую, которая проходит через центры молекул.
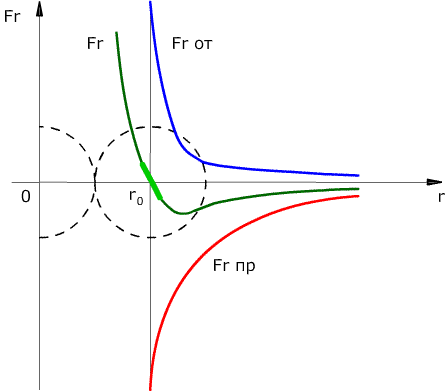
Рис. 1.1
Как видим, по мере уменьшения расстояния между молекулами r сила притяжения Fr пр увеличивается (красная линия на рисунке). Как уже было сказано, силы притяжения принято считать отрицательными, поэтому по мере уменьшения расстояния кривая уходит вниз, то есть в отрицательную зону графика.
Силы притяжения действуют по мере сближения двух атомов или молекул, пока расстояние r между центрами молекул находится в районе 10-9 м (2-3 диаметра молекул). По мере увеличения этого расстояния силы притяжения ослабевают. Силы притяжения являются короткодействующими силами.
![]() (1.1)
(1.1)
где a – коэффициент, зависящий от вида сил притяжения и строения взаимодействующих молекул.
При дальнейшем сближении атомов или молекул на расстояниях между центрами молекул порядка 10-10 м (это расстояние сравнимо с линейными размерами неорганических молекул) появляются силы отталкивания Fr от (синяя линия на рис.1.1). Эти силы появляются за счёт взаимного отталкивания положительно заряженных атомов в молекуле и убывают с увеличением расстояния r ещё быстрее, чем силы притяжения (что видно на графике – синяя линия более «круто» стремится к нулю, чем красная).
![]() (1.2)
(1.2)

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51 |




