Рассмотрим одноатомный идеальный газ. Предположим, что молекулы газа движутся хаотически, число взаимных столкновений между молекулами газа очень мало по сравнению с числом ударов о стенки сосуда, а соударения молекул со стенками сосуда абсолютно упругие. Выделим на стенке сосуда элементарную площадку ?s (cм. рис.) и вычислим давление, оказываемое на эту площадку. При каждом соударении, молекула, движущаяся перпендикулярно
площадке, передает ей импульс т0 v–(–m0 v) = 2 т0 v, где т0 — масса молекулы, v – ее скорость. За время ?t достигнут площадки ?s только те молекулы, которые заключены в объеме цилиндра с основанием ?s и высотой v?t. Число этих молекул равно n?s v?t, где п — концентрация молекул. Но необходимо учитывать, что реально молекулы движутся к площадке под разными углами и имеют различные скорости.
Для упрощения расчетов хаотическое движение молекул заменяют движением вдоль трех взаимно перпендикулярных направлений, тик что в любой момент времени вдоль каждого из них движется 1/3 молекул, причем половина (1/6) из них движется вдоль данного направления в одну сторону, половина - в противоположную. Тогда число ударов со стороны молекул, движущихся в заданном направлении, о площадку ?s будет ![]() . При столкновении с площадкой эти молекулы передадут ей импульс:
. При столкновении с площадкой эти молекулы передадут ей импульс:
![]()
![]() .
.
Тогда давление газа на стенку сосуда:
![]() (1)
(1)
Если газ и объеме V содержит N молекул, движущихся со скоростями v1, v2., то используют среднюю квадратичную скорость:
![]() (2)
(2)
характеризующую всю совокупность молекул газа. Уравнение (1) с учетом (2) примет вид:
![]() . (3)
. (3)
Полученное выражение называется основным уравнением молекулярно-кинетической теории идеальных газов. Это уравнение как раз и устанавливает связь между давлением и скоростью, вернее среднеквадратичной скоростью.
Введем E![]() – среднюю кинетическую энергию хаотического поступательного
– среднюю кинетическую энергию хаотического поступательного
движения одной молекулы, тогда основное уравнение запишется как:
![]()
или ![]() E
E
В полученном уравнении давление связано со средней энергией поступательного движения молекул. Таким образом, давление газа численно равно 2/3 средней кинетической энергии поступательного движения молекул, содержащихся в единице объема.
1.2 Газовые законы. Уравнение состояния идеального газа. Внутренняя энергия идеального газа. Закон равномерного распределения энергии по степеням свободы
Газовые законы. Уравнение состояния идеального газа
Экспериментальное исследование свойств газов, проведенное в ХVII-XVIII вв. Бойлем, Мариоттом, Гей-Люссаком, Шарлем, привело к формулировке газовых законов:
1. Изотермический процесс – Т=const.
Закон Бойля-Мариотта: pV=const – уравнение изотермы (рис.1.2)
График зависимости p от V приведен. Чем выше изотерма, тем более высокой температуре она соответствует, T2>T1.
2. Изобарный процесс: p= const.
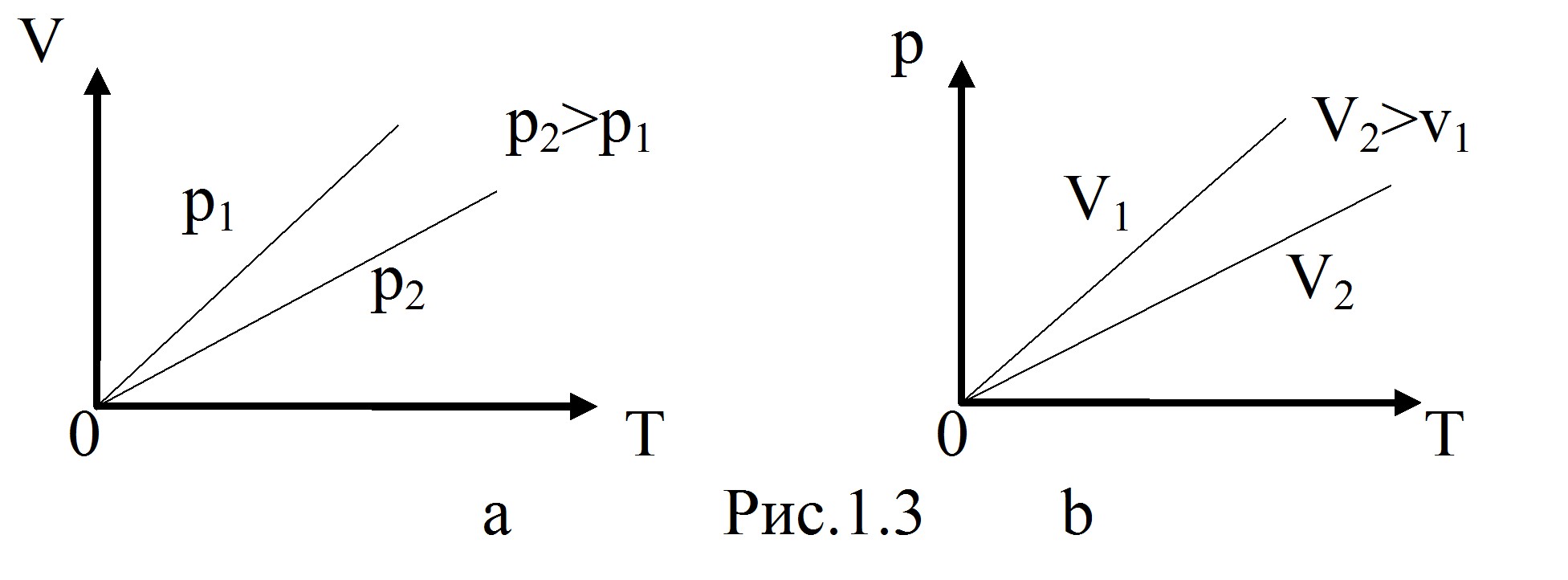
Закон Гей-Люссака: ![]() – уравнение изобары. График зависимости V от T Рис. 1.2 приведен на рисунке 1.3а. Чем ниже к оси
– уравнение изобары. График зависимости V от T Рис. 1.2 приведен на рисунке 1.3а. Чем ниже к оси
температуры наклонена изобара, тем большему давлению она соответствует, р2 > p1.
3. Изохорический процесс– V=const. Закон Шарля: ![]() – уравнение изохоры. График зависимости р от Т изображен на рисунке 1.3b. Чем ниже к оси температуры наклонена изохора, тем большему объему она соответствует, V2 >V1.
– уравнение изохоры. График зависимости р от Т изображен на рисунке 1.3b. Чем ниже к оси температуры наклонена изохора, тем большему объему она соответствует, V2 >V1.
Комбинируя выражения газовых законов, получим уравнение, связывающее р, V, Т (объединенный газовый закон): ![]() .
.
Постоянная в этом уравнении определяется экспериментально. Для 1 моль газа она оказалась равной R=8,31 ![]() и была названа универсальной газовой постоянной.
и была названа универсальной газовой постоянной.
1 моль равен количеству вещества системы, содержащей столько же структурных элементов, сколько содержится атомов в углероде-12 массой 0,012кг. Число молекул (структурных единиц) в 1 моле равно числу Авогадро: NA=6,02.1023моль-1.
Для R справедливо соотношение: R=k NA
Итак, для одного моля: ![]() .
.
Для произвольного количества газа ? = m/? (уравнение Менделеева-Клапейрона):
![]() ,
,
где ? - молярная масса газа.
Установим связь между уравнением кинетической теории газов и уравнением Менделеева-Клапейрона.
Так как n=N/V, то ![]() .
.
![]() E
E![]() ,
, ![]() .
.
Для количества молей вещества справедливо соотношение: ![]() , а для постоянной Больцмана: k = R /NA, поэтому последнее уравнение можно записать в виде:
, а для постоянной Больцмана: k = R /NA, поэтому последнее уравнение можно записать в виде: ![]()
или ![]() .
.
Степени свободы, распределение энергии по степеням свободы
До сих пор рассматривали модель идеального газа, молекулы которого считались материальными точками, то есть одноатомный газ. Для таких молекул число их степеней свободы, в соответствии с классической механикой, равняется количеству координат, необходимому для задания их положения в пространстве. Очевидно, что число координат в трехмерном пространстве, т. е. и число степеней свободы одноатомного газа, равно трем.
Однако молекула газа не обязательно должна состоять из одного атома, который считается материальной точкой. Газ может быть двухатомным, трёхатомным и т. д. Для молекул таких газов характерно наличие внутренней структуры и, соответственно, дополнительных степеней свободы. Если атомы в молекуле жестко связаны между собой, в качестве дополнительных степеней свободы выступают вращательные степени, характеризующие угловое положение молекулы в пространстве. В этом случае двухатомные молекулы имеют дополнительно две вращательные степени свободы, так как учет вращения вокруг оси, соединяющей атомы, считающиеся материальными точками, не имеет смысла. Следовательно, для такой молекулы общее число её степеней свободы равно пяти. Для молекул, состоящих из трех и более жестко связанных атомов, число дополнительных вращательных степеней свободы равно трем, а суммарное число степеней свободы - соответственно шести.
Если атомы в молекуле связаны не жесткой, а упругой связью, то кроме вращательных, появляются еще и колебательные степени свободы, наличие которых необходимо учитывать при описании свойств многоатомного газа, состоящего из таких молекул.
В одноатомном газе молекула имеет три степени свободы, соответствующие трем пространственным координатам. Вследствие равноправности этих координат, можно сделать предположение, что на каждую степень свободы молекулы одноатомного газа приходится в среднем кинетическая энергия, равная ![]()
![]() .
.
В случае многоатомного газа распределение энергии по степеням свободы его молекул подчиняется закону равнораспределения энергии по степеням свободы, который гласит: средняя кинетическая энергия, приходящаяся при тепловом равновесии на одну степень свободы молекулы равна ![]()
![]() .
.
Таким образом, в самом общем случае для определения суммарной кинетической энергии всех молекул газа ![]()
![]() (внутренней энергии идеального газа) необходимо использовать формулу:
(внутренней энергии идеального газа) необходимо использовать формулу:

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51 |




