или
![]() . (3.33)
. (3.33)
Отсюда следует:
![]() . (3.34)
. (3.34)
Интегрирование этого уравнения позволяет получить формулу:
![]() . (3.35)
. (3.35)
которая называется уравнением Пуассона в честь французского механика, математика и физика Симеона Дени Пуассона (1781 - 1840). Это уравнение адиабатического процесса для идеального газа, или адиабаты - кривой, описываемой этим уравнением в переменных P и V.
С помощью уравнения Клапейрона-Менделеева уравнение (3.37) можно переписать, используя другие параметры состояния идеального газа:
![]() , (3.36)
, (3.36)
![]() (3.37)
(3.37)
Сравнивая уравнение Пуассона (3.35) с уравнением Бойля-Мариотта: ![]() , можно убедиться, что адиабата (1) идеального газа, построенная в координатах P и V, всегда идёт круче изотермы (2).
, можно убедиться, что адиабата (1) идеального газа, построенная в координатах P и V, всегда идёт круче изотермы (2).
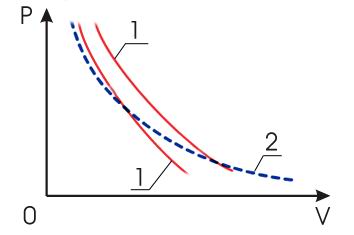
Рис.3.6
Это связано с тем, что, показатель адиабаты для газов всегда больше единицы и принимает наибольшее значение для одноатомных газов. Поэтому самую крутую адиабату имеют инертные газы, молекулы которых состоят из одного атома.
Поскольку адиабата пересекает все изотермы данной термодинамической системы, возможен адиабатический переход с одной изотермы на другую, путём сжатия или разрежения газа. А посредством изотермического изменения объёма возможен переход с одной адиабаты на другую.
Работу идеального газа в адиабатическом процессе можно определить с помощью выражения (3.24) Интегрирование этого выражения дает:
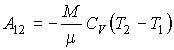 (3.38)
(3.38)
где: T1 и T2- температуры газа в начале и в конце процесса соответственно. В данном случае работа при переходе из одного состояния системы в другое определяется только функцией состояния системы ![]() , так как путь перехода однозначно задан уравнением Пуассона.
, так как путь перехода однозначно задан уравнением Пуассона.
Молярная теплоемкость газа CV может быть выражена через показатель адиабаты ![]()
![]() . Подстановка в формулу (3.30) соотношения Майера для теплоемкостей приводит её к виду:
. Подстановка в формулу (3.30) соотношения Майера для теплоемкостей приводит её к виду:
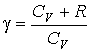 , (3.39)
, (3.39)
из которого следует искомое выражение:
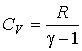 . (3.40)
. (3.40)
С учетом этой формулы выражение (3.38) может быть представлено в форме:
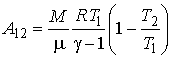 . (3.41)
. (3.41)
На основании уравнения адиабаты (3.36) запишем соотношение между температурами и объемами газа в начальном и конечном состояниях:
![]() (3.42)
(3.42)
или
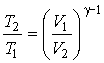 (3.43)
(3.43)
Подстановка этой формулы в выражение (3.41) дает:
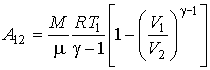 (3.44)
(3.44)
или с учетом уравнения Клапейрона-Менделеева:
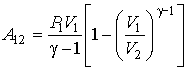 (3.45)
(3.45)
Формула (3.45) может быть получена и непосредственно интегрированием при подстановке в него уравнения Пуассона (3.35), записанного для произвольной точки адиабаты:
![]() (3.46)
(3.46)
Тогда имеем
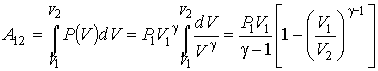 (3.47)
(3.47)
Адиабатический процесс может быть реализован в газе либо путём его термоизоляции, либо за счёт быстрого протекания процесса, когда процесс теплопередачи не успевает произойти. Первый способ применялся в опытах Джоуля, описанных выше, где было принципиально необходимо достижение газом состояния, близкого к равновесному. Поэтому каждый из опытов требовал продолжительного времени (около часа) и возникала необходимость введения поправок на тепловые потери.
Примером быстропротекающего процесса является распространение звука в воздухе. Несмотря на то, что такой процесс нельзя считать равновесным, опыт
показывает, что для его описания возможно применение уравнения Пуассона, полученного в рамках равновесной термодинамики.
В 1816 году, за семь лет до вывода Пуассоном уравнения адиабатического процесса, Пьером Симоном Лапласом (1749 - 1827) была получена формула для скорости распространения звука в газе:
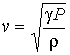 ,
,
где: P и ![]()
![]() - давление и плотность газа. Измерения значений v, P и
- давление и плотность газа. Измерения значений v, P и ![]()
![]() позволяют по этой формуле рассчитать значение показателя адиабаты
позволяют по этой формуле рассчитать значение показателя адиабаты ![]()
![]() . Для воздуха это значение близко к 1,4, что указывает на возможность с хорошей точностью считать его состоящим из двухатомных молекул.
. Для воздуха это значение близко к 1,4, что указывает на возможность с хорошей точностью считать его состоящим из двухатомных молекул.
Экспериментальное определение молярных теплоёмкостей CV и CP для реальных газов представляет собой довольно сложную задачу. Большой вклад в её решение внёс (1810 - 1878), под руководством которого были измерены молярные теплоёмкости многих веществ, в том числе газов. Исследования проводились в лаборатории при Сервской фарфоровой мануфактуре и носили прикладной характер, связанный с совершенствованием тепловых машин. Некоторыми из методик, разработанных Ренье, впоследствии воспользовался Джоуль при проведении своих опытов.
Важным классом термодинамических процессов являются процессы, происходящие при постоянной теплоемкости, то есть политропические процессы. К таким процессам, в частности, относятся адиабатический, изотермический, изобарический и изохорический процессы.
Для идеального газа нетрудно получить уравнение политропического процесса тем же способом, которым ранее было выведено уравнение Пуассона.
Пусть молярная теплоёмкость идеального газа в политропическом процессе равна С. Тогда в соответствии с первым началом термодинамики имеем выражение:
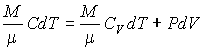 , (3.48)
, (3.48)
из которого следует:
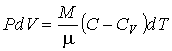 (3.49)
(3.49)

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51 |




