Подставляя это выражение в формулу (3.26) получим:
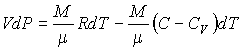 (3.50)
(3.50)
или с учетом соотношения Майера:
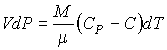 (3.51)
(3.51)
Сравнение формул (3.21) и (3.23) при условии, что ![]()
![]() , позволяет записать уравнение:
, позволяет записать уравнение:
![]() , (3.52)
, (3.52)
Здесь введен параметр:
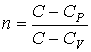 , (3.53)
, (3.53)
который называется показателем политропы.
Из этой формулы можно также получить зависимость молярной теплоемкости C от показателя политропы n:
![]() . (3.54)
. (3.54)
Преобразование формулы (3.52) к виду:
![]() (3.55)
(3.55)
и интегрирование полученного уравнения дает:
![]() (3.56)
(3.56)
Уравнение (3.56) называется уравнением политропического процесса или политропы – кривой, описываемой таким уравнением в переменных ![]() и
и ![]() .
.
Аналогично уравнениям адиабаты (3.36) и (3.37) уравнение политропы может быть переписано в других термодинамических координатах:
![]() , (3.57)
, (3.57)
![]() (3.58)
(3.58)
При адиабатическом процессе ![]()
![]() , что соответствует нулевой теплоемкости. Подставив C=0 в формулу (3.53) и сравнив получившееся выражение с (3.3), имеем
, что соответствует нулевой теплоемкости. Подставив C=0 в формулу (3.53) и сравнив получившееся выражение с (3.3), имеем ![]()
![]() , и уравнение политропы (3.56) становится уравнением адиабаты:
, и уравнение политропы (3.56) становится уравнением адиабаты:
![]() .
.
Если процесс изотермический, то ![]()
![]() , так как при этом dT
, так как при этом dT![]()
![]() . В этом случае показатель политропы n в пределе равен единице, и уравнение политропы (3.56) преобразуется в уравнение Бойля-Мариотта: PV=const. Обратим внимание на то, что поскольку при выводе уравнения политропы мы исключали величину dT, то этот вывод не может считаться полностью корректным для изотермического процесса.
. В этом случае показатель политропы n в пределе равен единице, и уравнение политропы (3.56) преобразуется в уравнение Бойля-Мариотта: PV=const. Обратим внимание на то, что поскольку при выводе уравнения политропы мы исключали величину dT, то этот вывод не может считаться полностью корректным для изотермического процесса.
Для изобарического процесса при C=CP показатель политропы n=0, и уравнение (3.56) принимает форму: P=const.
При изохорическом процессе C должно стать равным CV, что соответствует случаю, когда показатель ![]()
![]() . Очевидно, переход в формуле (3.56) к указанному пределу некорректен. Это связано с тем, что при выводе уравнения политропы предполагалось, что
. Очевидно, переход в формуле (3.56) к указанному пределу некорректен. Это связано с тем, что при выводе уравнения политропы предполагалось, что ![]()
![]() .
.
Если умножить уравнение (3.23) на величину (C-CP) и сложить его с уравнением (3.51) предварительно умноженным на величину (C-CV), то получим уравнение политропы в дифференциальном виде:
![]() . (3.59)
. (3.59)
При C=CV это уравнение приобретает форме:
![]() (3.60)
(3.60)
Отсюда имеем: dV=0 или V=const. Из уравнения (3.59) также следует, что в процессе, при котором C = CP, давление постоянно: P=const.
Для политропических процессов значение теплоёмкости и, соответственно, показателя политропы могут принимать любые величины. Отрицательные значения теплоёмкости соответствуют таким условиям, при которых внутренняя энергия термодинамической системы убывает при передаче ей положительного количества теплоты. Это может быть осуществлено при принудительном расширении газа.
В соответствии с формулой (3.49) при C < CV величины dV и dT имеют различные знаки, и с ростом объёма газа его температура, а, следовательно, и внутренняя энергия, уменьшаются. С этим, в частности, связано понижение температуры идеального газа при его адиабатическом расширении, так как в этом процессе C=0. Наоборот, при C > CV с ростом объёма газа его температура растёт. В соответствии с первым началом термодинамики этот рост должен быть обеспечен подводом к системе дополнительного количества теплоты.
Рассуждая аналогичным образом, можно на основании формулы (3.51) установить связь между приращениями давления и температуры. При C < CP с ростом давления температура газа будет возрастать, а при C>CP - уменьшаться.
Работа газа в политропическом процессе может быть определена с помощью действий, подобных проведенным при расчете работы в адиабатическом процессе:
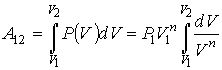 (3.61)
(3.61)
Интегрирование выражения (3.61) приводит к записи следующей формулы для определения работы в политропическом процессе:
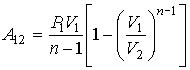 , (3.62)
, (3.62)
где: P1 и V1 - начальные давление и объём газа, V2 - его конечный объём.
Из этой формулы, в частности, следует, что работа при расширении газа всегда остаётся положительной, независимо от того, какое значение принимает показатель политропы - больше или меньше единицы.
Нетрудно видеть, что для адиабатического процесса при ![]()
![]() выражение (3.62) переходит в формулу (3.63). Для изобарического процесса, при n=0, выражение (3.36) дает:
выражение (3.62) переходит в формулу (3.63). Для изобарического процесса, при n=0, выражение (3.36) дает:
![]() , (3.63)
, (3.63)
где учтено, что при этом процессе P1= P2=P=const.
Формула (3.62) неприменима для описания изохорического процесса, так как при выводе уравнения политропы (3.52) исключался случай C=CV. Но из формулы (3.31) очевидно, что работа газа в изохорическом процессе равна нулю.
Другим процессом, не описывающимся соотношением (3.62), является изотермический процесс. Как было сказано выше, он является предельным случаем политропического процесса при ![]() . Работу в изотермическом процессе можно найти, если в формулу (3.61) в соответствии с законом Бойля-Мариотта подставить n=1, а затем выполнить интегрирование. Тогда будем иметь:
. Работу в изотермическом процессе можно найти, если в формулу (3.61) в соответствии с законом Бойля-Мариотта подставить n=1, а затем выполнить интегрирование. Тогда будем иметь:
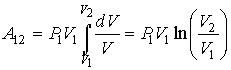 (3.64)
(3.64)

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51 |




