Они различные для различных веществ и обычно приведены в таблице (см. при решении задач!). Итак, при соответствующем изменении параметров состояния вещество испытывает фазовый переход (например, газ - жидкость).
Особенности поведения газов при повышенных давлениях и фазовый переход газ - жидкость не описываются уравнением состояния идеального газа (уравнением Клапейрона).
Для уточнения уравнения состояния, видимо, надо отказаться от представления о молекулах как материальных точках, а также от предположения, что отсутствует взаимодействие между молекулами. Т. е. считать газ реальным.
Такие поправки о конечных размерах молекул, о наличии сил взаимодействия между ними были предложены в 1873 г. Ван-дер-Ваальсом, соответствующее уравнение состояния названо его именем.
Предложенное уравнение состояния реального газа, как и другие (их более 200 разных уравнений), тоже приближенные. Еще и потому, что не существует пока способа точного вычисления сил взаимодействия между молекулами.
Положим, имеется 1 моль газа (![]() = 1 моль).
= 1 моль).
В уравнении: ![]() подразумевается, что V – объем сосуда с газом.
подразумевается, что V – объем сосуда с газом.
Но не весь объем сосуда находится в распоряжении молекул, т. к. каждая молекула сама занимает определенную часть объема сосуда, и эта часть объема недоступна для остальных молекул. Т. е. можно внести поправку и записать :
![]()
Здесь b – предельный объем, который занял бы газ при бесконечно большом давлении. Расчеты показывают: величина ![]() - учетверенному объему всех N молекул газа (
- учетверенному объему всех N молекул газа (![]() ), где r-радиус молекулы – «сферы».
), где r-радиус молекулы – «сферы».
«![]() » учитывает таким образом действие сил отталкивания (молекула «сохраняет свой размер»).
» учитывает таким образом действие сил отталкивания (молекула «сохраняет свой размер»).
Кроме сил отталкивания между молекулами действуют силы притяжения, которые приводят к тому, что давление молекул газа на любую площадку (стенки сосуда) будет при прочих равных условиях меньше, чем в случае идеального газа. Ведь любая молекула, находящаяся вблизи стенки сосуда, с одной стороны имеет больше «соседей», чем с другой, и поэтому испытывает результирующую силу со стороны остальных молекул, направленную внутрь газа. Т. О. давление на стенку сосуда станет меньше на величину ![]() :
:
![]()
или
![]()
Силы притяжения между молекулами стремятся «сблизить» их между собой. Но точно так же действует и внешнее давление р.
УМКД 042-18-38.1.11/01-2013 | Редакция № 1 от «11сентября»2013 г. | Страница 103 из 155 |
Давление, которое испытывает пристенный слой со стороны молекул газа, равно силе, действующей на все молекулы на единице поверхности слоя. Очевидно, эта сила пропорциональна плотности размещения (концентрации) молекул n. С другой стороны, число молекул в пристенном слое, испытывающих силу притяжения, тоже пропорционально n.
Следовательно, ![]() , а так как
, а так как ![]() (обратно пропорционально объему, занимаемому молем газа), то
(обратно пропорционально объему, занимаемому молем газа), то ![]() ,
,
здесь Vм – морлярный объем газа, а – коэффициент пропорциональности (зависит от характера сил притяжения между молекулами).
Поправка ![]() - учитывает действие сил притяжения между молекулами.
- учитывает действие сил притяжения между молекулами.
Итак, уравнение можно переписать:
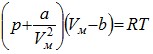 (6.1)
(6.1)
- уравнение Ван-дер-Ваальса для 1 моля реального газа
Для произвольного количества газа (имея в виду: 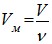 ) уравнение будет иметь вид:
) уравнение будет иметь вид: 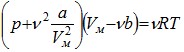 , где
, где ![]()
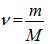 , m – масса газа, М – молярная масса газа, V – объем, занимаемый газом; а, b – поправки Ван-дер-Ваальса, приведены в справочных таблицах (а, Н?м4/моль2; b, м3/моль).
, m – масса газа, М – молярная масса газа, V – объем, занимаемый газом; а, b – поправки Ван-дер-Ваальса, приведены в справочных таблицах (а, Н?м4/моль2; b, м3/моль).
Уравнение Ван-дер-Ваальса можно переписать в виде:
![]()
или
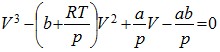
Уравнение имеет три корня, т. е. при одном и том же р, Т могут быть три значения объема, либо три значения плотности.
Для выяснения смысла корней уравнения удобно рассмотреть изотермы (изотермы Ван-дер-Ваальса), т. е зависимость р(V) при Т=const и сравнить их с опытными изотермами. Значению
р
p1
УМКД 042-18-38.1.11/01-2013 | Редакция № 1 от «11сентября»2013 г. | Страница 104 из 155 |
V
V1 V2 V3
Значению V1 соответствует жидкое состояние, V3 – газообразное. Смысл V2 надо выяснить.

Участки 3с и а4 изотермы Ван-дер-Ваальса совпадают (качественно!) с участками опытной изотермы. При этом 3с – газ, а4 – жидкость. Состояния, отвечающие участку 1b2 не могут существовать, т. к. с увеличением р не может V уменьшаться, такие «странные» свойства должны быть, по меньшей мере, крайне неустойчивыми. Состояния, соответствующие участкам с2 и а1, могут реализовываться при особых условиях, хотя они менее устойчивы, чем состояния участка abc. Состояние вещества, соответствующее кривой с2, газообразное, т. к. с2 является продолжением ветви изотермы 3с. Но давление газа (пара) в любом из этих состояний выше рн при той же температуре, что противоестественно. Это своеобразное состояние вещества может наблюдаться при быстром охлаждении закрытого сосуда, например, с воздухом, содержащим водяные пары. Только воздух должен быть тщательно очищен от следов пыли, от электрических зарядов (т. е. любой «грязи»). При этих условиях, несмотря на охлаждение, т. е. уменьшение упругости насыщенных паров воды, пар длительное время не конденсируется. Это состояние пересыщенного (переохлажденного)пара. В конце концов на стенках сосуда все-таки появятся капли воды, т. е. пересыщенный пар распадается на воду и насыщенный пар при данной более низкой температуре. Состояния участка а1 практически ещё труднее реализовать из-за их малой устойчивости. Эти состояния называют перегретой жидкостью (но эта жидкость в закрытом сосуде). Состояния участков с2 и а1. в отличие от нестабильных состояний участка 1b2, называются метастабильными.
Итак, состояния, отвечающие V2, не наблюдаются в опыте из-за их нестабильности. Участок изотермы abc – это состояние пара, находящегося в равновесии с жидкостью, т. е. двухфазное состояние. С увеличением Т положение изотерм изменяется (они располагаются выше), при этом максимумы и минимумы сближаются (по вертикали и по горизонтали). Наконец, при определенной температуре Т сливаются и вырождаются в точку перегиба. Т. е. при повышении Т уменьшается различие между тремя корнями уравнения Ван-дер-Ваальса.
При Т=Тк все три значения V «сливаются». Из уравнения Ван-дер-Ваальса можно получить значения критических параметров через константы «а» и «b»:
УМКД 042-18-38.1.11/01-2013 | Редакция № 1 от «11сентября»2013 г. | Страница 103 из 155 |
![]() ;
; ![]() ;
; ![]() .
.
Уравнение Ван-дер-Ваальса является лишь приближенно верным, оно пригодно лишь для довольно грубых количественных оценок соотношений между параметрами, определяющими состояние реального вещества. Лучшее совпадение с опытом достигается в них введением большего числа постоянных. Хотя физический смысл их не столь ясен, как в уравнении Ван-дер-Ваальса.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51 |




