Рис. 4.6
Применительно к рассматриваемой тепловой машине неравенство (4.24) может быть записано в виде:
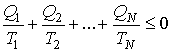 , (4.25)
, (4.25)
или
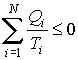 . (4.26)
. (4.26)
Величина ![]()
![]() называется приведенным количеством теплоты, которое численно равно количеству теплоты, полученной системой, при абсолютной температуре
называется приведенным количеством теплоты, которое численно равно количеству теплоты, полученной системой, при абсолютной температуре ![]() , деленной на эту температуру.
, деленной на эту температуру.
При переходе к бесконечному числу тепловых резервуаров, с которыми рабочее тело тепловой машины обменивается теплотой, суммирование в формуле (4.26) может быть заменено интегрированием по замкнутому термодинамическому циклу:
![]() . (4.27)
. (4.27)
Из этой формулы следует, что сумма приведенных количеств теплоты на замкнутом цикле для любой термодинамической системы не может быть больше нуля. Неравенство (4.27) было получено в 1862 году Клаузиусом и носит его имя.
Неравенство Клаузиуса (4.27) позволяет отличать обратимые и необратимые круговые термодинамические процессы. В случае, если термодинамический цикл состоит только из обратимых процессов, неравенство (4.27) переходит в равенство Клаузиуса:
![]() , (4.28)
, (4.28)
УМКД 042-18-38.1.11/01-2013 | Редакция № 1 от «11сентября»2013 г. | Страница 79 из 155 |
имеющее принципиальное значение для построения равновесной термодинамики.
Случай строгого неравенства в формуле (4.27) соответствует описанию необратимых круговых термодинамических процессов, и это выражение применяется в неравновесной термодинамике.
Неравенство Клаузиуса говорит о том, что энтропия изолированной системы не может убывать. С другой стороны, если систему предоставить самой себе, то она будет переходить из состояний менее вероятных в состояния более вероятные. Попав в наиболее вероятное состояние, система будет пребывать в нем наиболее долго. Если у нескольких состояний системы вероятность одинаково максимальная, то система будет переходить из одного максимально вероятного состояния в другое максимально вероятное состояние и обратно. Следовательно, энтропия и вероятность ведут себя сходным образом: они либо возрастают, либо остаются неизменными. Можно предположить, что между энтропией и вероятностью существует определенная связь. Больцман установил («принцип Больцмана»), что энтропия равна:
![]() ,
,
где k – постоянная Больцмана, ? – термодинамическая вероятность состояния системы – число способов, которыми может быть реализовано данное состояние макросистемы (число микросостояний, осуществляющих данное макросостояние, или статистический вес данного макросостояния).
Термодинамическая вероятность ? ? 1, в отличие от математической вероятности, которая меньше или равна 1.
Третье начало термодинамики (теорема Нернста) — физический принцип, определяющий поведение энтропии при приближении температуры к абсолютному нулю. Является одним из постулатов термодинамики, принимаемым на основе обобщения значительного количества экспериментальных данных.
Третье начало термодинамики может быть сформулировано так:
«Приращение энтропии при абсолютном нуле температуры стремится к конечному пределу, не зависящему от того, в каком равновесном состоянии находится система».
![]()
или
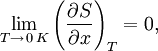
где x — любой термодинамический параметр.
Третье начало термодинамики относится только к равновесным состояниям.
Поскольку на основе второго начала термодинамики энтропию можно определить только с точностью до произвольной аддитивной постоянной (то есть, определяется не сама энтропия, а только её изменение):
![]() ,
,
третье начало термодинамики может быть использовано для точного определения энтропии. При этом энтропию равновесной системы при абсолютном нуле температуры считают равной нулю.
УМКД 042-18-38.1.11/01-2013 | Редакция № 1 от «11сентября»2013 г. | Страница 80из 155 |
Третье начало термодинамики позволяет находить абсолютное значение энтропии, что нельзя сделать в рамках классической термодинамики (на основе первого и второго начал термодинамики). В классической термодинамике энтропия может быть определена лишь с точностью до произвольной аддитивной постоянной S0, что не мешает термодинамическим исследованиям, так как реально измеряется разность энтропий (S0) в различных состояниях. Согласно третьему началу термодинамики, при ![]() значение
значение ![]() .
.
В 1911 году Макс Планк сформулировал третье начало термодинамики, как условие обращения в нуль энтропии всех тел при стремлении температуры к абсолютному нулю: ![]() . Отсюда S0 = 0, что даёт возможность определять абсолютное значения энтропии и других термодинамических потенциалов. Формулировка Планка соответствует определению энтропии в статистической физике через термодинамическую вероятность (W) состояния системы S = klnW. При абсолютном нуле температуры система находится в основном квантово-механическом состоянии. Если оно невырожденно, то W = 1 (состояние реализуется единственным микрораспределением) и энтропия S при
. Отсюда S0 = 0, что даёт возможность определять абсолютное значения энтропии и других термодинамических потенциалов. Формулировка Планка соответствует определению энтропии в статистической физике через термодинамическую вероятность (W) состояния системы S = klnW. При абсолютном нуле температуры система находится в основном квантово-механическом состоянии. Если оно невырожденно, то W = 1 (состояние реализуется единственным микрораспределением) и энтропия S при ![]() равна нулю. В действительности при всех измерениях стремление энтропии к нулю начинает проявляться значительно раньше, чем могут стать существенными дискретность квантовых уровней макроскопической системы и влияние квантового вырождения.
равна нулю. В действительности при всех измерениях стремление энтропии к нулю начинает проявляться значительно раньше, чем могут стать существенными дискретность квантовых уровней макроскопической системы и влияние квантового вырождения.
Из третьего начала термодинамики следует, что абсолютного нуля температуры нельзя достичь ни в каком конечном процессе, связанном с изменением энтропии, к нему можно лишь асимптотически приближаться, поэтому третье начало термодинамики иногда формулируют как принцип недостижимости абсолютного нуля температуры.
Из третьего начала термодинамики вытекает ряд термодинамических следствий: при ![]() должны стремиться к нулю теплоёмкости при постоянном давлении и при постоянном объёме, коэффициенты теплового расширения и некоторые аналогичные величины. Справедливость третьего начала термодинамики одно время подвергалась сомнению, но позже было выяснено, что все кажущиеся противоречия (ненулевое значение энтропии у ряда веществ при T= 0) связаны с метастабильными состояниями вещества, которые нельзя считать термодинамически равновесными.
должны стремиться к нулю теплоёмкости при постоянном давлении и при постоянном объёме, коэффициенты теплового расширения и некоторые аналогичные величины. Справедливость третьего начала термодинамики одно время подвергалась сомнению, но позже было выяснено, что все кажущиеся противоречия (ненулевое значение энтропии у ряда веществ при T= 0) связаны с метастабильными состояниями вещества, которые нельзя считать термодинамически равновесными.
Третье начало термодинамики часто нарушается в модельных системах. Так, при ![]() энтропия классического идеального газа стремится к минус бесконечности. Это говорит о том, что при низких температурах уравнение Менделеева — Клапейрона неадекватно описывает поведение реальных газов.
энтропия классического идеального газа стремится к минус бесконечности. Это говорит о том, что при низких температурах уравнение Менделеева — Клапейрона неадекватно описывает поведение реальных газов.
Таким образом, третье начало термодинамики указывает на недостаточность классической механики и статистики и является макроскопическим проявлением квантовых свойств реальных систем.
В квантовой механике, тем не менее, в модельных системах третье начало также может нарушаться. Таковы все случаи, когда применяется распределение Гиббса и основное состояние является вырожденным.
Несоблюдение третьего начала в модели, однако, не исключает того, что в каком-то диапазоне изменения физических величин эта модель может быть вполне адекватна.
УМКД 042-18-38.1.11/01-2013 | Редакция № 1 от «11сентября»2013 г. | Страница 81 из 155 |
5. Процессы переноса
5.1 Основные газокинетические понятия. Физическая сущность процессов переноса вещества, импульса, энергии. Общее уравнение переноса
Средняя длина свободного пробега, эффективный диаметр молекул.
Равновесное состояние газа в молекулярно-кинетической теории рассматривается как состояние полной хаотичности движения молекул, распределение которых по скоростям подчиняется закону Максвелла.
Любое неравновесное состояние газа всегда связано с нарушением полной хаотичности движения и максвелловского распределения молекул по скоростям. Основной особенностью неравновесных состояний является стремление газа самопроизвольно переходить к равновесному состоянию. Это обусловлено хаотическим тепловым движением молекул с непрерывными столкновениями их друг с другом, которое и приводит к постоянному перемешиванию молекул, изменению их скоростей и энергии. Установление в газе максвелловского распределения молекул по скоростям при переходе его в равновесное состояние всегда связано с направленным переносом массы, импульса и энергии. Процессы переноса массы, импульса и энергии в газе называют явлениями переноса.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51 |




