Несколько иначе был организован эксперимент по определению распределения по скоростям для атомов цезия, выполненный в 1947г. немецким физиком-экспериментатором Иммануэлем Эстерманом (1900-1973) совместно с О. Симпсоном и Штерном. На рис.2.7. приведено схематическое изображение опыта Эстермана. Пучок атомов цезия вылетал через отверстие в печи 1 с
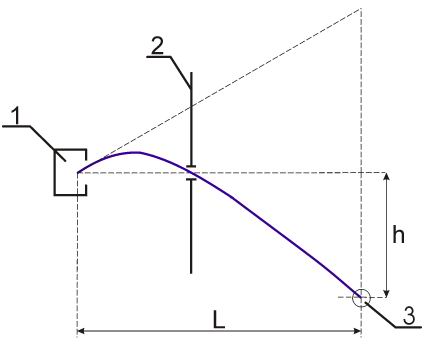
Рис.2.7
некоторой скоростью ![]() и под действием силы тяжести начинал двигаться по параболе. Атомы, прошедшие через узкую щель в диафрагме 2, улавливались детектором 3, который можно было располагать на различных высотах
и под действием силы тяжести начинал двигаться по параболе. Атомы, прошедшие через узкую щель в диафрагме 2, улавливались детектором 3, который можно было располагать на различных высотах ![]() .
.
Величина отклонения ![]() пучка в гравитационном поле Земли зависела от скорости атома. В этих опытах отклонение
пучка в гравитационном поле Земли зависела от скорости атома. В этих опытах отклонение ![]() составляло величину порядка нескольких долей миллиметра при расстоянии
составляло величину порядка нескольких долей миллиметра при расстоянии ![]() от печи до детектора равном 2 метрам. Перемещая датчик и регистрируя количество атомов цезия, попадающих в детектор за единицу времени, можно было построить зависимость интенсивности пучка от величины
от печи до детектора равном 2 метрам. Перемещая датчик и регистрируя количество атомов цезия, попадающих в детектор за единицу времени, можно было построить зависимость интенсивности пучка от величины ![]() . Последующий пересчет, с учетом известной зависимости высоты
. Последующий пересчет, с учетом известной зависимости высоты ![]() от скорости атома
от скорости атома ![]() , давал распределение по скоростям атомов цезия.
, давал распределение по скоростям атомов цезия.
Все проведенные эксперименты подтвердили справедливость полученного Максвеллом распределения по скоростям для атомных и молекулярных пучков.
В опытах (1911г.) Дюнуайе молекулярные пучки создавались путем испарения различных металлов, и поэтому молекулы исследуемых газов представляли собой атомы этих металлов. Такие эксперименты позволили проверить предсказания молекулярно-кинетической теории, которые она дает для случая газов, молекулы которых можно рассматривать как материальные точки, то есть для одноатомных газов.
Схема опыта Дюнуайе с молекулярными пучками показана на рис. 2.8. Стеклянный сосуд, материал которого выбирался таким, чтобы обеспечивать высокий вакуум, был разделён на три отделения 1, 2 и 3 двумя перегородками с диафрагмами 4. В отделении 1 находился газ, в качестве которого в данном эксперименте были использованы пары натрия, полученные при его нагревании. Молекулы этого газа могли свободно пролетать через отверстия в диафрагмах, коллимирующие молекулярный пучок 5, то есть позволяющие ему проходить только в пределах малого телесного угла. В отделениях 2 и 3 был создан сверхвысокий вакуум, такой, чтобы атомы натрия могли пролетать их без столкновений с молекулами воздуха.
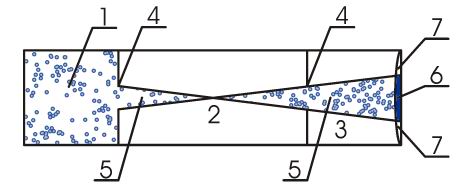
Рис.2.8
Нерассеянный молекулярный пучок оставлял на торцевой стенке сосуда след 6. Но даже в случае сверхвысокого вакуума имело место рассеяние молекулярного пучка на краях диафрагм 4. Поэтому на торцевой стенке сосуда имелась область "полутени" 7, в которой оставляли следы частицы, претерпевшие рассеяние. По мере ухудшения вакуума в отделении 3 область 7 увеличивалась. По величине
размытости следа рассеянных атомов натрия можно было оценить длину их свободного пробега. Такие оценки были проведены Максом Борном (1882 - 1970) на основании результатов опытов, аналогичных опыту Дюнуайе.
2.2 Барометрическая формула. Распределение Больцмана. Отрицательные абсолютные температуры
При статистическом описании распределения микрочастиц в пространстве координат x, y, и z обычно используется не функция распределения f(x, y,z), а концентрация n(x, y,z), которая определяется формулой:
![]() , (2.1)
, (2.1)
где N0 - полное число микрочастиц в объеме системы.
Введение концентрации n(x, y,z) микрочастиц в качестве основной функции при статистическом описании их распределения в пространстве связано с тем, что именно она обычно выступает непосредственно измеряемой величиной, а не функция распределения f(x, y,z), описывающая вероятность нахождения одной микрочастицы в той, или иной точке пространства.
Формула для нахождения среднего значения какой - либо функции ![]()
![]() при использовании концентрации n(x, y,z) имеет вид:
при использовании концентрации n(x, y,z) имеет вид:
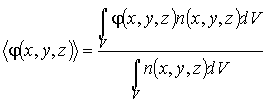 , (2.2)
, (2.2)
где ![]() - объем термодинамической системы.
- объем термодинамической системы.
Если на систему не действуют внешние силы, и она находится в состоянии термодинамического равновесия, то концентрация микрочастиц будет одинакова во всех точках системы: n(x, y,z)=const. В случае, когда на микрочастицы системы воздействует внешнее силовое поле, например, гравитационное, то их концентрация становится различной в разных точках пространства. При этом состояние термодинамического равновесия должно сохраняться.
Рассмотрим случай нахождения идеального газа во внешнем гравитационном поле. При нахождении концентрации молекул газа n(x, y,z) во внешнем поле будем исходить из предположения, что любой бесконечно малый объем газа находится в состоянии механического равновесия, а температура газа T во всех точках одинакова. Только при выполнении этих условий состояние газа можно считать равновесным, так как иначе в газе возникли бы потоки вещества и теплоты, что сделало бы состояние газа неравновесным.
Пусть гравитационное поле однородно, а ось Oz направлена вертикально вверх. Тогда концентрация молекул газа будет зависеть только от координаты ![]() : n=n(z). На рис. 2.1 схематически изображен бесконечно малый выделенный объем газа dV=dSdz, находящийся в равновесии. Снизу на этот выделенный объем газа воздействует давление P, а сверху - соответственно давление P+dP. Условие механического равновесия для объема газа dV=dSdz запишется в виде:
: n=n(z). На рис. 2.1 схематически изображен бесконечно малый выделенный объем газа dV=dSdz, находящийся в равновесии. Снизу на этот выделенный объем газа воздействует давление P, а сверху - соответственно давление P+dP. Условие механического равновесия для объема газа dV=dSdz запишется в виде:
![]() (2.3)
(2.3)
или
![]() , (2.4)
, (2.4)
где![]()
![]() - плотность газа, g - ускорение свободного падения, m - масса одной молекулы газа.
- плотность газа, g - ускорение свободного падения, m - масса одной молекулы газа.
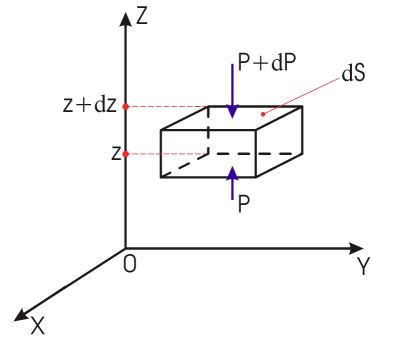
Рис. 2.1
Подстановка в формулу (2.4) выражения для плотности газа:
![]() , (2.5)
, (2.5)
которое является следствием основного уравнения молекулярно-кинетической теории:
![]() , (2.6)
, (2.6)
дает следующее уравнение для давления газа:
![]() . (2.7)
. (2.7)
Здесь к - постоянная Больцмана.
Интегрирование уравнения (2.7) при условии z=0: ![]()
![]() позволяет определить зависимость давления от высоты:
позволяет определить зависимость давления от высоты:
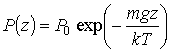 , (2.8)
, (2.8)
где P0 - давление газа на высоте, принятой за начало отсчета.
С учетом записанной ранее формулы для постоянной Больцмана:
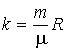 , (2.9)
, (2.9)
Где ![]()
![]() - молярная масса газа, выражение (2.8) можно представить в виде:
- молярная масса газа, выражение (2.8) можно представить в виде:

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51 |




