![]() (3.7)
(3.7)
Считая, что внутренняя энергия идеального газа пропорциональна количеству вещества:
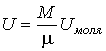 , (3.8)
, (3.8)
его теплоемкость в изохорическом процессе можно определить с помощью формулы:
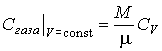 (3.9)
(3.9)
здесь: Uмоля - внутренняя энергия одного моля газа, а молярная теплоемкость при постоянном объем CV равна:
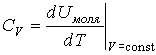 , (3.10)
, (3.10)
или, как обычно принято записывать в термодинамике
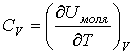 . (3.11)
. (3.11)
Символ V после закрывающей скобки указывает на то, что дифференцирование происходит при неизменном значении объема ![]() .
.
Ранее получено: кинетическая, а, следовательно, и внутренняя энергия идеального газа, линейно зависят от его температуры. Из этого следует, что молярная теплоемкость идеального газа в изохорическом процессе постоянна:CV=const, и не зависит от температуры идеального газа. Тогда выражение для его внутренней энергии с точностью до произвольной постоянной, которую обычно принимают равной нулю, можно записать в следующем виде:
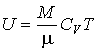 (3.12)
(3.12)
Из этого выражения следует, что внутренняя энергия идеального газа зависит только от его температуры и не зависит от других параметров его состояния, в частности от его объема.
Отсутствие зависимости внутренней энергии идеального газа от его объема было экспериментально подтверждёно в опытах Гей-Люссака и Джоуля, схема которых показана на рис. 3.3
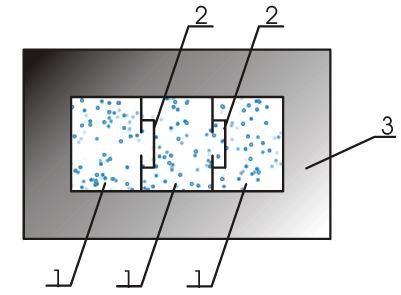
Рис.3.3
В опытах Гей-Люссака адиабатически изолированный жёсткий сосуд имел несколько отделений 1, разделённых перегородками 2, которые можно было медленно извлекать, причём трение в системе практически отсутствовало. В одном из отделений первоначально находился газ, который, по мере открывания перегородок постепенно заполнял другие отделения сосуда, причём каждый раз после открытия перегородки система приходила в состояние термодинамического равновесия. При этом процессе, так как сосуд был адиабатически изолированным, внутренняя энергия газа не изменялась. Опыты показали, что температура газа при этом также не изменяется. Это подтверждало независимость внутренней энергии идеального газа при постоянстве температуры от его объёма.
Опыты Джоуля являлись усовершенствованным продолжением опытов Гей-Люссака. Джоуль поместил сосуд в калориметр 3, и тем самым избавил себя от необходимости использовать адиабатически изолированный сосуд. Это дало возможность более тщательно добиваться установления термодинамического равновесия и повысить точность эксперимента. Температуру газа в сосудах Джоуль контролировал посредством измерения температуры воды в калориметре. Опыты Джоуля подтвердили, что внутренняя энергия идеального газа не зависит от занимаемого им объёма. Однако, дальнейшие более точные опыты Джоуля, проведённые им совместно с Томсоном (лордом Кельвином) показали, что если газ не является идеальным, его внутренняя энергия зависит от объёма, занимаемого им (эффект Джоуля-Томпсона).
Ранее была рассмотрена молекулярно-кинетическую модель идеального газа и получена зависимость кинетической энергии молекул газа от его температуры. Так как внутренняя энергия идеального газа с точностью до
произвольной постоянной равна кинетической энергии теплового движения его молекул, то для молярной теплоемкости такого газа можно записать:
![]() , (3.13)
, (3.13)
где число степеней свободы i зависит от физико-химической структуры молекулы газа.
Из формулы (3.13) следует, что для одноатомного газа молярная теплоемкость CV=![]()
![]() R, а для газа, молекулы которого состоят из двух жестко связанных атомов CV=
R, а для газа, молекулы которого состоят из двух жестко связанных атомов CV=![]()
![]() R. Соответственно для газов из жестких, многоатомных молекул CV=3R.
R. Соответственно для газов из жестких, многоатомных молекул CV=3R.
При использовании выражения (3.13) для практических расчетов реальных газов необходимо помнить, что оно является приближенным. Как указывалось в при обсуждении выражения для кинетической энергии многоатомного газа, существует зависимость количества учитываемых при расчете степеней свободы от температуры. Это приводит к тому, что при значительных изменениях температуры теплоемкость газа может существенно изменяться. Например, для молекул водорода, при температуре порядка 50 К вращательные степени свободы как бы "вымерзают" и его молярная теплоёмкость CV становится близкой к CV=![]()
![]() R. А при температурах порядка 300 - 400 К вращательные степени свободы "включаются" и его теплоёмкость CV приобретает значение CV=
R. А при температурах порядка 300 - 400 К вращательные степени свободы "включаются" и его теплоёмкость CV приобретает значение CV=![]()
![]() R. При дальнейшем, значительном по сравнению с комнатной, повышении температуры начинают проявляться колебательные степени свободы. Для двухатомного газа, например водорода, это приводит к увеличению энергии его молекулы на величину kT, и соответственно к возрастанию молярной теплоемкости на R. Поэтому при очень высоких температурах молярная теплоёмкость водорода стремится к значению CV=
R. При дальнейшем, значительном по сравнению с комнатной, повышении температуры начинают проявляться колебательные степени свободы. Для двухатомного газа, например водорода, это приводит к увеличению энергии его молекулы на величину kT, и соответственно к возрастанию молярной теплоемкости на R. Поэтому при очень высоких температурах молярная теплоёмкость водорода стремится к значению CV=![]()
![]() R.
R.
Теплоемкость идеального газа в процессе, происходящем с изменением объема, отличается от полученного выше выражения (3.13). Это связано с тем, что при изменении объема газа им совершается работа и, в соответствии с первым началом термодинамики, подведенная теплота и изменение внутренней энергии становятся не равными друг другу. При расширении газа часть подведенной теплоты затрачивается на совершение им работы.
Поэтому для произвольного политропического процесса при определении молярной теплоемкости необходимо вместо выражения (3.10) использовать формулу:
![]() , (3.14)
, (3.14)
где: ![]() - объем одного моля газа. Последнее слагаемое в числителе этой формулы описывает работу, совершенную одним молем газа в рассматриваемом процессе.
- объем одного моля газа. Последнее слагаемое в числителе этой формулы описывает работу, совершенную одним молем газа в рассматриваемом процессе.
Если процесс происходит при постоянном давлении, то с учетом выражения (3.10) имеем:
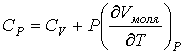 . (3.15)
. (3.15)
Использование уравнения Клапейрона-Менделеева, записанного для одного моля газа:
![]() , (3.16)
, (3.16)
дает:
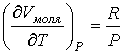 . (3.17)
. (3.17)
Тогда из выражения (3.15) следует формула для нахождения молярной теплоемкости при постоянном давлении:
![]() , (3.18)
, (3.18)
которая называется соотношением Майера, в честь Юлиуса Роберта Майера (1814 - 1878). Из этой формулы с учетом выражения (3.13) имеем:

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51 |




