Если форма поверхности несферическая, то ?Dр выражается через среднюю кривизну нормального сечения. Нормальным сечением поверхности называется линия пересечения поверхности плоскостью, проходящей через нормаль в данной точке. В геометрии доказывается, что полусумма обратных радиусов кривизны:
![]()
для любой пары взаимно перпендикулярных нормальных сечений имеет одно и то же значение. Эта величина и есть средняя кривизна поверхности в данной точке.
Радиусы R1 и R2 в формуле – алгебраические величины. Если центр кривизны нормального сечения находится под данной поверхностью, соответствующий радиус кривизны положителен; если центр кривизны лежит над поверхностью, радиус кривизны отрицателен. Неплоская поверхность может иметь среднюю кривизну, равную нулю. Для этого нужно, чтобы радиусы кривизны R1 и R2 были одинаковы по величине и противоположны по знаку.
УМКД 042-18-38.1.11/01-2013 | Редакция № 1 от «11сентября»2013 г. | Страница 116 из 155 |
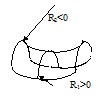
Рис.7.4
Для сферы Н=1/R, поэтому: ![]() .
.
Лаплас доказал, что эта формула справедлива для поверхности любой формы, если под Н понимать среднюю кривизну поверхности в той точке, под которой определяется дополнительное давление. Подставив сюда выражение для средней кривизны, получим формулу для добавочного давления под произвольной поверхностью:
![]()
Это формула Лапласа. Для сферической искривленной поверхности (R1=R2=R) это выражение переходит в![]() , для цилиндрической (R1=R, R2=?) – избыточное давление
, для цилиндрической (R1=R, R2=?) – избыточное давление ![]() . В случае плоской поверхности (R1=R2=?) силы поверхностного натяжения избыточного давления не создают.
. В случае плоской поверхности (R1=R2=?) силы поверхностного натяжения избыточного давления не создают.
Добавочное давление обуславливает изменение уровня жидкости в узких трубках (капилляр), вследствие чего оно еще называется капиллярным давлением.
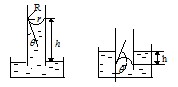
Изменение высоты уровня жидкости в узких трубках или зазорах получило название капиллярности. (Лат. capillus) означает волос. Капилляр – «трубка, тонкая, как волос»).
Если опустить капилляр в смачиваемую жидкость, то под действием лапласовского давления жидкость в нем поднимается. Между жидкостью в капилляре и широком сосуде устанавливается разность уровней h, при которой капиллярное (добавочное) давление уравновешивается гидростатическим:
![]() .
.
здесь R – радиус мениска. Выразим его через краевой угол ? и радиус капилляра r:
![]() .
.
УМКД 042-18-38.1.11/01-2013 | Редакция № 1 от «11сентября»2013 г. | Страница 117 из 155 |
Тогда высота поднятия жидкости в капилляре: ![]() .
.
Смачивающая жидкость (?q<?/2, cos ?q>0) поднимается по капилляру, и эта формула дает положительное значение h, а несмачивающая жидкость (?>?/2, cos ?<0) опускается по капилляру, и формула дает отрицательные значения h. Из полученного выражения видно, что высота поднятия (опускания) жидкости в капилляре обратно пропорциональна его радиусу. В тонких капиллярах жидкость поднимается достаточно высоко.
Рассмотрим поднятие смачивающей жидкости между двумя пластинами, разделенными узким зазором d. Если пластины параллельны, то мениск имеет цилиндрическую форму. Высота капиллярного подъема в этом случае также определяется из условия равенства лапласовского и гидростатического давлений.
Для цилиндрической поверхности R1=R - радиус цилиндра, R2=?Ґ, поэтому избыточное давление за счет искривления поверхности: ![]() , тогда высота капиллярного подъема в этом случае:
, тогда высота капиллярного подъема в этом случае:
![]() .
.
Капиллярные явления имеют большое значение в природе и технике. Например, влагообмен в почве и в растениях осуществляется за счет поднятия воды по тончайшим капиллярам. В капилляре переменного сечения капля смачиваемой жидкости под воздействием разности лапласовских давлений втягивается в сторону его утончения. Этим объясняется т. н. расклинивающее действие смачивающих жидкостей: жидкости, проникая в микротрещины, увеличивают их и тем самым понижают прочность твердых тел. На капиллярности основано действие фитилей, впитывание влаги бетоном и т. д.
8. Фазовые превращения
8.1 Фазовые превращения первого и второго рода. Диаграмма состояний трехфазной системы. Уравнение Клапейрона-Клаузиуса
Понятие фаза в термодинамике рассматривают в более широком смысле, чем агрегатные состояния. Под фазой в термодинамике понимают термодинамически равновесное состояние вещества, отличающееся по физическим свойствам от других возможных равновесных состояний того же вещества. Иногда неравновесное метастабильное состояние вещества также называют фазой, но метастабильной. Фазы вещества могут отличаться характером движения структурных частиц и наличием или отсутствием упорядоченной структуры. Различные кристаллические фазы могут отличаться друг от друга типом кристаллической структуры, электропроводностью, электрическими и магнитными свойствами и др. Жидкие фазы отличаются друг от друга концентрацией компонентов, наличием или отсутствием сверхпроводимости и т. п.
Переход вещества из одной фазы в другую называется фазовым переходом. К фазовым переходам относятся явления парообразования и плавления, конденсации и кристаллизации и др. В двухфазной системе фазы находятся в равновесии при одной и той же температуре. При увеличении объёма некоторая часть жидкости превращается в пар, но при этом для поддержания температуры неизменной необходимо извне передать некоторое количество теплоты. Таким образом, для осуществления перехода из жидкой фазы в газообразную системе необходимо передать теплоту без изменения температуры системы. Эта теплота идёт на изменение фазового состояния вещества и называется теплотой фазового превращения или скрытой теплотой перехода. С повышением температуры скрытая теплота перехода фиксированной массы вещества уменьшается, а при критической температуре она равна нулю. Для характеристики фазового перехода используют удельную теплоту фазового перехода. Удельной теплотой фазового перехода называется количество скрытой теплоты, приходящейся на единицу массы вещества.
УМКД 042-18-38.1.11/01-2013 | Редакция № 1 от «11сентября»2013 г. | Страница 118 из 155 |
Фазовые переходы с поглощением или выделением скрытой теплоты перехода называются фазовыми переходами первого рода. При этом внутренняя
энергия и плотность изменяются скачком. При переходе из более упорядоченного состояния в менее упорядоченное состояние энтропия увеличивается. Ниже в таблице приведены фазовые переходы первого рода и их основные характеристики.
Таблица.
Фазовый переход | Направление перехода | Скрытая теплота перехода | Изменение энтропии при фазовом переходе |
Парообразование | Жидкость ? пар |
LП – удельная теплота парообразования, т - масса жидкости, переведённой в пар. |
Энтропия возрастает ?SП >0 |
Конденсация | Пар ? жидкость |
LКОН – величина удельной теплоты конденсации, т - масса пара, переведённого в жидкость |
?Sкр < 0 |
Плавление | Твёрдое тело? жидкость |
LПЛ – удельная теплота плавления, т - масса твёрдого тела, переведённого в жидкость |
Энтропия возрастает ?Sпл > 0 |
Кристаллизация | Жидкость ? твёрдое тело |
LКР – величина удельной теплоты кристаллизации, т - масса жидкости, переведённой в твёрдое тело - кристалл |
?Sкр < 0 |
Сублимация (или возгонка) | Твёрдое тело ? Пар |
LС – удельная теплота сублимации, т - масса твёрдого тела, переведённого в пар |
?Sc > 0 |
Десублимация (Кристаллизация минуя жидкую фазу) | Пар ? твёрдое тело (минуя жидкую фазу) |
LКР – величина удельной теплоты кристаллизации, т - масса пара, переведённого в твёрдое тело - кристалл |
?Sкр < 0 |
Существует связь между давлением, при котором находится в равновесии двухфазная система, и температурой при фазовых переходах первого рода. Эта связь описывается уравнением Клапейрона – Клаузиуса. Рассмотрим вывод этого уравнения для закрытых систем. Если число частиц в системе постоянно, то изменение внутренней энергии, согласно первому началу термодинамики, определяется выражением: ![]() . Равновесие между фазами наступит при условии, что Т1 = Т2 и Р1 = Р2 . Рассмотрим бесконечно малый обратимый цикл Карно (рис.8.1), изотермы которого соответствуют состоянию двухфазной системы при температурах Т и dT. Поскольку параметры состояния при этом изменяются бесконечно мало, изотермы и адиабаты на рис.8.1 изображены прямыми. Давление в таком цикле изменяется на величину dP. Работа системы за цикл определяется формулой:
. Равновесие между фазами наступит при условии, что Т1 = Т2 и Р1 = Р2 . Рассмотрим бесконечно малый обратимый цикл Карно (рис.8.1), изотермы которого соответствуют состоянию двухфазной системы при температурах Т и dT. Поскольку параметры состояния при этом изменяются бесконечно мало, изотермы и адиабаты на рис.8.1 изображены прямыми. Давление в таком цикле изменяется на величину dP. Работа системы за цикл определяется формулой: ![]() . Предположим, что цикл реализован для системы масса вещества которой равна единице. Коэффициент полезного действия такого элементарного цикла Карно можно определить по формулам:
. Предположим, что цикл реализован для системы масса вещества которой равна единице. Коэффициент полезного действия такого элементарного цикла Карно можно определить по формулам: ![]() или
или ![]() , где LП – удельная теплота парообразования. Приравнивая правые части этих равенств, и подставив выражение работы через давление и объём, получим:
, где LП – удельная теплота парообразования. Приравнивая правые части этих равенств, и подставив выражение работы через давление и объём, получим: ![]() . Соотнесём изменение давления с изменением температуры и получим:
. Соотнесём изменение давления с изменением температуры и получим:

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51 |




