Решение.
Температуры и объемы газа, совершающего адиабатический процесс, связаны между собой соотношением
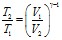 (1)
(1)
где ![]() — показатель адиабаты (для водорода как двухатомного газа
— показатель адиабаты (для водорода как двухатомного газа ![]() =1,4).
=1,4).
Отсюда получаем выражение для конечной температуры Т2:
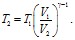 (2)
(2)
Подставляя численные значения заданных величин в (2), найдём
![]()
Работа А газа при адиабатическом расширении определяется в соответствии с известными формулами: ![]() (3)
(3)
УМКД 042-18-38.1.11/01-2013 | Редакция № 1 от «11сентября»2013 г. | Страница 129 из 155 |
Подставив в (3) численные значения величин, получим
![]() 29,8 кДж.
29,8 кДж.
Работа А2 газа при изотермическом сжатии выражается формулой
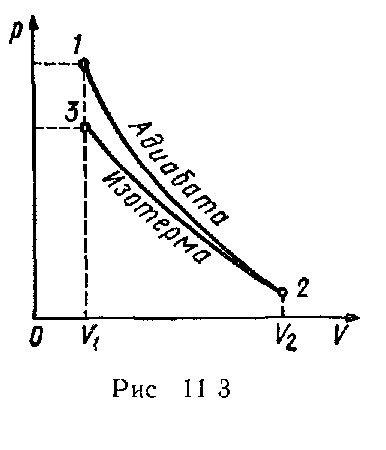
![]() (4.4.3.4)
(4.4.3.4)
Произведя вычисления по формуле (4), найдем А2= - 21 кДж.
Знак минус показывает, что при сжатии газа работа совершена внешними силами.
Общая работа, совершенная газом при рассмотренных выше процессах, равна
![]() 29,8 + (— 21) = 8,8 кДж.
29,8 + (— 21) = 8,8 кДж.
Решите задачи: (Сборник задач по курсу общей физики под ред. вып.1989г) №13-2,4,5,23,25,27,31,33
Тема: Второе начало термодинамики
Цель занятия: Научить расчету изменения энтропии в различных процессах в газе. Отработать навыки расчета КПД тепловых машин, работающих по разным циклам. Дать сравнительную оценку КПД машин. Закрепление основных понятий
Повторить теоретический материал по теме занятия и ответьте на следующие вопросы:
- что называют циклическим процессом?
- как рассчитывается работа, совершаемая газом за цикл?
- что называют тепловой машиной?
- как рассчитать кпд тепловой машины?
- из каких процессов составлен цикл карно?
- в чем суть теорем Карно?
- изобразите и объясните принципиальную схему охлаждения воздуха в камере домашнего холодильника.
- какие циклы тепловых машин вам известны, из каких процессов они составлены?
- что называют энтропией? Как её рассчитать?
- поясните следующее определение энтропии: «Энтропия есть мера неупорядоченности системы»
- каковы границы применимости первого и второго законов термодинамики?
-какими значениями свободной энергии и энтропии характеризуется термодинамическая система в равновесном состоянии?
УМКД 042-18-38.1.11/01-2013 | Редакция № 1 от «11сентября»2013 г. | Страница 130 из 155 |
- как можно доказать, что абсолютный нуль температуры недостижим?
- как изменяется энтропия в обратимых и необратимых процессах?
- в чем физический смысл неравенства Клаузиуса?
- как связаны энтропия системы и термодинамическая вероятность?
- что называют термодинамической вероятностью? как она определяется?
Рассмотрите примеры решения задач:
Задача 1. Найдите изменение ![]() S энтропии при нагревании воды массой
S энтропии при нагревании воды массой ![]() 100 г от температуры
100 г от температуры ![]() =0 °С до температуры t2= 100 °С и последующем превращении воды в пар той же температуры. Удельная теплоемкость воды равна 4200 Дж/(К•кг). Удельная теплота парообразования для воды равна 2,25•106 Дж/кг.
=0 °С до температуры t2= 100 °С и последующем превращении воды в пар той же температуры. Удельная теплоемкость воды равна 4200 Дж/(К•кг). Удельная теплота парообразования для воды равна 2,25•106 Дж/кг.
Решение.
Найдем отдельно изменение энтропии ![]() при нагревании воды и изменение энтропии
при нагревании воды и изменение энтропии ![]() при превращении ее в пар. Полное изменение энтропии выразится суммой
при превращении ее в пар. Полное изменение энтропии выразится суммой ![]() и
и ![]() .
.
Как известно, изменение энтропии выражается общей формулой
![]() (1)
(1)
При бесконечно малом изменении ![]() температуры нагреваемого тела затрачивается количество теплоты ?Q=mc•dT, где
температуры нагреваемого тела затрачивается количество теплоты ?Q=mc•dT, где ![]() - масса тела; с — его удельная теплоемкость. После подстановки величины ?Q в формулу для
- масса тела; с — его удельная теплоемкость. После подстановки величины ?Q в формулу для![]() , получим формулу для вычисления изменения энтропии при нагревании воды:
, получим формулу для вычисления изменения энтропии при нагревании воды:
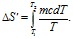 (2)
(2)
Вынесем за знак интеграла постоянные величины и произведем интегрирование, тогда получим
![]() (3)
(3)
После подстановки численных значений и вычислений найдем
![]() = 132 Дж/К.
= 132 Дж/К.
При вычислении изменения энтропии во время превращения воды в пар той же температуры (фазовый переход первого рода есть изотермический процесс) можно вынести за знак интеграла постоянную температуpу T. Тогда, вычислив интеграл, найдем
![]() (4)
(4)
где Q — количество теплоты, переданное при превращении нагретой воды в пар той же температуры.
Подставив в формулу (4) выражение для количества теплоты, необходимое для фазового перехода I рода (превращение воды в пар),
Q= ![]() , (5)
, (5)
где ![]() — удельная теплота парообразования, получим
— удельная теплота парообразования, получим
![]() (6)
(6)
Произведя вычисления по формуле (6), найдем: ![]() 605 Дж/К.
605 Дж/К.
УМКД 042-18-38.1.11/01-2013 | Редакция № 1 от «11сентября»2013 г. | Страница 131 из 155 |
Полное изменение энтропии при нагревании воды и последующем превращении ее в пар равно ![]() =737 Дж/К.
=737 Дж/К.
Задача 2. Определите изменение ![]() энтропии при изотермическом расширении кислорода массой
энтропии при изотермическом расширении кислорода массой ![]() =10 г от объема
=10 г от объема ![]() =25 л до объема
=25 л до объема ![]() = 100 л.
= 100 л.
Решение.
Так как процесс изотермический, то в общем выражении (4.5.17) для изменения энтропии
![]() (1)
(1)
температуру выносим за знак интеграла. Выполнив это, получим соотношение
![]() (2)
(2)

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51 |




