- Почему в задачах термодинамики предлагается чаще рассматривать процессы, как протекающие бесконечно медленно, хотя реальные процессы протекают с конечной скоростью?
- Какая из физических величин, входящих в формулу, выражающую I закон термодинамики, является функцией состояния, функцией процесса? Что это означает?
- При каком условии процесс в идеальном газе называют адиабатическим?
- Запишите уравнение адиабатического процесса
- При каком условии реально протекающие процессы можно считать адиабатическими?
- Как рассчитывается работа при адиабатическом процессе?
- Как записывается первый закон термодинамики применительно к адиабатическому процессу?
- Как изменяется температура газа при адиабатическом сжатии? при адиабатическом расширении?
- Какова теплоемкость газа в адиабатическом процессе?
- Какой процесс (при каком условии) называют политропным?
- Как определяется показатель политропы?
- Каков показатель политропы, если процесс в газе по своим свойствам близок к:
а) адиабатному; б) изотермическому; в) изохорному; г) изобарному?
- При каких значениях показателя политропы расширение двухатомного идеального газа осуществляется: а) с подводом тепла; б) с отводом тепла?
- Как найти удельную теплоемкость кислорода в политропном процессе?
Рассмотрите примеры решения задач:
Задача 1. Идеальный газ сжимают адиабатически. Получить для этого случая зависимость от давления средней длины свободного пробега и среднего числа соударений в единицу времени.
Решение
Используем выражение для средней длины свободного пробега: ![]() и
и
уравнение состояния идеального газа в виде: ![]() , тогда получаем:
, тогда получаем:
![]()
из уравнения адиабаты: ![]() , где
, где ![]()
В итоге получается: ![]() .
.
Аналогично, зная: ![]() , где
, где 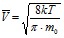 , получим:
, получим: ![]()
Задача 2 Для газовой смеси, состоящей из кислорода массой m1=1г и гелия массой m2=8г при температуре t = 27 ![]() найдите внутреннюю энергию U.
найдите внутреннюю энергию U.
Решение.
УМКД 042-18-38.1.11/01-2013 | Редакция № 1 от «11сентября»2013 г. | Страница 127 из 155 |
Кислород – двухатомный газ, при температуре t = 27 ![]() колебательные степени свободы не возбуждаются, поэтому число степеней свободы для кислорода i1=5. Гелий – одноатомный газ, число степеней свободы i2=3. Полная внутренняя энергия всего количества смеси равна в соответствии с формулой (4.1.37):
колебательные степени свободы не возбуждаются, поэтому число степеней свободы для кислорода i1=5. Гелий – одноатомный газ, число степеней свободы i2=3. Полная внутренняя энергия всего количества смеси равна в соответствии с формулой (4.1.37):
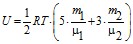 .
.
Проверка размерность внутренней энергии:
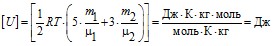
Представим размерность данных задачи в системе СИ и проведем расчет:
![]()
![]()
![]() .
.
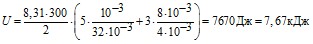
Задача 3. Кислород занимает объем ![]() =
=![]() и находится под давлением
и находится под давлением ![]() =200 кПа. Газ нагрели сначала при постоянном давлении до объема
=200 кПа. Газ нагрели сначала при постоянном давлении до объема ![]() =
=![]() , а затем при постоянном объеме до давления
, а затем при постоянном объеме до давления ![]() =500 кПа. Постройте график процесса и найдите: 1) изменение
=500 кПа. Постройте график процесса и найдите: 1) изменение ![]() U внутренней энергии газа; 2) совершенную газом работу А; 3) количество теплоты Q, переданное газу.
U внутренней энергии газа; 2) совершенную газом работу А; 3) количество теплоты Q, переданное газу.
Решение.
Построим график процесса (рис.1). На графике точками 1, 2, 3 обозначены состояния газа, характеризуемые параметрами ![]()
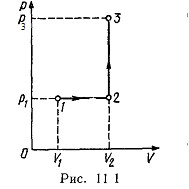
Рис. 1
Изменение внутренней энергии газа при переходе его из состояния 1 в состояние 3 выражается формулой
![]() U=
U=![]() • ?T, (1)
• ?T, (1)
где ![]() — молярная теплоемкость газа при постоянном объеме; m — масса газа; ?T — разность температур, соответствующих конечному З и начальному 1
— молярная теплоемкость газа при постоянном объеме; m — масса газа; ?T — разность температур, соответствующих конечному З и начальному 1![]() состояниям, т. е.
состояниям, т. е.![]()
УМКД 042-18-38.1.11/01-2013 | Редакция № 1 от «11сентября»2013 г. | Страница 128 из 155 |
Так как ![]() , (2)
, (2)
То ![]() . (3)
. (3)
Температуры ![]() и
и ![]() выразим из уравнения Менделеева— Клапейрона:
выразим из уравнения Менделеева— Клапейрона:
![]() (4)
(4)
С учетом (4.4.2.4) выражение (4.4.2.3) принимает вид:
![]() (5)
(5)
Подставим в (5) значения величин, учитывая, что для кислорода, как двухатомного газа, ![]() =5, и, произведя вычисления, получим:
=5, и, произведя вычисления, получим:
![]() =3,25 МДж.
=3,25 МДж.
Полная работа, совершаемая газом, равна А=![]() , где
, где ![]() — работа на участке 1—2;
— работа на участке 1—2; ![]() — работа на участке 2—3.
— работа на участке 2—3.
На участке 1—2 давление постоянно (p=const). Работа в этом случае выражается формулой ![]() .На участке 2—3 объем газа не изменяется и, следовательно, работа газа на этом участке равна нулю (
.На участке 2—3 объем газа не изменяется и, следовательно, работа газа на этом участке равна нулю (![]() =0). Таким образом,
=0). Таким образом,
A=![]() (6)
(6)
Подставив в формулу (6) численные значения физических величин и произведя вычисления, получим: а=0,4 МДж.
Согласно первому началу термодинамики количество теплоты Q, переданное газу, будет равно Q=![]() =3,65 МДж.
=3,65 МДж.
Задача 4. В цилиндре под поршнем находится водород массой ![]() =0,02 кг при температуре Т = З00 К. Водород начал расширяться адиабатически, увеличив свой объем в пять раз, а затем был сжат изотермически, причем объем газа уменьшился в пять раз. Найдите температуру Т2 в конце адиабатического расширения и работу А, совершенную газом. Изобразите процесс графически.
=0,02 кг при температуре Т = З00 К. Водород начал расширяться адиабатически, увеличив свой объем в пять раз, а затем был сжат изотермически, причем объем газа уменьшился в пять раз. Найдите температуру Т2 в конце адиабатического расширения и работу А, совершенную газом. Изобразите процесс графически.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51 |




