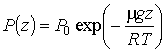 . (2.10)
. (2.10)
Эта зависимость носит название барометрической формулы. Она, в частности, позволяет рассчитывать зависимость давления атмосферы от высоты в случае, если температура атмосферы постоянна, а гравитационное поле - однородно. Для реальной атмосферы Земли на высотах примерно до 10 км её температура уменьшается в среднем на 6 К на 1 км подъема. Далее до высот
порядка 20 км температура остается практически постоянной, а выше - постепенно возрастает до ~ 270 К на высоте около 55 км. На этой высоте давление атмосферы становится уже меньше 0,001 от атмосферного давления на уровне моря.
Несмотря на указанную зависимость температуры атмосферы Земли от высоты, формула (2.10) позволяет достаточно точно определять высоту по результатам измерения давления, что нашло применение в приборах, предназначенных для определения высоты полета самолетов.
Подстановка уравнения состояния (2.6) в выражение (2.8) позволяет получить следующую зависимость концентрации молекул идеального газа от координаты ![]() :
:
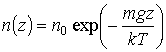 , (2.11)
, (2.11)
где n0 - концентрация газа при z=0.
Формула (2.11) была получена в предположении, что газ находится в однородном гравитационном поле и, следовательно, потенциальную энергию его молекулы в зависимости от координаты ![]() можно выразить простой формулой:
можно выразить простой формулой:
![]() . (2.12)
. (2.12)
Сопоставление формул (2.11) и (2.12) позволяет сделать вывод, что для однородного гравитационного поля распределение концентрации газа зависит от потенциальной энергии его молекул в этом поле. Считая, что данное утверждение справедливо для любого потенциального силового поля, потенциальная энергия молекул газа в котором описывается зависимостью ![]()
![]() , запишем выражение для определения концентрации молекул газа в виде:
, запишем выражение для определения концентрации молекул газа в виде:
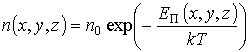 , (2.13)
, (2.13)
где n0 - концентрация газа в точке, соответствующей началу координат x=y=z=0 при условии, что ![]()
![]() =0.
=0.
Формула (2.13) была впервые получена в 1866 году Л. Больцманом и описывает распределение, получившее название распределения Больцмана.
Это распределение позволяет рассчитывать концентрацию газа, находящегося в равновесном состоянии во внешнем силовом поле. Причем это поле не должно быть обязательно гравитационным, а может иметь любое происхождение, в частности, быть электростатическим или полем сил инерции.
Анализ распределения Больцмана показывает, что концентрация молекул газа тем выше, чем меньше их потенциальная энергия. Кроме этого, с понижением температуры увеличивается отличие концентраций в точках с различными значениями потенциальной энергии молекул. А при стремлении температуры к абсолютному нулю, молекулы начинают скапливаться в месте, где их потенциальная энергия принимает наименьшее значение. Указанные особенности распределения Больцмана являются следствием теплового движения молекул, так как кинетическая энергия их поступательного движения в среднем равна ![]()
![]() и уменьшается пропорционально уменьшению температуры. А уменьшение кинетической энергии приводит к уменьшению количества молекул,
и уменьшается пропорционально уменьшению температуры. А уменьшение кинетической энергии приводит к уменьшению количества молекул,
способных преодолеть потенциальный порог, высота которого характеризуется величиной потенциальной энергии высотой ![]()
![]() .
.
Распределение Больцмана (5.21) было использовано французским физиком Жаном Батистом Перреном (1870 - 1942) при экспериментальном определения постоянной Больцмана k и постоянной Авогадро NA. В работах, выполненных Перреном в 1908-1911 годах, измерялось распределение концентрации микроскопических частиц во внешнем гравитационном поле. Отметим, что совокупность микрочастиц, находящихся во взвешенном состоянии в жидкости, близка по своей молекулярно-кинетической структуре к идеальному газу и может описываться газовыми законами. Это делает возможным при определении распределения микрочастиц во внешнем силовом поле использовать формулу Больцмана.
В соответствии с формулой (2.11) по мере подъема на высоту ![]() концентрация n(z) экспоненциально убывает. Перрен для экспериментального определения зависимости n(z) использовал микроскоп, глубина резкости объектива которого обеспечивала измерение положения микроскопических частиц в тонком слое эмульсии (толщиной около 100 мкм) с точностью до 1 мкм. Эмульсия представляла собой взвесь одинаковых сферических частиц специального древесного сока или смолы (гуммигута) в воде. Размер этих частиц в опытах Перрена достигал значения менее 0,4 мкм.
концентрация n(z) экспоненциально убывает. Перрен для экспериментального определения зависимости n(z) использовал микроскоп, глубина резкости объектива которого обеспечивала измерение положения микроскопических частиц в тонком слое эмульсии (толщиной около 100 мкм) с точностью до 1 мкм. Эмульсия представляла собой взвесь одинаковых сферических частиц специального древесного сока или смолы (гуммигута) в воде. Размер этих частиц в опытах Перрена достигал значения менее 0,4 мкм.
Полученная в эксперименте зависимость концентрации от высоты n(z) и измеренная независимым способом масса микроскопических частиц m позволили с помощью распределения Больцмана (2.11) рассчитать постоянную Больцмана k. Дальнейшее определение постоянной Авогадро выполнялось по формуле: ![]() , где
, где ![]() - универсальная газовая постоянная. Полученное таким образом значение постоянной Авогадро оказалось близко к установленному позднее более точными методами значению
- универсальная газовая постоянная. Полученное таким образом значение постоянной Авогадро оказалось близко к установленному позднее более точными методами значению ![]() .
.
Проведенные Перреном эксперименты, кроме установления величины постоянной Авогадро, позволили также доказать применимость формулы Больцмана к описанию распределения не только молекул газа, но и любых других микрочастиц.
Распределение Максвелла-Больцмана
Полученные ранее распределения Больцмана и Максвелла позволяют определить соответственно зависимость концентрации молекул от координат n(x, y,z) и функцию распределения по скоростям f(vx, vy, vz ).. При этом распределение Больцмана описывается в пространстве координат x, y, и z, , а распределение Максвелла в пространстве скоростей vx, vy, vz.
Если ввести 6-мерное пространство, координатами молекулы в котором являются величины x, y,z, vx, vy, vz, то функция распределения в таком пространстве будет зависеть от этих шести переменных: nf (x, y,z, vx, vy, vz). Считая пространственные переменные x, y,z и компоненты скорости vx, vy, vz статистически независимыми друг от друга можно записать:
![]() (2.14)
(2.14)
Или
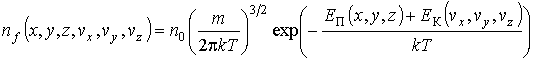 , (2.15)
, (2.15)
где выражение для кинетической энергии имеет вид:
![]() . (2.16)
. (2.16)
Формула (2.15) описывает распределение, называющееся распределением Максвелла-Больцмана. Она может быть использована в случае, когда полная энергия молекулы E равна сумме её потенциальной энергий EП во внешнем силовом поле и кинетической энергии EK её поступательного движения:
![]() .
.
При получении закона распределения Максвелла-Больцмана предполагалось, что температура газа не зависит от координаты точки. В частности, температура газа на всех высотах над поверхностью Земли при термодинамическом равновесии должна быть одинакова. С этим утверждением связан парадокс, всесторонне рассмотренный Максвеллом. Дело в том, что при движении вверх молекулы газа должны затрачивать свою кинетическую энергию на преодоление силы тяжести, и поэтому их средняя кинетическая энергия (а, следовательно, и температура) должна уменьшаться. Но этого не происходит вследствие того, что при этом не все молекулы (из-за недостатка их кинетической энергии) смогут преодолеть силу тяжести. Молекулы, имеющие недостаточную кинетическую энергию, не могут подняться высоко, что приведет, в соответствии с распределением Больцмана, к уменьшению их концентрации с высотой. Поэтому температура газа останется неизменной.
Функция распределения в случае, когда кинетическая энергия зависит только от скорости ![]()
![]()
![]() , а потенциальная - только от радиус-вектора
, а потенциальная - только от радиус-вектора ![]()
![]() частицы, имеет вид:
частицы, имеет вид:

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51 |




