Рис. 34. Формы колоний (вид сверху)
|
|
|
|
|
|
|
|
зование глубинных колоний сопровождается разрывом плотной среды. Еще менее характерны донные колонии, образующиеся при соприкосновении агаризованной среды с дном чашки Петри. Эти колонии обычно имеют вид довольно крупных бесцветных прозрачных налетов.
Описание колонии часто дополняют характером роста микроорганизмов по штриху на поверхности скошенной плотной питательной среды. При этом отмечают его интенсивность — скудный, умеренный, обильный и особенности — налет сплошной с ровным или волнистым краем, четко видный в виде цепочки изолированных колоний, диффузный, перистый, древовидный или ризоид
Рис. 35. Формы колоний (вид сбоку) 
ный. Отмечают оптические свойства штриха, его цвет, поверхность и консистенцию. При описании колонии и роста микроорганизмов по штриху обязательно указывают состав среды и возраст культуры, так как колонии одного и того же микроорганизма на различных средах могут отличаться рядом признаков. В определителях обычно приведены описания колоний и роста микроорганизмов по штриху только на мясопептонном агаре или на мясо-пептонном агаре и мясопептонной желатине.
Рост на картофеле. Многие микроорганизмы растут на ломтиках картофеля и образуют налеты, характерные для представителей данного вида. Особенность роста на картофеле является диагностическим признаком и играет определенную роль при идентификаций. Ломтики картофеля подготавливают в качестве среды следующим образом. Клубни тщательно моют водой, очищают от кожуры и пробочным сверлом вырезают кусочки в форме цилиндра длиной 4...5 см. Цилиндры разрезают по диагонали (на клинья) и для нейтрализации клеточного сока погружают на 1 ч в 1%-й раствор гидрокарбоната натрия (NaHCO3) или скошенную поверхность картофеля натирают мелом. После этого кусочки картофеля помеща
ют в пробирки, на дно которых предварительно положена вата, смоченная водой. Стерилизуют картофель при 50кПа.
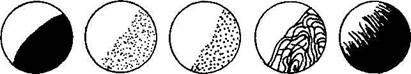
Рис. 36. Края колоний (вид под микроскопом) |
Посев делают петлей, втирая посевной материал в скошенную поверхность картофеля. Отмечают рост микроорганизмов или его отсутствие. Если рост есть, то указывают его интенсивность и характерные особенности, используя те же признаки, что и при описании роста па плотных средах. Особое внимание обращают на образование пигмента.
Рост в жидкой среде. Рост микроорганизмов в жидких питательных средах при стационарных условиях культивирования характеризуется большим единообразием по сравнению с ростом на плотных средах. Он сопровождается помутнением среды, образованием пленки или осадка. Отмечая особенности роста в жидких средах, указывают прежде всего его интенсивность: скудный, умеренный или обильный. Помутнение среды может быть однородным, хлопьевидным или с шелковистой волнистостью.
Если образуется пленка, указывают ее особенности: кольцеобразная или сплошная, тонкая или толстая, плотная или рыхлая, гладкая или складчатая, сухая или слизистая, всползающая или опадающая.
При образовании осадка характеризуют его свойства: скудный или обильный, рыхлый, плотный, хлопьевидный, зернистый или слизистый. Обычно для того чтобы охарактеризовать рост в жидкой среде, используют МПБ. Если изучаемый микроорганизм не растет в МПБ, то подбирают такую жидкую среду, которая подходит для него. Рост в МПБ и в жидких средах описывают, используя 4...7-суточные культуры, выращенные в стационарных условиях.
Тема 6. МЕТОДЫ ВЫДЕЛЕНИЯ ЧИСТОЙ КУЛЬТУРЫ. ОПРЕДЕЛЕНИЕ БИОХИМИЧЕСКИХ СВОЙСТВ МИКРОБОВ
Чистой культурой называют микроорганизмы одного вида, выросшие на питательной среде отдельно от других видов. Часто употребляемый термин разновидность применим к микроорганизмам определенного вида, но отличающегося от последнего каким-либо одним признаком. Штаммом называют культуру одного вида микробов, выделенную из конкретного источника (из органов животного, из корма, пробы почвы, воды и других объектов). Клон — культуры микробов, происходящие из одной клетки.
Выделение чистой культуры. Метод Дригальского. Берут несколько чашек Петри со стерильным МПА, в одну из них на поверхность агара наносят каплю смеси бактерий. Специальным шпателем или пастеровской пипеткой, изогнутой на огне горелки в виде шпателя, растирают каплю по поверхности агара, закрывают крышкой чашку. Этим же шпателем растирают поверхность другой чашки, затем третьей, четвертой и т. д. Чашки помещают в термостат, перевернув вверх дном, чтобы образующийся конденсат не смывал культуру. Самый густой рост будет в первой чашке, в последней чашке обычно получают изолированные друг от друга колонии. Колонии изучают по их внешнему виду, из них готовят бактериологический препарат, окрашивают и микроско-пируют. Отобрав колонию с характерными признаками и соответствующими морфологическими, тинкториальными свойствами для искомого вида возбудителя, из нее бактериологической петлей производят посев в пробирки с МПБ и МПА (отвивка, пересев колонии) для получения чистой культуры одного вида микробов.
Для выделения чистой культуры бактерий часто используют метод, основанный на неодинаковом воздействии химических веществ, антибиотиков, добавленных к питательным средам, на развитие разных видов микробов. Эти вещества, угнетая рост одних видов, не влияют на рост других. На этом принципе основано применение многих элективных сред с красками: яично-крах-мальные среды для выделения микобактерий туберкулеза, глюко-зо-печеночная среда с генцианвиолетом (или кристаллвиолетом) для получения роста бруцелл и подавления роста других видов микроорганизмов.
Метод Пастера. Основан на последовательном разведе: нии в 10 пробирках с жидкой средой капли смеси бактерий с расчетом получить в последней пробирке чистую культуру. Кох, введя в лабораторную практику использование плотных сред, применил принцип Пастера, но разведения производил в плотной расплавленной среде и содержимое каждой пробирки с разным количеством исследуемого материала выливал в отдельную чашку Петри. После выдерживания в термостате в последних чашках с наибольшим разведением обнаруживают изолированные колонии. Пересеяв отдельную колонию в среды в пробирках, культивируя в термостате, получают чистую культуру. При исследовании воды, молока, фекалий и других материалов используют методы, предложенные Пастером и Кохом.
При выделении спорообразующих микроорганизмов, учитывая стойкость спор при нагревании, исследуемый материал (или смесь выросших разных культур) прогревают в водяной бане при 80 °С в течение 30 мин, при этом все вегетативные формы погибают, а споры сохраняются. После прогревания производят пластинчатый посев по Дригальскому с последующей отвивкой колонии. Помимо этого метода при выделении культуры спорообразующего патогенного вида микроба прибегают к биопробе: после прогревания смесь микробов вводят подкожно лабораторному животному (белая мышь, морская свинка); через 1...3сут животное гибнет. Труп вскрывают и из разных внутренних органов пастеровской пипеткой производят посев на питательные среды для получения чистой культуры возбудителя.
Нередко для выделения чистой культуры подвижных видов бактерий используют метод Мечникова и Шукеви-ч а. Каплю исследуемого материала помещают на дно пробирки со скошенным агаром (обязательно в конденсационную воду). Если в смеси с разными бактериями будет находиться подвижный вид микроба (протей, столбнячная палочка и др.), то через 12... 18 ч на поверхности агара появляется рост бактерий искомого вида, пересевом которого с самой верхней части агара достигается получение чистой культуры. Для выделения анаэробов посевы на средах в пробирках, чашках Петри помещают в эксикатор или анаэростат.
Биохимические свойства микробов. Для описания и идентификации микроорганизмов широко используют некоторые особенности их обмена веществ, выявляемые по способности расти на диагностических средах и вызывать те или иные превращения веществ, входящих в состав этих сред. К биохимическим признакам, которые, как правило, необходимы при определении систематического положения различных представителей бактерий, относят способность использовать углеводы, сахара и спирты. Микроорганизмы характеризуются неодинаковой способностью использовать различные углеводы и спирты в качестве единственных источников углерода и энергии.
Для идентификации большинства гетеротоофных микроорганизмов необходимо определить, какие углеводы и спирты обеспечивают рост изучаемого организма и какими изменениями среды он сопровождается. Как правило, для этих целей используют следующие углеводы — арабинозу, ксилозу, глюкозу, фруктозу, галактозу, сахарозу, мальтозу, лактозу, а также спирты— глицерин и маннит. Рост на средах с этими соединениями может приводить к накоплению органических кислот, нейтральных продуктов, газов.
Образование кислот регистрируют по изменению активной кислотности (рН) среды, газа —по появлению на поверхности среды пены и вытеснению среды из поплавка. Углеводы или спирты составляют 1 % основного состава среды. Основой (фоном) среды является водопроводная вода; в нее входят 0,5 % пептона и 0,1 % КНРО4. Чтобы обнаружить изменение рН, к среде добавляют индикатор бромкрезолпурпур из расчета 2 мл 1,6%-го спиртового раствора на 1 л среды: при рН 6,8 индикатор имеет пурпурный, а при рН 5,2 —желтый цвет. Вместо бромкрезолпурпура можно использовать в такой же концентрации бромтимолблау, который при рН 6,0 дает желтый цвет, а при рН 7,6 — синий.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51 52 53 54 |












