Размеры бактерий колеблются от 0,1 до 1 мкм. В состав бактериальной клетки входят капсула, клеточная стенка, цитоплазма-тическая мембрана и цитоплазма, в которой находятся нуклеоид, рибосомы и включения (цв. рис. II).
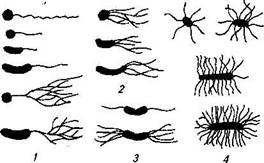
Некоторые бактерии снабжены жгутиками и ворсинками. По типу расположения жгутиков бактерии делят на монотрихи, лофотрихи, амфотрихи и перитрихи (рис. 13)
Морфология спирохет. Спирохеты — извитые подвижные бактерии. Патогенные спирохеты принадлежат к трем родам:
|
Рис. 12. Основные формы бактерий:
/—монококки; 2 — диплококки; 3 — тет-ракокки; 4— стрептококки; 5 —стафилококки; 6— сариины; 7 — бактерии и стреитобактерш; S— плектрщши; д — клострияии; 10— вибрионы; 11 — спириллы; 12 — спирохеты.
Borrelia, Treponema, Leptospira.
Клетка спирохеты имеет цилиндрическую извитую форму, содержит цитоплазму, ограниченную цитоплаз-матической мембраной, снаружи которой расположена клеточная стенка со слабо-выраженным пептидоглика-новым слоем. Длина патогенных спирохет 3...20 мкм, толщина 0,1—0,5 мкм. Представители отдельных родов
отличаются по длине и толщине, числу и характеру завитков. Спирохеты грамотрицательны. Боррелии в отличие оттрепонем и лептоспир хорошо окрашиваются анилиновыми красителями. Морфологию трепонем и лептоспир изучают путем микроскопии живых микроорганизмов в препаратах «раздавленная» или «висячая» капля с помощью темнопольного или фазово-контрастного метода, а также в мазках, окрашенных по Романовскому—Гимза или другими специальными методами.
|
Морфология риккетсий, хламидий и микоплазм. Риккетсии и хламидии являются облигатными внутриклеточными паразитами и представляют собой мелкие грамотрицательные микроорганиз-
Рис. 13. Типы бактерий в зависимости от расположения жгутиков:
/ — монополярные монотрихи;
2— монополярные лофотрихи;
J—биполярные моно - и ло-
фотри)(и; 4— перитрмхи
мы, характеризующиеся выраженным полиморфизмом: образуют кокковидные, палочковидные и нитевидные формы. Размеры рик-кетсий варьируют от 0,5 до 3...4 мкм, длина нитевидных форм достигает 10...40 мкм. Спор и капсул не образуют, окрашиваются по методу Здродовского в красный цвет.
Хламидии имеют шаровидную, овоидную или палочковидную формы. Их размеры колеблются в пределах 0,1 ...2,5 мкм. Морфология хламидии зависит от стадии их внутриклеточного цикла развития, который характеризуется превращением небольшого шаровидного элементарного образования в крупное инициальное тельце с бинарным делением. Перед делением частицы хламидии обволакиваются особой структурой, напоминающей бактериальную капсулу. Хламидии окрашиваются по методу Романовского—Гимза, грамотрица-тельны, хорошо видны в прижизненных препаратах при фазо-во-контрастной микроскопии.
Микоплазм ы отличаются от бактерий отсутствием клеточной стенки: вместо нее у них трехслойная липопротеидная ци-топлазматическая мембрана. Размеры микоплазм колеблются в пределах 125...250 мкм. Они имеют форму круглых, овальных или нитевидных образований, грамотрицательны.
Определение подвижности микроорганизмов.
Для определения подвижности бактерий применяют методы «висячая капля» и «раздавленная капля».
Метод «висячая капля». Каплю 18...20-часовой бульонной культуры или каплю конденсата агаровой культуры наносят на покровное стекло. Специальным предметным стеклом с углублением (луночкой), края которого слегка смазывают вазелином, накрывают каплю культуры так, чтобы покровное стекло прилипло к предметному стеклу. Препарат перевертывают покровным стеклом вверх, и капля «висит» над луночкой (рис. 14).
Микроскопируют препарат в сухой системе объективов при слегка затемненном поле зрения (пользуются диафрагмой и опущенным конденсором). Под малым увеличением находят край капли, затем, приподняв тубус, переводят в рабочее состояние объектив среднего увеличения (40...60), осторожно,
под контролем глаза (смотреть сбоку) опускают тубус до соприкосновения фронтальной линзы объектива с покровным
стеклом. Затем, глядя в окуляр, осторожно поднимают
макрометрическим винтом тубус и находят в поле зрения
каплю. Далее микрометрическим винтом настраивают микроскоп до оптимальной видимости микробов. Рис. 14. Препарат «висячая капля.
|
Метод «раздавленная капля». На обычное предметное стекло наносят каплю суточной бактериальной культуры, осторожно накрывают покровным стеклом так, чтобы между стеклами не образовались пузырьки воздуха, а капля культуры не растеклась за края покровного стекла. Осторожно опускают объектив среднего увеличения и микроскопируют.
В обоих случаях на сероватом фоне поля зрения хорошо заметно движение микробных клеток.
Приготовление красителей и окраска мазков-препаратов. Методы пересева микроорганизмов.
Микроскопируют микробы в живом и неживом состоянии. Для изучения морфологических и тинкториаль-ных свойств микроорганизмов готовят специально окрашенный препарат, применяя для этого различные анилиновые красители.
Краски и красящие растворы. Наиболее часто в микробиологической практике используются следующие анилиновые краски: фуксин (основной), метиловый красный, нейтральный красный — в растворе имеют красный цвет; карболовый кристаллвиолет, ме-тилвиолет, генцианвиолет, готовая жидкая краска Гимза (азур-эозин) фиолетового цвета; метиленовая синь, бриллиантовая и малахитовая зелень.
Из сухих кристаллических или порошкообразных красителей готовят водные или спиртовые растворы красок. Последние обычно готовят впрок, так как они хорошо сохраняются в темноте (посуда из темного стекла, темное помещение). Для усиления действия красящих растворов на микробную клетку используют различные протравители, которые добавляют в раствор красителя (фенол, едкий калий) или ими обрабатывают препарат перед окрашиванием (слабые растворы соляной, серной или хромовой кислот). Также с целью протравливания препарат с налитой на него краской прогревают или заливают предварительно подогретым раствором краски. Краски, нестойкие в растворе, не сохраняющиеся длительное время, готовят только непосредственно перед употреблением в виде 1 ...2%-го раствора.
Спиртоводные растворы. Карболовый фуксин (фуксин Циля). Кристаллы основного фуксина предварительно растворяют в 96%-м этиловом спирте. Сначала готовят насыщенный спиртовой раствор (на 5...10 г краски 100 мл спирта). Для лучшего и более быстрого растворения кристаллы краски предварительно растирают в фарфоровой ступке в небольшом количестве спирта с добавлением нескольких капель глицерина. Чисто спиртовой раствор для окраски непригоден, поэтому готовят спиртоводный раствор: к 10...20 мл насыщенного спиртового раствора фуксина добавляют 100 мл дистиллированной воды с 5 % фенола (протрава). Полученный раствор фуксина фильтруют через фильтровальную бумагу. В ряде случаев фуксин Циля перед использованием разбавляют еще раз дистиллированной водой (1:10) и получают его рабочий раствор (фуксин Пфейффера).
Карболовый кристаллвиолет, метипвиолет, генцианвиолет. Первые два красителя в растворе очень быстро выпадают в осадок и при окрашивании могут исказить микроскопическую картину. Чаще используют генцианвиолет, который получают смешением метил - и кристаллвиолета с добавлением декстрина; он дает более ровное окрашивание. Для приготовления спиртоводного раствора 1 г сухого генцианвиолета растворяют в 10 мл спирта, растирая в ступке с глицерином и кристалликами фенола (2 %), затем добавляют дистиллированную воду. Чтобы избежать образования осадка при хранении раствора, листы фильтровальной бумаги пропитывают насыщенным спиртовым раствором краски, высушивают их на воздухе, нарезают мелкими полосками или квадратиками и сохраняют в темной банке с притертой пробкой.
При окраске препарата на него накладывают высушенную полоску с генцианвиолетом, сверху наливают несколько капель воды, выдерживая 2...3 мин.
Раствор метиленовой сини (щелочная синь Леффлера). Для приготовления раствора 3 г краски настаивают длительное время (3...4 мес) в 100 мл 96%-го спирта, затем 30 мл насыщенного раствора разбавляют в 100 мл дистиллированной воды, содержащей 1 мл!%-го раствора едкого калия (протрава). Фильтруют.
Водные растворы. 2%-й сафранин: 2 г сухого красителя заливают 100 мл горячей дистиллированной воды, фильтруют через бумажный фильтр и сразу используют свежий раствор для окрашивания.
1%-й раствор малахитовой зелени: 1 г кристаллической краски растворяют в 100 мл горячей дистиллированной воды, фильтруют ее, остужают и используют для окрашивания.
Готовую жидкую краску азур-эозин (краска Гимза) применяют при специальных методах окрашивания бактерийных препаратов. Перед употреблением ее необходимо разбавить дистиллированной водой (1:10), но при этом сразу образуется осадок. Чтобы последний не влиял на препарат, окрашивание проводят, по рекомендации Романовского, следующим образом: на дно чашки Петри кладут стеклянные палочки или спички с обломанными головками, на них помещают препарат мазком вниз, раствор краски подливают под препарат (метод Романовского—Гимза).
Приготовление микроскопических препаратов.
Для микроскопического исследования с целью выявления форм микробов, их структурных и биохимических особенностей препарат готовят на предметном стекле. В качестве материала применяют взвеси бактерий; непосредственно бактериальную культуру, выросшую на жидкой или плотной среде; молоко, кровь, гной (препарат-мазок); ткани печени, селезенки или других органов (препарат-отпечаток, кляч-препарат).
Для приготовления препарата на рабочем столе должны быть: исследуемый материал (взвесь бактерий, микробные культуры, гной и др.), обезжиренные предметные стекла, бактериологическая петля, газовая (или спиртовая) горелка, бутыль с сифоном дистиллированной воды, сливная чашка с «мостиком», красители, фиксирующие и протравливающие жидкости.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51 52 53 54 |