Актиномицеты (лучистые грибы). Это одноклеточные растительные организмы, совмещающие в себе признаки бактерий и низших грибов. Гифы мицелия актиномицетов лучезарно разрастают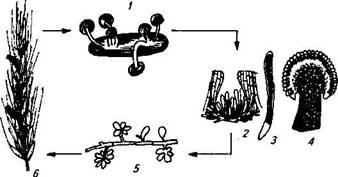
Рис. 25. Цвкл раиитня возбудителя спорыньи Claviceps purpuretr.
/ — проросший склероций с головчатыми стропами; 2—перитеций; 3 —
аск; 4 — головчатая строма в разрезе; 5—гифы с конидиями; 6 —колос
ржи с рожками спорыньи
ся по субстрату (откуда и название лучистые), что сближает их с грибами. Толщина гиф не превышает толщину бактерий, поэтому их также рассматривают под иммерсионной системой микроскопа.
Мицелий субстратный и воздушный. Вначале образуется субстратный, а затем воздушный мицелий, придающий колонии бархатистый вид. Колонии актиномицетов плотной консистенции, прочно сросшиеся с питательной средой, поэтому извлекаются вместе с субстратом. Актйномицеты образуют пигмент и бывают окрашены в разные цвета: розовый, красный, бурый, черный и др. Вид актиномицетов определяют по строению воздушного мицелия. От мицелия отходят спорангиеносцы со спорами на концах (органы плодоношения). Актйномицеты — аэробы, растут на крахмально-аммиачном агаре при 30...35 °С.
Приготовление препарата. Культуру гриба, выращенную на плотной питательной среде, извлекают препаровальной иглой или упругой петлей, наносят на предметное стекло и накрывают таким же стеклом. Раздавливают, разъединяют стекла вдоль поверхности, в результате чего получается два мазка. Культуру, выращенную на жидкой питательной среде, наносят на предметное стекло петлей. Фиксированный мазок окрашивают фуксином Пфейффера.
Микроскопическая картина: тонкие разветвленные нити (гифы), расположенные пучками или тяжами.
Дрожжи. Это безмицелиальные одноклеточные почкующиеся грибы, принадлежащие к классу аскомицетов. Форма клеток разная, но чаще овальная, круглая или лимо но подобная.
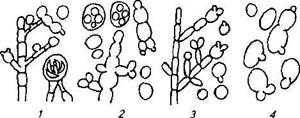
Рис. 26. Форма дрожжей, типы образования асков, мицелия и почкования:
I— Endomycopsis (эски, мицелии, почкование); 2 — Saccharomyces (аски, почкование); 3-Candida (мицелий, почкование); 4— Torutopsis (почкование)
Клетки дрожжей имеют оболочку, цитоплазму и, в отличие от прокариотов, оформленное ядро, которое хорошо видно в неокрашенном препарате. Цитоплазма молодых клеток более однородна: с течением времени появляются вакуоли. Дрожжи крупнее бактериальных клеток, их диаметр колеблется от 10 до 15 мкм. Внутри клеток дрожжей образуются споры (от 4 до 12), после чего они становятся сумками (асками). Различают еще артроспоры, или покоящиеся клетки дрожжей. Они отличаются от вегетативных форм наличием двухконтурной оболочки, большим количеством запасных питательных веществ (гликогена, жира) и отсутствием вакуолей. Размножение дрожжей происходит почкованием, спорами и половым путем (копуляцией) (рис. 26).
Приготовление препарата. Каплю культуры дрожжей, которую готовят заранее, наносят петлей на предметное стекло. Накрывают покровным стеклом и рассматривают под иммерсионной системой микроскопа. Клетки дрожжей видны и при меньшем увеличении (х400), но для сравнения их величины с другими микроорганизмами препарат лучше рассматривать под иммерсионной системой.
Микроскопическая картина: округлые и вытянутые клетки, среди которых могут быть и почкующиеся.
Тема 4. МЕТОДЫ СТЕРИЛИЗАЦИИ
Стерилизация (от лат. sterilis — бесплодие) — обеспложивание, уничтожение патогенных и непатогенных микроорганизмов, их вегетативных и споровых форм в каком-либо объекте. В лабораториях стерилизуют питательные среды, стеклянную посуду (пробирки, пипетки, колбы и др.), инструменты, перевязочный материал, халаты. Для создания специальных условий работы стерилизуют воздух и все предметы в боксах.
Для стерилизации используют физические, химические или биологические средства в зависимости от стерилизуемого материала. Механизм действия при разных способах стерилизации неодинаковый, но в основе каждого из них лежит способность нарушения жизненных процессов микробной клетки: денатурация белков, угнетение функции ферментных систем и др.
В практике применяют полную и неполную стерилизацию. При полной стерилизации уничтожаются вегетативные и споровые формы микроорганизмов, при неполной (частичной) —только вегетативные формы бактерий и вирусы, но с сохранением споровых форм бацилл. При этом обеспечиваются условия, предотвращающие развитие спор (резкое охлаждение).
Физические методы стерилизации. Прокаливание (фламбирование). На огне пламени горелки (газовой или спиртовой) стерилизуют бактериологические петли, пастеровские пипетки, стекла, инструменты (пипетки, иглы и др.).
Стерилизация сухим жаром. Стерилизация сухим нагретым воздухом осуществляется в специальном сушильном металлическом шкафу с двойными стенками (печь Пастера). Снаружи шкаф облицован теплонепроницаемым материалом. В верхней части вмонтирован термометр. Между теплонепроницаемой обшивкой и внутренним металлическим шкафом на дне находится автоматический электронагревательный элемент. Внутри шкафа на металлических сетчатых полочках размещают стерилизуемый материал.
В печи Пастера стерилизуют стеклянную чистую, хорошо промытую, предварительно высушенную посуду. Колбы закрывают ватными пробками, накрывают бумажными колпачками и завязывают. Пробирки, чашки Петри и пипетки завертывают в пергаментную бумагу.
При включении шкафа в электросеть воздух внутри него нагревается. По достижении заданной температуры отмечают время начала стерилизации. Режимы стерилизации: температура 155...ШГС, экспозиция 2 ч; 165...170Х - 1...1,5ч; 180'С—1ч. По истечении времени стерилизации прибор отключают; когда температура'понижается примерно до 45 °С, тогда шкаф открывают.
Воспламеняющиеся вещества, жидкости, питательные среды, резиновые предметы сухим жаром стерилизовать нельзя.
Стерилизация влажным жаром. Кипячение — простой, доступный способ стерилизации в специальных металлических стерилизаторах (или другой чистой посуде). Кипячением стерилизуют иглы, шприцы, пинцеты, ножницы, скальпели и другие инструменты, резиновые и стеклянные предметы, которые раскладывают в стерилизаторах на металлические решетчатые вставки, покрытые 2...3 слоями марли или тонком слоем гигроскопической ваты. Шприцы стерилизуют в разборном состоянии,
|
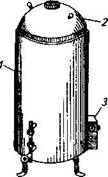
Рис. 27. Текучепаровой аппарат Коха:
/— паровой котел; 2— крышка; 3 — электронагревательный блок
в иглы вставляют мандрены; режущие инструменты—лезвия скальпелей, ножниц следует обертывать марлей или ватой. В стерилизатор наливают воду (желательно дистиллированную), чтобы она полностью покрывала инструменты. Для лучшей стерилизации в воду добавляют 2 % гидрокарбоната натрия (двууглекислой соды). Кипятят в течение 20...25 мин. После стерилизации воду осторожно сливают; инструменты используют только после их охлаждения.
Стерилизацию текучим паром проводят в аппарате Коха (текучепаровой аппарат) (рис. 27), который представляет собой сосуд цилиндрической формы, сверху неплотно закрытый крышкой с отверстием посредине для термометра.
На дне аппарата имеется решетчатая подставка на ножках, до уровня которой наливают воду. На подставку помещают специальное металлическое ведерко также с дном в виде решетки. В это ведерко ставят стерилизуемые питательные среды в пробирках (или маленьких колбочках). Ведерко закрывают неплотно крышкой. При нагревании образующиеся водяные пары, устремляясь вверх, проходят через отверстия в подставке и дне ведерка, обволакивают стерилизуемые пробирки со средами и нагревают их. Стерилизуют в течение 30...40 мин.
Учитывая, что однократная стерилизация данным способом уничтожает только вегетативные формы бактерий, а споры сохраняются, стерилизацию текучим паром осуществляют дробно — три дня подряд. После первой стерилизации материал постепенно остывает при комнатной температуре до следующего дня. Если в культурах имелись споры, они «прорастают» в вегетативную форму. В последующие дни стерилизацию текучим паром повторяют (полная дробная стерилизация). Таким способом часто стерилизуют питательные среды с углеводами, молоко, среды с желатиной, желчью, то есть субстраты, которые не выдерживают нагревания выше 100 °С, длительного действия пара или сухого жара.
Тиндализация — дробная стерилизация в водяной бане при 56..,58 "С в течение 5...6 сут: в первый день прогревают в течение 2 ч, в последующие дни — по 1 ч. Метод был предложен Тиндалем для стерилизации материалов, разрушающихся (денатурирующихся) при нагревании до температуры выше 58...60 °С (коллоидные растворы, сыворотки крови, асцитная жидкость и другие белоксо-держащие вещества).Тиндализацию можно проводить в водяной бане с регулируемой температурой (рис. 28).
Пастеризация— метод неполной стерилизации, предложенный Пастером с целью сохранения питательной ценности пищевого продукта (молоко, мясные, рыбные и овощные консервы), которая снижается при кипячении (разрушаются витамины и другие нестойкие к действию высокой температуры вещества). Продукт нагревают при 80 "С в течение 30 мин, затем резко охлаждают (до4...8°С).
На крупных предприятиях (молокозаводах) применяют специальные пастеризаторы с охладительной системой. Пастеризацией достигается частичная стерилизация, так как убиваются вегетативные формы бактерий, а споры сохраняются. Резкое охлаждение препятствует «прорастанию» спор и последующему размножению бактерий.
Стерилизация паром под давлением
(автоклавирование)~ самый эффективный метод стерилизации (температура выше 100 X). Осуществляют его в специальном аппарате—автоклаве. Принцип стерилизации основан на том, что чистый насыщенный водяной пар при высоком давлении, конденсируясь, повышает температуру внутри котла (автоклава). Уменьшение объема пара после конденсации способствует проникновению его во внутрь стерилизуемого предмета.'

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51 52 53 54 |