|
Принцип действия у «ло-душечных» терморегуляторов основан на том, что плоская
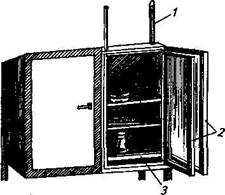
Рнс. 31. Термостат:
контактный термометр; 2—дверцы термостата; 3— полки
латунная гофрированная коробочка с запаянной в ней жидкостью укрепляется таким образом со специальным устройством, что при нагревании выше заданной температуры жидкость в коробочке, расширяясь, оказывает давление на ее стенки и происходит отключение от сети. По мере охлаждения термостата жидкость в коробочке также охлаждается и не давит на ее стенки («подушечки»), поэтому стержень с рычажком, к которому плотно подходит «подушечка», включаются в сеть обогревания.
В современных термостатах обычно применяют контактный терморегулятор — ртутный термометр с впаянными с двух сторон платиновыми проволоками. Один конец проволоки достигает канала термометра, а другой заканчивается снаружи клеммой. Проволоку с помощью наружного магнита располагают на различном уровне от столбика ртути в термометре, и температура автоматически поддерживается в термостате.
Для культивирования анаэробов и микроаэрофильных бактерий используют эксикатор и анаэростат.
Эксикатор представляет собой стеклянный сосуд с притертой крышкой. На его дно ставят часовое стекло или открытую чашку Петри с химическими веществами, которые активно связывают кислород воздуха [например, пирогаллол с гидроксидом (едким натром)]. Сверху на специальный выступ эксикатора кладут фарфоровую подставку с отверстиями, а на нее пробирки или чашки с посевами и плотно закрывают крышку. Для герметичности края эксикатора смазывают вазелином; затем эксикатор помещают в термостат.
|
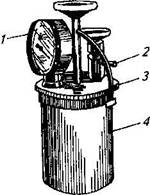
Анаэростат (рис. 32) — металлический герметически закрывающийся цилиндрический сосуд, снабженный кранами для удаления воздуха или подачи нужного для работы газа (СО2, Ni, О2 и др.) и вакуум-манометром. Посевы помещают внутрь цилиндра, закрывают крышкой и с помощью насоса из анаэростата удаляют воздух. Степень разрежения внутри прибора показывает вакуум-манометр в миллиметрах ртутного столба (от 0 до 760). Анаэростат с посевами также ставят в термостат.
Питательные среды. Техника посева микроорганизмов. Любая микробиологическая работа и, следовательно, выполнение любой практической задачи связаны с приготовлением питательных сред для выращивания микроорганиз-
Рис. 32. Анаэростат:
/ — манометр; 2— кран для отвода воздуха; 3 — крышка; 4— емкость для размещения посевов
мов. Среды необходимы для накопления, выделения и сохранения микроорганизмов, а также для выращивания культур с целью исследования их обмена веществ или получения биологических препаратов и ценных продуктов метаболизма.
Среда должна содержать все компоненты, необходимые для конструктивных и энергетических процессов клетки: источники углерода, азота, зольные элементы, микроэлементы. Синтетические возможности микроорганизмов и способы получения ими энергии разнообразны, поэтому очень разнятся их потребности в источниках питания. Следовательно, универсальных сред, одинаково пригодных для роста всех без исключения микроорганизмов, не существует.
Разнообразие обмена веществ микроорганизмов обусловлено источниками углерода и азота; вот почему эти элементы представлены в средах различными веществами и именно они определяют специфичность сред.
Автотрофные микроорганизмы способны использовать в качестве единственного источника углерода диоксид углерода или карбонаты, тогда как потребность в углероде гетеротрофных микроорганизмов данные соединения углерода не могут удовлетворить.
Для развития гетеротрофных микроорганизмов среда должна содержать более восстановленные соединения углерода, которые в зависимости от физиолога-биохимических особенностей организма могут быть представлены различными органическими соединениями, например кислотами, спиртами, углеводами, углеводородами.
Неодинаковы требования микроорганизмов и к источнику азота. В состав всех сред входят различные азотсодержащие соединения. Это могут быть нитраты или соли аммония, одна или несколько аминокислот. Наконец, известны микроорганизмы, нуждающиеся в полном наборе аминокислот или белках.
Потребности разнообразных групп микроорганизмов в зольных элементах и микроэлементах удовлетворяются обычно за счет одних и тех же минеральных солей. Поэтому так называемый «минеральный фон» сред для многих микроорганизмов может быть очень близким по составу.
Кроме элементов, необходимьтх для конструктивных процессов, среда должна содержать и энергетический материал. В средах для культивирования гетеротрофных организмов соединения углерода в большинстве случаев служат и энергетическим материалом. В средах для хемоавтотрофных организмов эту роль выполняют минеральные соли.
Из вышесказанного ясно, что при составлении сред следует обязательно учитывать особенности обмена веществ микроорганизмов. Кроме того, среды для одного и того же микроорганизма могут отличаться в зависимости от цели исследования. Например, среда для длительного сохранения микроорганизма в лабораторных условиях заметно отличается от сред, предназначенных для получения тех или иных продуктов обмена веществ.
Однако какой полноценной ни была бы среда, ее компоненты могут остаться недоступными, если активная кислотность среды (рН) не соответствует значениям, при которых возможно развитие изучаемых микроорганизмов. Поэтому в приготовленной среде проверяют значение рН и, если необходимо, доводят его до нужной величины растворами кислот (HCi, H2SO4), щелочей (NaOH, КОН) или солей, имеющих щелочную реакцию (Na2CO3, >JaHCO5). В процессе стерилизации рН сред может изменяться, поэтому нередко требуется дополнительное определение его в стерильных средах и в случае надобности корректирование стерильными растворами кислоты или щелочи.
i Среды для культивирования в зависимости от состава составляют две группы; 1) естественные (натуральные) среды неопределенного или искусственного состава, 2) синтетические среды. Натуральные среды используют главным образом для поддержания культур микроорганизмов, накопления их биомассы и диагностических целей. Примерами натуральных сред неопределенного состава, которые широко применяют в лабораторной практике, служат мясопептонный бульон, агар, неохмеленное пивное сусло, дрожжевая и картофельная среды.
(Необходимость культивирования микробов обусловлена не только выделением возбудителя болезни из исследуемого материала и определением его вида, но и накоплением микробной массы для изготовления биологических препаратов: вакцин, антигенов и аллергенов. Для культивирования микроорганизмов в лабораторных условиях применяют различные искусственные питательные
среды.
Питательные среды бывают: по консистенции — жидкие, плотные, полужидкие; по происхождению —животного, растительного происхождения и синтетические среды постоянного состава; по назначению —обычные, или простые, для выращивания большинства микроорганизмов; специальные — для культивирования микробов, не растущих или плохо растущих на обычных питательных средах; дифференциально-диагностические — употребляемые для определения родовых или видовых особенностей исследуемых бактериальных культур (гемолитических, сахаролитических, про-теолитических, редуцирующих и других свойств); селективные — для выделения микробов одного рода или вида из материала, содержащего смесь разных видов микроорганизмов, на которых одни виды хорошо растут, а другие не растут; среды обогащения
(накопительные).
Основу многих питательных сред животного происхождения составляет мясная вода. Ее готовят из свежего нежирного говяжьего мяса, не содержащего костей, фасций, сухожилий. Измельченное мясо (мелкие кусочки или фарш) заливают дистиллированной водой в соотношении 1 : 2 (на 1 кг мяса 2 л воды). Экстрагируют 12...24 ч, кипятят 1,5...2 ч, фильтруют, добавляют дистиллированную воду до первоначального объема, разливают в бутыли, колбы, закрывают ватно-марлевыми пробками и стерилизуют в автоклаве.
Обычные (простые) среды. Мясопептонный бульон (МПБ) — жидкая питательная среда. Для его приготовления к I л мясной воды добавляют 1 % пептона, 0,5 % химически чистой поваренной соли и кипятят. Мясная вода слабокислой реакции, поэтому МПБ подщелачивают — добавляют небольшое количество 10—15%-го раствора КОН или NaOH, кипятят 2...3 мин, проверяют рН электропотенциометром. Мясопептонный бульон фильтруют через бумажный фильтр, разливают по пробиркам, автоклави-руют.
Мясопептонный агар (МПА) — плотная питательная среда. К МПБ добавляют 2 % агар-агара (безазотистое органическое вещество, полученное из морских водорослей) и кипятят до его расплавления, в горячем виде определяют рН, кипятят еще 5... 10 мин, фильтруют в горячем виде через ватно-марлевый фильтр, разливают в пробирки или колбочки, автоклавируют. После стерилизации горячие пробирки с агаром укладывают наклонно под углом 5...6 "С: при застывании образуется скошенная плотная поверхность. Для посева на агаровые пластинки его заливают в чашки Петри (рис. 33).
Мясопептонный полужидкий агар готовят так же, как и МПА; различие заключается в том, что агар-агара добавляют меньше — 0,15...0,25 %.
Специальные питательные среды. Бульон Мартена. Свиные желудки (или сычуги рогатого скота) очищают от жира, фасций, измельчают в мясорубке, заливают водой (1 : 4) и добавляют 1 % (к объему жидкости) соляной кислоты. Смесь выдерживают при 50 "С 24 ч, нейтрализуют 20%-м раствором NaOH до щелочной реакции по лакмусу, автоклавируют при 120 X 15 мин. Для приготовления бульона смешивают равные объемы мясной воды и полученной смеси, кипятят 10 мин, подщелачивают 20%-м раствором NaOH до рН 7,9, кипятят 30 мин, фильтруют, разливают в пробирки, автоклавируют при 50,6 кПа (110 °С) 30 мин.
Агар Мартена. Добавление 2 % агара обеспечивает получение плотной среды.
|
Бульон Хоттингера. Готовят из триптического гидро-лизата (перевара) мясных отходов—фасций, жира, сухожилий:

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51 52 53 54 |