Вместе с патологическим материалом направляют сопроводительную, в которой указывают: название хозяйства (адрес); сведения о признаках болезни, применяемых средствах лечения, кормлении животных и уходе за ними; данные об эпизоотической обстановке в прошлом и настоящее время; какие и когда проводились прививки, а также вид и возраст павшего животного; перечень материала, направляемого для исследования; основные патологические изменения в трупе; предполагаемая причина падежа; на какое заболевание необходимо провести исследование.
Поступивший в лабораторию неконсервированный материал можно хранить при 4°С в течение 1...2сут; консервированный в 50%-м растворе глицерина (кусочки органов) — несколько недель; для длительного хранения материал замораживают при —15...—20 С.
Кровь для серологических исследований у крупного рогатого скота, овец, лошадей берут из яремной вены в стерильные бактериологические пробирки в объеме 10... 15 мл, у свиней — из хвостовой, передней краниальной вен или глазного синуса, у птиц — из подкрылковых вен, у кроликов — из краевой ушной вены. Пробирки с кровью выдерживают до формирования сгустка в тепле (1,5...2 ч), затем для отделения от стенок пробирки обводят сгусток стеклянной чистой палочкой или спицей. Для отстаивания
сыворотки пробирки с кровью помещают в холодильник (4...6Х) на 18...20ч. После ретракции сгустка сыворотку крови переливают в серологические пробирки с резиновыми пробками. При необходимости сыворотку крови консервируют, добавляя в пробирку несколько крупинок борной кислоты, тиомерсал (конечное разведение 1 : 10 000), или замораживают.
Принципиальная схема микробиологического исследования.
Диагностика инфекционных болезней включает в себя комплекс исследований: эпизоотологические, клинические, патологоанатоми-ческие, микробиологические. При важности каждого из них и ценности именно комплексного подхода микробиологическое исследование особенно важно, поскольку с его помощью либо непосредственно обнаруживают этиологический (причинный) агент болезни, либо косвенными специфическими иммунологическими методами доказывают его присутствие.
Микробиологическое исследование состоит из следующих этапов;
1. Обнаружение возбудителя непосредственно в исследуемом
материале без изоляции в виде чистой культуры на питательных
средах с помощью разных методов:
неиммунологические методы: а) выявление возбудителя путем микроскопического исследования окрашенных (по Граму и др.) мазков-отпечатков из органов и тканей; б) обнаружение при помощи генетических методов (генные зонды, ПЦР) нуклеиновых кислот возбудителя;
иммунологические методы: выявление антигенов возбудителя с помощью различных серологических реакций (РП, РДП, МФА, ИФА, РИГА и др.).
2. Обнаружение возбудителя (его токсинов) с помощью био
пробы: заражение исследуемым материалом чувствительных лабо
раторных животных.
3. Выделение культуры возбудителя из исследуемого материа
ла путем посева на питательные среды.
4. Идентификация выделенной культуры микроорганизмов по
совокупности морфологических, тинкториальных, культуральных,
ферментативных и патогенных свойств. При этом широко исполь
зуют серологические (РА, РП, РДП, ИФА и др.), а в случае необ
ходимости генетические методы идентификации изолированных
микроорганизмов.
5. Серологическая (ретроспективная) диагностика. Обнаруже
ние специфических следов пребывания возбудителя — антител в
сыворотке крови исследуемых животных при помощи различных
серологических реакций (РА, РСК, ИФА и др.). Серологические
реакции наиболее широко применяют при диагностике хроничес
ки протекающих бактериозов.
Аллергические исследования в отличие от перечисленных выше методов проводят непосредственно на животных в хозяйстве: при помощи диагностических аллергенов выявляют состоя-
![]() ние гиперчувствительности замедленного типа. Аллергическую пробу в основном применяют для иммунологической диагностики хронических бактериозов.
ние гиперчувствительности замедленного типа. Аллергическую пробу в основном применяют для иммунологической диагностики хронических бактериозов.
Изложенная схема отражает возможные, но не обязательные направления микробиологических исследований. При каждой конкретной инфекции схему исследования строят с учетом особенности биологии возбудителя и инфекционного процесса.
Определение патогенности.
Патогенность микроорганизма, выделенного при исследовании патологического материала, определяют с помощью биологической пробы (биопробы), т. е. заражением лабораторных животных: белых мышей и крыс, морских свинок, кроликов, голубей, кошек, а также собак (чаще щенков), кур, мелкого и крупного рогатого скота (телят), обезьян, лошадей и др. Выбор вида животного для биопробы основывается на его восприимчивости к исследуемому объекту. Для биопробы берут не только выделенную микробную культуру, но и непосредственно патологический материал, из которого для этой цели готовят взвесь растертой в стерильной ступке ткани органов, гной, слизь, разбавленные физиологическим раствором. Биологическая проба необходима также при установлении безвредности биологических препаратов (вакцин, сывороток).
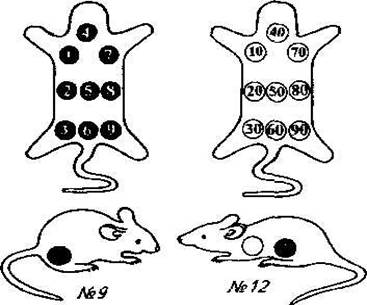
Помещение для содержания лабораторных животных (виварий) должно иметь несколько отделений: карантинное, клиническое для выполнения определенных работ (взятие крови, заражение, вскрытие и др.), кладовую, кухню и др. Перед заражением животных метят: кроликов и морских свинок — металлическими сережками с номерами, белых мышей и крыс — раствором краски (фуксина, метиленовой сини и др.) (рис. 39).
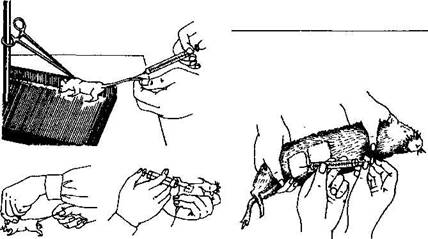
 Для удобства и безопасности работы животных фиксируют (рис. 40 и 41). Морских свинок помощник держит брюшком вверх так, чтобы средний палец левой руки находился на шее, а большой и 'указательный — под передними конечностями, правой рукой при
Для удобства и безопасности работы животных фиксируют (рис. 40 и 41). Морских свинок помощник держит брюшком вверх так, чтобы средний палец левой руки находился на шее, а большой и 'указательный — под передними конечностями, правой рукой при
Рис 39. ключ к мечению зараженных животных
держивают задние конечности. Мышь берут одной рукой за кончик хвоста, другой — за кожную складку затылка, ближе к ушам, и повертывают в удобное для манипуляции положение.
Крыс фиксируют корнцан гами, захватив складку
Рис. 40. Фиксация и заражение мышей |
|
Рис. 41. Фиксация и заражение морских свинок |
кожи затылка, плотно прижимают голову к поверхности стола, другой рукой держат за хвост и поворачивают в удобное положение, оттягивая корнцангом голову.
Животных заражают следующими методами: накожным (скарификация), внутрикожным, подкожным, внутримышечным, внутривенным, внутрибрюшинным, оральным, интраназальным, интрацеребральным и в переднюю камеру глаза. Используемые при этом инструменты (шприцы, иглы и др.) должны быть стерильными.
При скарификации скальпелем делают небольшой надрез кожи — насечку и в нее апплицируют исследуемый материал или бактериальную культуру. Испытуемый материал можно также втирать жесткой щеточкой. Место заражения выстригают и дезинфицируют.
При внутрикожном способе пальцами левой руки оттягивают кожу и в образующуюся между ними кожную складку вводят кончик иглы. Вводимая доза материала не должна превышать 0,2 мл. Показатель правильного введения — небольшая припухлость величиной с горошину.
При подкожном инфицировании пальцами левой руки оттягивают кожу; у кроликов — со стороны спины несколько сбоку, у белых мышей и крыс — со спины ближе к основанию хвоста. В образовавшийся «кармашек»-складку вводят иглу шприца, затем его содержимое. Объем вводимого вещества не должен превышать для мышей 1 мл, для крыс, морских свинок— 10 мл, кроликов — 20...25 мл.
При внутримышечном заражении инъецируемый материал чаше вводят с внутренней поверхности бедра. Голубей и
кур можно заражать также и в грудную мышцу. Доза введения мышам составляет 0,5 мл, морским свинкам и крысам — 3...5 мл, кроликам — 5...8 мл. Большой объем лучше вводить дробно в 2...3 места.
При внутрибрюши ином заражении животное фиксируют головой вниз, иглу шприца вводят в нижнюю треть живота, чуть отступя от белой линии.
Внутривенно исследуемый материал кроликам вводят в краевую вену уха, мышам и крысам — в вену хвоста. Перед заражением место инъекции протирают тампоном, смоченным ксилолом или теплой водой, чтобы вызвать наполнение сосудов кровью.
При интрацеребральном заражении животных фиксируют в спинном положении. У кроликов для этой цели трепанируют череп в участке между надбровным углом и черепным гребнем. Поле операции выстригают, дезинфицируют, пальцами левой руки растягивают кожу над глазницей параллельно черепному гребню и рассекают ее (раздвигают ее края), крестообразно разрезают надкостницу, маленьким трепаном прокалывают черепную кость и извлекают небольшой кусочек ее; из шприца вводят 0,2 мл исследуемого материала. После этого соединяют края надкостницы, края кожной раны заливают коллодием.
У мышей и крыс трепанацию не делают, а легким проколом костной ткани вводят кончик иглы и инъецируют материал.
Интраназально заражение осуществляют капельным способом, используя глазную пипетку. Предварительно животное слегка наркотизируют — к носу прикладывают вату, смоченную эфиром.
При оральном заражении исследуемый материал добавляют в корм, воду или вводят через небольшой зонд.
В случае гибели зараженного животного труп вскрывают, соблюдая правила асептики, и производят бактериологическое исследование.
Для вскрытия труп фиксируют в спинном положении (брюшком вверх) на деревянной доске или лотке с застывшим парафином; конечности растягивают и закрепляют мелкими гвоздиками. Кожно-шерстный покров дезинфицируют 5%-м раствором фенола или лизола. Разрезают кожу вдоль белой линии от промежности до грудино-ключичного сочленения, а затем делают поперечные надрезы (рис. 42). Отпрепарированные кожные лоскуты отводят в сторону. Так же надрезают брюшину, вскрывают брюшную полость, подрезают ребра, диафрагму, вскрывают грудную полость. При вскрытии обращают внимание на патологоанатомическую картину.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51 52 53 54 |