Разведения удобно производить следующим образом. В отдельной пробирке готовят основное (исходное) разведение сыворотки — 1: 25, смешивая 0,1 мл испытуемой сыворотки с добавлением 2,4 мл физиологического раствора. В опытные пробирки разливают по 1 мл физиологического раствора. Затем из исходного разведения 1 мл жидкости переносят в первую опытную пробирку, смешивают с физраствором (разведение 1: 50) и 1 мл переносят во вторую пробирку (1: 100), из второй 1 мл — в третью и т. д. Из последней пробирки 1 мл выливают в сливную чашку, чтобы в каждой пробирке осталось по 1 мл разведенной сыворотки (рис. 44).
Во все пробирки добавляют по две капли стандартного антигена (концентрация 10 млрд микробных тел в 1мл), смешивают встряхиванием и выдерживают в термостате 4...6 ч при 37 °С, а затем при комнатной температуре 14...16 ч.
При постановке РА (как при каждой серологической реакции) обязательны контроли: в тех же разведениях испытывают сыворотку нормальную (от здорового животного) и позитивную (от заведомо больного животного или стандартную биофабричного производства) с тем же антигеном.
|
Компоненты при постановке реакции вносят в пробирки индивидуальными мерными пипетками с резиновыми грушами или дозаторами, групповыми дозаторами (рис. 45...47) и автоматическими пипетками с изменяющимися объемами (5...25Омкл).
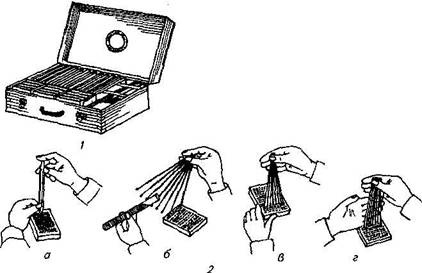
Рис. 45. Многоканальные пипетки для мнкротнтровання: / —оБший вид; 2. а, б, в, г — последовательность работы |
|
|
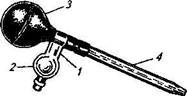
Рис. 46. Одиночная автоматическая пипетка:
/ — стеклянный патрубок; 7—расширение для сбора избыточной жидкости; J — резиновая груша; 4 — пипетка-мерник
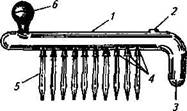
Рис. 47. Групповая автоматическая пипетка:
/ — стеклянный цилиндр; 2 — отверстие для слива избыточной жидкости; 3— приемник для избыточной жидкости; 4 —отверстия нижней части цилиндра; 5— пипетки-мерники; 6— резиновая груша
Для контроля антигена в 1 мл физиологического раствора добавляют две капли антигена для исключения самоагглютинации.
Учет РА осуществляют невооруженным глазом или с помощью агглюти носко па, начиная с контрольных пробирок. Результат РА принято выражать количеством крестов:
++++ (#) —полное просветление жидкости; образовавшийся агглютинат имеет вид перевернутого зонтика, при встряхивании разбивается в глыбки, хлопья разной величины, жидкость остается прозрачной;
+ + +(///) — неполное просветление жидкости; агглютинат, как и в предыдущем опыте, в виде зонтика, при встряхивании разбивается на более мелкие глыбки, комочки;
++(++) — неполное просветление жидкости; агглютинат в виде зонтика, но при встряхивании разбивается на хлопья разной величины, жидкость мутная;
+ — наличие небольшого нехарактерного осадка в виде «пуговки», жидкость над ним мутная. При встряхивании такой осадок легко разбивается, увеличивая мутность;
— (минус) — вся жидкость мутная, на дне пробирки небольшой осадок антигена с ровными краями в виде «пуговки» и при встряхивании разбивается в равномерную муть.
РА в 3...4 креста учитывается как положительная степень проявления агглютинации, в два креста — сомнительная, один крест или отсутствие агтлютината — выражает отрицательный результат. Реакцию оценивают не только по степени выраженности (++ + +, + + + или + +), но и по высоте титров, то есть степени разведения сывороток, давших положительный результат РА. Например, для диагностики бруцеллеза крупных животных диагностическим титром считают положительный результат РА с сывороткой в разведении не ниже 1:100, при сальмонеллезном аборте кобыл — выше 1 : 500.
Капельный (пластинчатый) метод РА. Используют для быстрого обследования поголовья животных в лаборатории и в условиях хозяйства. На чистую стеклянную пластинку наносят микропипеткой исследуемую сыворотку по 0,04; 0,02; 0,01 и 0,005 мл. К каждой сыворотке добавляют по одной капле антигена определенной концентрации, постепенно смешивают чистой стеклянной палочкой, начиная с наименьшего объема сыворотки. Условно считают, что сыворотка в первой капле соответствует разведению 1: 50, во второй — 1:100, в третьей — 1: 200, в четвертой — 1: 400. Через 2...3 мин производят учет. Для ускорения реакции стекло слегка подогревают, держа высоко над пламенем горелки.
Положительный результат проявляется образованием в капле сыворотки комплекса антиген — антитело в виде крупинок, хлопьев и просветлением жидкости. При отрицательном результате капля смеси сыворотки и антигена остается равномерно мутной (отсутствие в сыворотке антител).
Пластинчатым методом РА пользуются также для ориентировочного определения вида микроба или его идентификации (типизации). На предметное стекло наносят каплю известной специфической сыворотки и отдельно каплю физраствора (для контроля). В каждую каплю добавляют культуру испытуемого микроба в количестве, взятом бактериологической петлей, и равномерно размешивают. Положительная реакция указывает на гомологич-ность антигена с известным антителом.
Кровяно-капельный метод РА. Реакцию чаще применяют для диагностики пуллороза (сальмонеллеза птиц) и бруцеллеза. На обезжиренное предметное стекло наносят каплю цельной крови (взятой у птиц из гребешка или сережки), в нее добавляют каплю соответствующего антигена и смешивают стеклянной палочкой. Для лучшей видимости феномена агглютинации биопромышленность выпускает антиген, подкрашенный гематоксилином.
В положительных случаях РА (когда в крови присутствуют специфические антигену антитела) через 30...60 с в капле смеси появляются глыбки, хлопья склеенного антигена (агглютинат).
Кольцевая проба (реакция) с молоком. В основном используют при обследовании крупного рогатого скота на бруцеллез и при контроле сборного молока. В агглютинацион-ные пробирки наливают по 2...3 мл свежего цельного молока и добавляют антиген (окрашенный гематоксилином) по 0,2 мл (2 капли). Пробирки встряхивают до равномерного окрашивания молока, выдерживают в водяной бане (или термостате) при 37 °С в течение 45.60 мин. При наличии в молоке антител образуется комплекс антиген—антитело, который адсорбируется на капельках жира и при отстаивании всплывает наверх, образуя синее кольцо в нижнем слое сливок; столбик молока обесцвечивается.
Отрицательная реакция характеризуется синей окраской всего молока в пробирке и слегка желтоватым слоем сливок.
РА методом адсорбции антител (по Касте л л а н и). У некоторых микробов наряду со специфическими видовыми антигенами имеются еще групповые, общие с другими видами одного рода или семейства бактерий. При введении в организм животного (и человека) таких бактерий (например, сальмонелл) образуются антитела как против видоспецифических, так и групповых (общих для разных видов) антигенов. Если в реакции участвует микроб, обладающий групповым и типовым антигенами, то происходит полная агглютинация общих (групповых) и тииоспе-цифических антигенов, при этом из сыворотки все антитела адсорбируются. Если антиген не типоспецифичен антителам, происходит реакция агглютинации за счет групповых антигенов и групповых антител, типоспецифические антитела в сыворотке остаются.
Адсорбированные групповые антитела удаляют; сыворотки с групповым агглютинатом центрифугируют, а надосадочную жидкость (сыворотку с оставшимися типоспецифическими антителами) отсасывают и вновь используют в РА. Так как сыворотка, истощенная групповыми антигенами, содержит только специфические антитела, она будет реагировать положительно лишь со специфическим антигеном. На этом принципе основан метод' получения монорецепторных сывороток.
Реакция Кумбса. В ряде случаев при постановке РА выпадения агглютината не происходит. Одной из причин этого является наличие в сыворотке больных животных наряду с полными антителами так называемых неполных или блокирующих антител, которые тормозят образование агглютината (выпадение комплекса антиген—антитело в виде осадка). Методика выявления неполных антител в организме больного разработана Кумбсом.
Прямая реакция Кумбса (рис. 48) заключается в том, что к эритроцитам больного животного добавляют специфическую антигло-булиновую сыворотку (содержащую антитела против глобулинов сыворотки). Эритроциты агглютинируют. При непрямой реакции исследуют сыворотку больного, которую соединяют с эритроцитами здорового животного, затем, как и при прямом методе, добавляют антиглобулиновую сыворотку. Блокирующие (неполные) антитела соединяются с эритроцитами, и добавленная антиглобули-новая сыворотка, вступая в реакцию с неполными антителами, приводит к агглютинации эритроцитов, нагруженных неполными антителами.
Для диагностических целей в ветеринарии разработана удобная модификация методики реакции Кумбса — бактерийный вариант, в котором вместо эритроцитов применяют специфический бактерийный антиген.
Бактерийный вариант реакции Кумбса. С исследуемыми сыворотками ставят обычную РА. После учета результата реакции в пробирки, в которых отсутствует агглютинация, добавляют по 2 мл физраствора и центрифугируют при 4000 мин~' в течение 15 мин. Надосадочную жидкость удаляют, к осадку добавляют 1 мл антиглобулиновой сыворотки в рабочем титре (установлен предварительно). Центрифужные пробирки встряхивают, содержимое переносят в агглютинационные пробирки, ставят их в термостат при 37...38 °С на 16...48 ч, а затем выдерживают еще 1 ч при комнатной температуре. Учет производят по характеру агглютината, как при обычном методе РА. Реакция Кумбса очень чувствительная и позволяет более точно выявлять больных.
Реакция гемагглютинации (РГ А). Основана на том, что некоторые виды бактерий и вирусов обладают способностью адсорбироваться на поверхности эритроцитов разных видов животных (и птиц), вызывая их склеивание и образование агглютината (прямая РГА).

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51 52 53 54 |